基本介紹
- 中文名:骨橋蛋白
- 外文名:osteopontin
- 類別:蛋白質
- 適用範圍:醫學研究
- 分布:組織和細胞中
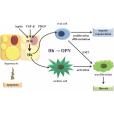
OPN(一種高度糖基化和磷酸化的酸性活性蛋白)一般指本詞條
OPN是母乳中重要的活性物質,具有調節免疫、促進腸道發育等多種生物學意義,是嬰兒早期發育重要的營養支持。母乳活性成分是指天然存在於母乳中的,具有生物學效應的成分,比如以免疫球蛋白、OPN活性蛋白、溶菌酶、脂肪球膜蛋白為代表的活性蛋白類,還包括細胞因子、生長因子寡聚糖、益生菌、OPO、gsMO、a-lac等成分。...
OPN,智慧型助聽器,OPN內置高速處理器,以每秒一百次頻率分析接收到的聲音。2016年7月,英國老牌助聽器廠商Oticon宣布將推出能聯網產品OPN。佩戴者可“聽到”各種智慧型家居用品的聲音,如門鈴、煙霧偵測器和嬰兒監視器等,甚至是推特新訊息提示。OPN內置高速處理器,以每秒一百次頻率分析接收到的聲音,讓配戴者聽到來自四方...
OPN OPN是一家主要從事金融科技的企業,掌門人 / 聯合創始人Jun Hasegawa。領導團隊 掌門人 / 聯合創始人:Jun Hasegawa。所獲榮譽 2024年4月9日,OPN以71億人民幣的企業估值入選《2024·胡潤全球獨角獸榜》,排名第1118名。
骨橋蛋白(Osteopontin,OPN)是一種分泌型的磷酸化糖蛋白,參與多種惡性腫瘤的發生和轉移。人OPN通過選擇性剪接產生三種剪下體,其功能與機制尚不清楚。我們前期研究發現OPN在肝癌侵襲轉移中發揮重要作用,可作為預後指標和干預靶點,並初步發現三種剪接體在肝癌的發生髮展中可能扮演不同的角色。本項目擬在前期研究的...
《骨橋蛋白與類風濕性關節炎的免疫病理機理研究》是依託上海交通大學,由臧敬五擔任項目負責人的面上項目。項目摘要 骨橋蛋白(OPN)是最新發現的具有十分重要生理與病理作用的分子。在體內具有很強的炎症趨化作用,OPN的表達與T細胞、單核細胞在肉芽腫性炎症、間質性腎炎以及肺纖維化等炎症病變的浸潤相關。在炎症與...
骨橋蛋白(OPN)是一種多功能的細胞外基質糖蛋白,研究提示OPN與子宮蛻膜化和胚胎生長發育有關,但機制還不清楚。本項目擬建立人子宮內膜基質細胞體外誘導蛻膜化模型和小鼠體內、體外研究模型,採用RNA過表達和干涉技術,結合生物信息學算法,利用啟動子分析、染色質免疫共沉澱和靶基因驗證等方法,研究在著床和蛻膜化...
《非小細胞肺癌OPN對TAM的功能調控研究》是依託天津醫科大學,由孫冰生擔任項目負責人的青年科學基金項目。中文摘要 腫瘤間質中浸潤的巨噬細胞(TAM)在非小細胞肺癌(NSCLC)侵襲轉移中的作用尚存爭議。不同研究的結果並不一致,甚至相反。儘管有報導提示TAM存在抑制和促進腫瘤發展兩大亞群,然而如何鑑別這些亞群至今尚...
《嬰幼兒食品和乳品中骨橋蛋白的測定高效液相色譜法》是中國飛鶴聯合國家奶業科技創新聯盟、中國農業科學院北京牧醫所等單位共同完成制定的國際首個嬰幼兒食品和乳品中骨橋蛋白(OPN)檢測方法標準。該方法標準於2023年發布。簡介 《嬰幼兒食品和乳品中骨橋蛋白的測定高效液相色譜法》,是國際首個嬰幼兒食品和乳品中骨...
《從Wnt通路靶向調節OPN探討骨關節炎發病的分子機制》是依託中南大學,由高曙光擔任項目負責人的青年科學基金項目。項目摘要 骨關節炎(OA)是一種累及軟骨、滑膜和軟骨下骨等結構的疾病。Wnt/β-catenin通路與軟骨細胞功能行為等密切相關,我們曾證實Wnt抑制因子1、β-catenin與軟骨退變程度相關。OPN是一種糖蛋白,我們...
《骨橋蛋白OPN對肝再生中肝細胞增殖的作用研究》是依託河南師範大學,由王改平擔任項目負責人的青年科學基金項目。項目摘要 骨橋蛋白(OPN)通過促進炎症反應、細胞增殖或遷移而參與多種肝病的發生,但作為急性期蛋白、炎性細胞因子的OPN是否參與促進肝再生中的細胞增殖缺乏研究。前期工作發現OPN具有顯著促肝再生作用。而...
《骨橋蛋白在小鼠胚胎著床中的作用和調節機制》是依託武漢大學,由謝青貞擔任項目負責人的面上項目。項目摘要 採用纖連蛋白(FN)鋪板、體外胚胎培養技術,建立小鼠假孕、人工蛻膜化、延遲著床或延遲著床激活等模型,套用間接免疫螢光、定量PCR和Western blot等方法檢測小鼠胚胎和子宮內膜骨橋蛋白(OPN)的mRNA和蛋白水平...
《骨橋蛋白在腸道微生態調節肝損傷中的作用及機制研究》是依託浙江大學,由刁宏燕擔任項目負責人的面上項目。項目摘要 腸道微生態與肝病發生髮展存在密切關係。闡明腸道微生態調節肝病的免疫機制是最佳化肝病治療的迫切需要。骨橋蛋白(OPN)作為一種細胞因子, 在肝病發展過程中發揮重要作用。我們前期實驗發現腸道致病菌...
《骨橋蛋白在樹突狀細胞對B肝病毒識別中作用的研究》是依託浙江大學,由刁宏燕擔任項目負責人的面上項目。項目摘要 慢B肝是肝硬化和肝細胞癌的主要病因,且B肝慢性化機制不甚明了。樹突狀細胞(DC)的成熟障礙和抗原提呈功能缺陷是機體無法發揮免疫清除效應的主要原因之一。闡明DC功能的調節機制是治療慢B肝的迫切...
《骨橋蛋白(OPN)對TLR3/4和RIG-I介導的IFN-β表達的調控作用及機制》是依託山東大學,由高成江擔任項目負責人的面上項目。中文摘要 I型干擾素在抗病毒感染中發揮重要作用,但其分子調節機制仍不是完全清楚。我們前期實驗發現,LPS和poly(I:C)均可誘導巨噬細胞中骨橋蛋白OPN的表達;OPN缺...
《骨橋蛋白在Graves'病甲亢中致病機制的研究》是依託上海交通大學,由王曙擔任項目負責人的面上項目。項目摘要 Graves'病甲亢(GD)是一種常見的自身免疫性內分泌疾病,是由於促甲狀腺激素受體自身抗體(TRAb)升高所致,其主要治療方法- - 抗甲狀腺藥物(ATD)療程長,復發率較高。要改善治療方法、縮短療程,就必須...
《OPN/IRF1/HOTAIR通路對125I 粒子放射生物效應的作用及分子機制》是依託中山大學,由高飛擔任項目負責人的面上項目。中文摘要 降低放射抵抗、提高放射生物效應是125I粒子治療實體瘤的難題。我們已證實125I粒子照射後腫瘤進展組織中OPN的表達升高,並證明OPN可降低放射生物效應。那么OPN下調粒子放...
《OPN和BSP對骨內植入材料界面巨噬細胞免疫回響的調控》是依託武漢大學,由夏海斌擔任項目負責人的面上項目。項目摘要 骨內種植體植入體內早期反應的主導細胞是巨噬細胞。與聚合物-骨界面的巨噬細胞持續存在與融合不同,鈦-骨整合界面早期的巨噬細胞則快速消失。鈦植入骨內後先形成OPN和BSP為主的粘合線蛋白層,而...
《整合素αvβ3及其配體OPN在胚胎著床中的作用機制研究》是依託揚州大學,由張曉梅擔任項目負責人的青年科學基金項目。項目摘要 胚胎著床是一個複雜的過程,包括定位、黏附、入侵併最終植入子宮內膜。著床成功的必要條件是胚胎的成熟和子宮內膜容受性的建立。許多分子參與調節胚胎著床過程的建立,但詳細的分子機制仍不清...
《NK細胞通過分泌IFN-γ和OPN誘導肝臟胰島素抵抗》是王福艷為項目負責人,寧波大學為依託單位的青年科學基金項目。項目摘要 肝臟是糖和脂代謝的重要器官,肝臟胰島素抵抗對2型糖尿病(T2DM)發病非常重要,但其影響因素並不明確。肝臟又是重要的免疫器官,含有NK細胞、NKT細胞、枯否細胞等多種固有免疫細胞。NK細胞對於...
光分組(OPN)網是在光域上實現分組交換技術的智慧型光網路,大致可分為三層,其中底層是物理層,與光纖鏈路的物理特性直接相關;頂層是業務層,由異步轉移模式(ATM)、同步數字型系(SDH)相應地,OPN的基本功能可總結為波長交換、光分組路由、流量控制、衝突排除、同步、信頭識別與處理、級聯能力等,這些功能由OPS...
“全媒體傳播網”,傳播“全媒體”新概念。“全媒體”在英文中為“omnimedia”,為前綴omni和單詞media的合成詞。“全媒體傳播網”域名取英譯“Omnimedia Propagation Network”每個單詞第一個字母,組合為“opn”。基本解釋:“全媒體”指媒體機構、經過記者採訪,編輯,及運營商採用文字、圖形、圖像、動畫、網頁、...
Emmanual Unni等2004年進行的小鼠動物模型測定了甲基源硒抗TM6小鼠乳腺增生贅疣(TM6-HOG)的效果和測定該模型系統中甲基源硒的體內靶標。結果表明3ppm硒顯著降低乳脂墊中細胞增殖、誘導半胱天冬酶-3活性、和乳腺腫瘤中骨橋蛋白基因(OPN)表達。OPN是一個分泌的含RGD(精氨酸-甘氨酸-天冬氨酸)的磷蛋白,它與...
啟賦3蘊淳是惠氏營養品旗下的超高端品牌啟賦3,推出的全新產品線。全新上市的啟賦蘊淳富含突破性OPN活性蛋白,能進入腸道與血液循環,突破性激活全身免疫細胞,,有效減少寶寶50%發熱發生率,給寶寶帶來初乳般免疫保護。 2023年2月,惠氏啟賦蘊淳通過新國標註冊。 啟賦3蘊淳配方 新國標啟賦還使用了獨創的科研專利工藝...
BSP、OPN(骨橋蛋白) 能和補體因子H形成緊密的複合體,有可能導致補 體不能發揮作用。Fedarko報導了重組BSP和OPN能阻止鼠白血病細胞被人補體系統的攻擊,表現 出這一特徵的還有人MCF-7乳癌細胞和U-226骨髓 瘤細胞。在使用特定多肽和抗體阻斷BSP和OPN的活性實驗中確定了腫瘤細胞逃避監視的這一機 制。基因表達...
《處理器寶典之AMD篇》是一個電腦程式語言教程。基本信息 AMD CPU編碼的秘密 CPU身上的OPN代碼是CPU所有特性的表達,但是這種OPN代碼是CPU廠商自家生產時的標記,長長一串的代碼表示了CPU所屬的類別,針腳數目,最高電壓、最高溫度、核心的製程和核心的名稱,由於同一接口型號的CPU,由於周期的不同,可能使用了不同的...
啟賦有機奶粉是惠氏於2017年推出的有機奶粉。啟賦有機的奶源源自全球黃金奶源地——阿爾卑斯高山有機牧場,有機牧草0激素,0化肥,0農藥。在配方上,啟賦有機是啟賦推出的首款【有機活性蛋白OPN】配方,啟賦有機通過中國/歐盟/愛爾蘭三重國際權威有機認證。 2023年2月,惠氏啟賦蘊萃通過新國標註冊。 品牌介紹...
1.骨橋蛋白(OPN)對肝再生中肝細胞增殖的作用研究,國家青年科學基金項目,2013/01-2015/12,主持。2.重組胰島再生源蛋白RegIIIγ的真核表達及活性研究,河南省重點研發與推廣專項,2018-2019,主持。3.大鼠再生肝肝細胞的蛋白質組學研究,河南省基礎與前沿技術研究項目, 2012-2014,主持。4.骨橋蛋白(OPN)對...
