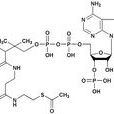
生化意義,乙醯輔酶A,分解代謝,糖酵解,丙酮酸的去路,糖酵解的調節,糖酵解的分支,氧化分解,甘油的氧化分解,脂肪酸的氧化,生成利用,酮體的生成,酮體的利用,生理意義,分解代謝,三羧酸循環,脫氨基作用,α-酮酸代謝,氨的代謝,徹底氧化,三羧酸循環,氫的燃燒,NADH的氧化,ATP的總結算,
生化意義 乙醯輔酶A是人體內重要的化學物質。首先,丙酮酸氧化
脫羧 ,脂酸的
β-氧化 的產物。同時,它是脂酸合成,膽固醇合成和
酮體 生成的碳來源。
三大營養物質 的徹底氧化殊途同歸,都會生成乙醯輔酶A以進入三羧酸循環。
乙醯輔酶A 乙醯輔酶A是能源物質代謝的重要中間代謝產物,在體內能源物質代謝中是一個樞紐性的物質。糖、脂肪、蛋白質三大營養物質通過乙醯輔酶A匯聚成一條共同的代謝通路——三羧酸循環和
氧化磷酸化 ,經過這條通路徹底氧化生成二氧化碳和水,釋放能量用以ATP的合成。乙醯輔酶A是
合成脂肪酸 、酮體等能源物質的
前體物質 ,也是合成膽固醇及其衍生物等
生理活性物質 的前體物質。
分解代謝 糖是多羥基醛和多羥基酮及其衍生物的總稱。人體最重要的
單糖 是葡萄糖(glucose),葡萄糖是糖在體內的運輸形式;人體最重要的多糖是
糖原 ,糖原是葡萄糖在體內的儲存形式;食物中的多糖主要是澱粉,澱粉由澱粉酶水解為葡萄糖後才能吸收,經血液運往全身各組織被利用或儲存。糖的主要生理功能是氧化供能,每克糖徹底氧化可釋能16.7 kJ(4kcal),一般由糖氧化供給的能量約占人體所需總能量的50%~70%。
【
糖的有氧氧化 】葡萄糖→
丙酮酸 →乙醯輔酶A→CO2+H2O。此過程在只能有
線粒體 的細胞中進行,並且必須要有氧氣供應。糖的有氧氧化是機體獲得ATP的主要途徑,1分子葡萄糖徹底氧化為二氧化碳和水可合成30或32分子ATP(過去的理論值為36或38分子ATP)。
【糖的無氧氧化】葡萄糖→丙酮酸→乳酸。在細胞無線粒體或缺乏
氧氣 時進行,1分子葡萄糖氧化產生2分子乳酸,淨合成2分子ATP。此過程產生的乳酸如果積累過多會導致乳酸酸中毒。
【糖原合成】葡萄糖→
肝糖原 、肌糖原。糖原是機體糖的貯存形式,但由於糖原的貯存需要水的存在,因此貯存量較小,也正因為糖原親水,所以糖原的利用速度比脂肪快。
【糖轉化為脂肪】葡萄糖→乙醯輔酶A→脂肪酸→脂肪。這是糖轉化為脂肪的途徑,脂肪是機體高度還原的能源貯存形式,疏水,可以大量貯存,但利用速度較慢。
糖酵解 葡萄糖或糖原的葡萄糖單位通過糖酵解途徑分解為丙酮酸,這個過程稱為糖的無氧分解。由於此過程與
酵母菌 使糖
生醇發酵 的過程基本相似,故又稱糖酵解(圖5-1-3)。反應在胞液中進行,不需要氧氣。
糖酵解的反應過程可分兩個階段:①活化吸能階段,通過消耗2分子ATP使1分子葡萄糖裂解為2分子3碳糖。②3碳糖氧化釋放能量階段,產生2分子丙酮酸、2分子
NADH 和4分子ATP。糖酵解過程淨產生ATP 2分子(圖5-1-4)。
在
糖酵解 進行過程中,有三種
酶催化 的反應不可逆,這三個酶稱為
關鍵酶 ,它們使糖酵解由葡萄糖向丙酮酸方向進行。
【
己糖激酶 】或肝中【
葡萄糖激酶 】催化葡萄糖
磷酸化 生成6-磷酸葡萄糖,由ATP提供能量和磷酸基團。這一步反應不僅活化了葡萄糖,使其能進入各種
代謝途徑 ,還能捕獲進入細胞內的葡萄糖,使之不再透出細胞膜。反應不可逆,反應過程中消耗1分子ATP。己糖激酶或葡萄糖激酶是
糖酵解途徑 的第一個
限速酶 。
【
磷酸果糖激酶 -1】催化6-磷酸果糖轉變為
1,6-二磷酸果糖 ,這是酵解途徑中的第二個磷酸化反應,需要ATP和Mg,反應不可逆。磷酸果糖激酶-1是
糖酵解 過程中最重要的限速酶。此酶為變構酶。檸檬酸、ATP為變構抑制劑,ADP、
AMP 和 F-1,6-BP等為變構
激活劑 。
胰島素 誘導其生成。
【
丙酮酸激酶 】催化
磷酸烯醇式丙酮酸 轉變為丙酮酸,磷酸烯醇式丙酮酸的高能磷酸鍵在催化下轉移給ADP生成ATP,自身生成烯醇式丙酮酸後自發轉變為丙酮酸。反應不可逆。是
糖酵解途徑 中第二個以底物水平磷酸化方式生成ATP的反應。丙酮酸激酶是糖酵解途徑中的又一個限速酶,具有
別構酶 特性,ATP是其
別構抑制劑 ,ADP是
別構激活劑 。
在
糖酵解 過程中有2步反應生成ATP,其一是在
磷酸甘油酸激酶 催化下將1,3-二磷酸甘油酸分子上的1個
高能磷酸鍵 轉移給ADP生成ATP;另1個是
丙酮酸激酶 催化使磷酸烯醇式丙酮酸的高能磷酸鍵轉移給ADP生成ATP。這兩步反應的共同點是底物分子都具有
高能鍵 ,底物分子的高能鍵轉移給ADP生成ATP的方式稱為【
底物水平磷酸化 】。底物水平磷酸化是ATP的生成方式之一,另一種ATP的生成方式是氧化過程中脫下的氫(以NADH和FADH2形式存在)線上粒體中氧化成水的過程中,釋放的能量推動ADP與磷酸合成為ATP,這種方式稱為【氧化磷酸化】(見本章第二節)。
丙酮酸的去路 糖酵解過程的產物丙酮酸有多種分支去路
1.生成乙醯輔酶A:丙酮酸在有氧氣和線粒體存在時進入線粒體,經
丙酮酸脫氫酶複合體 (表5-1-2)催化氧化脫羧產生NADH、CO2和乙醯輔酶A,乙醯輔酶A進入三羧酸循環和氧化磷酸化徹底氧化為CO2和H2O,釋放的能量在此過程中可產生大量ATP。這是糖的有氧氧化過程。糖的有氧氧化是機體獲得ATP的主要途徑。
丙酮酸生成乙醯輔酶A的反應是
糖有氧氧化 過程中重要的不可逆反應。丙酮酸脫氫產生NADH+H,釋放的
自由能 則貯於乙醯輔酶A中。乙醯輔酶A可參與多種
代謝途徑 。
2.丙酮酸在無氧或無線粒體條件下加氫還原為乳酸。
糖酵解 過程生成的產物有3個:NADH、ATP和丙酮酸。NADH、ATP的生成必將導致底物NAD和ADP的顯著減少,而這兩種底物的減少將嚴重抑制糖酵解的繼續進行。ATP在體內會很快被消耗而生成ADP和磷酸,因此ATP的抑制作用幾乎可以忽略不計。NADH在有氧氣存在的條件下線上粒體中被氧化為水而重新生成NAD,但在無氧或無線粒體的細胞中是無法進行這個過程的,因此NAD的減少和NADH的增多在無氧或無線粒體的細胞中對糖酵解的抑制非常顯著。在這些細胞中解決的辦法是,產物丙酮酸作為受氫體將NADH的氫接受重新生成NAD, 丙酮酸加氫還原為乳酸。
乳酸的生成使NAD再生,能在一定時間內暫時解除
糖酵解 的抑制,但是如果乳酸進一步增多,乳酸的抑制作用將增強,最後糖酵解被完全抑制。同時乳酸解離產生的H也增多,體液pH下降。這些綜合結果被稱為【
乳酸酸中毒 】。在缺氧和劇烈運動時最容易產生乳酸中毒現象。乳酸中毒的解除需依賴氧氣的充分供應,此時,乳酸可脫氫生成丙酮酸通過有氧氧化代謝或進入肝臟進行
糖異生 。
紅細胞缺乏線粒體,因此,紅細胞只能依賴糖的無氧氧化(
酵解 )獲得能量,所釋放的乳酸經血液循環至肝臟代謝(糖異生)。某些組織細胞如視網膜、睪丸、白細胞、腫瘤細胞等,即使在有氧條件下仍以糖酵解為其主要供能方式。
機體在缺氧情況下,尤其在劇烈運動時肌肉的氧分得不到足夠供應(儘管此時氣喘吁吁),糖的無氧氧化(葡萄糖→乳酸)是機體獲得能量的一種有效方式,但無法維持很長時間,如果導致嚴重的乳酸中毒,又不能恢復氧氣供應,
糖酵解 被完全抑制,ATP消耗不能再生,生命過程將終止。
3.丙酮酸經轉氨基作用生成丙氨酸,作為蛋白質合成的原料。
4.在植物和酵母菌細胞內,無氧情況下丙酮酸脫羧產生乙醛,乙醛由NADH還原為乙醇(乙醇發酵)。乙醇發酵有很大的經濟意義,在發麵、製作麵包和饅頭,以及釀酒工業中起著關鍵性的作用。在釀醋工業上,微生物也是先在不需氧條件下形成
乙醛 而後在有氧條件下氧化為乙酸(醋酸)。
糖酵解的調節 正常生理條件下,人體內的各種代謝過程受到嚴格而精細的調節,以保持內環境穩定,適應機體生理活動的需要。這種調節控制主要是通過改變酶的活性來實現的。己糖激酶(葡萄糖激酶)、
磷酸果糖激酶 -1、
丙酮酸激酶 是糖酵解的關鍵酶,它們的活性大小,直接影響著整個
代謝途徑 的速度和方向,其中以磷酸果糖激酶-1最為重要。
1.激素的調節 胰島素可誘導GK、PFK-1、PK的合成,因而使糖酵解過程增強。
2.
代謝物 對限速酶的
變構調節 磷酸果糖激酶-1(PFK-1)是三個限速酶中催化效率最低的,故而是
糖酵解途徑 中最重要的調節點。該酶分子為四聚體。分子中不僅具有與底物結合的部位,還具有與變構激活劑和變構
抑制劑 結合的部位。F-1,6-BP、ADP、AMP等是其變構激活劑,而ATP、檸檬酸等為其變構抑制劑。在這些代謝物的共同調節下,機體可根據能量需求調整糖分解速度。當細胞內能量消耗增多,ATP濃度降低,AMP、ADP濃度增加,則磷酸果糖激酶-1被激活,糖分解速度加快,使ATP生成量增加;當細胞內有足夠的ATP儲備時,ATP濃度增加,AMP、ADP濃度下降,磷酸果糖激酶-1被抑制,糖分解速度減慢,減少ATP生成量,避免能量的浪費;當飢餓時,機體動員儲存脂肪分解氧化,生成大量乙醯CoA,乙醯CoA可與草醯乙酸縮合成檸檬酸,抑制磷酸果糖激酶-1的活性,從而減少糖的分解,以維持飢餓狀態下血糖濃度。
糖酵解的分支 磷酸戊糖途徑(pentose phosphate pathway)由6-磷酸葡萄糖開始,全過程可分為二個階段:第一階段是6-磷酸葡萄糖脫氫氧化生成NADPH+H 、CO2和5-磷酸核糖。第二階段為一系列基團轉移反應。
1.反應過程(圖5-1-6)
(1)5-磷酸
核糖 生成 6-磷酸葡萄糖在6-磷酸葡萄糖脫氫酶和6-磷酸葡萄糖酸脫氫酶相繼催化下,經2次脫氫和1次脫羧,生成2分子NADPH+H 和1分子CO2後生成5-磷酸
核酮糖 ,5-磷酸核酮糖經
異構酶 催化轉變為5-磷酸核糖。
(2)基團移換反應 此階段由4分子5-磷酸
木酮糖 和2分子5-磷酸核糖在轉
酮基 酶、轉醛基酶催化下,通過一系列反應,最後生成4分子6-磷酸果糖和2 分子3-磷酸
甘油醛 。2分子3-磷酸甘油醛可縮合成1分子6-磷酸果糖。綜上所述,1分子6-磷酸葡萄糖經磷酸戊糖途徑氧化,需5 分子6-磷酸葡萄糖伴行,最後又生成5分子6-磷酸葡萄糖,實際消耗1分子6-磷酸葡萄糖。
磷酸戊糖途徑中的限速酶是6-磷酸葡萄糖
脫氫酶 ,此酶活性受NADPH+H濃度影響,NADPH+H 濃度增高時抑制該酶活性,因此磷酸戊糖途徑的代謝速度主要受細胞內NADPH+H 需求量的調節。
2.磷酸戊糖途徑的生理意義
磷酸戊糖途徑的主要生理意義是產生5-磷酸
核糖 和NADPH+H。
(1)生成5-磷酸核糖(R-5-P):磷酸戊糖途徑是體內利用葡萄糖生成5-磷酸核糖的唯一途徑。5-磷酸核糖是合成核酸和
核苷酸 輔酶的重要原料。對於缺乏6-磷酸葡萄糖脫氫酶的組織如肌肉,也可利用
糖酵解 中間產物3-磷酸甘油醛和6-磷酸果糖經轉
酮基 酶和轉醛基
酶催化 的逆反應生成。故損傷後修復的再生組織、更新旺盛的組織,此途徑都比較活躍。
(2)生成NADPH+H :①NADPH+H是體內許多
合成代謝 中氫原子的
供體 ,如脂肪酸、膽固醇和類固醇激素等化合物的合成,都需要大量NADPH,因此在脂肪、固醇類化合物合成旺盛的組織,如肝臟、哺乳期乳腺、脂肪組織、腎上腺皮質及睪丸等組織中,磷酸戊糖途徑特別活躍。②NADPH+H是
谷胱甘肽 (GSH)
還原酶 的輔酶,對於維持細胞中谷胱甘肽於還原狀態起重要作用。GSH是細胞中重要的抗氧化物質,有清除H2O2和過氧化物,保護細胞中含巰基的酶和蛋白質免遭氧化破壞的作用,以維持
細胞結構 和功能的完整。紅細胞中如發生H2O2和過氧化物的積累,將使紅細胞的壽命縮短並增加血紅蛋白氧化為
高鐵血紅蛋白 的速率,後者沒有運氧功能。遺傳性6-磷酸葡萄糖
脫氫酶 缺陷的患者,磷酸戊糖途徑不能正常進行,NADPH+H缺乏,GSH含量減少,常在進食蠶豆或使用某些藥物後誘發急性溶血性黃疸。③NADPH+H是加單氧
酶系 的組成成分,參與激素、藥物、毒物的
生物轉化 過程。
(3)中間產物3-磷酸甘油醛:3-磷酸甘油醛是三種代謝途徑的樞紐。如果磷酸戊糖途徑受阻,3-磷酸甘油醛則可進入糖的無氧分解或糖的有氧分解途徑;反之,若用碘乙酸抑制3-磷酸甘油醛脫氫酶,使糖的無氧分解和有氧分解不能進行,則3-磷酸甘油醛可進入磷酸戊糖途徑。磷酸戊糖途徑在整個代謝過程中沒有氧的摻入,但可使葡萄糖降解,這在種子萌發的初期作用很大。植物染病或受傷時,磷酸戊糖途徑增強,所以它與植物的抗病能力有一定關係。
(4)與植物光合作用有關:磷酸戊糖途徑產生的三碳糖、五碳糖、七碳糖都是植物光合作用的中間產物,有的反應是光合作用與卡爾文循環中某些反應的相應逆反應,而且它與卡爾文循環還有一些相同的酶。
氧化分解 脂肪(三脂醯甘油或甘油三酯)在體內主要功能是氧化分解,為機體提供生命活動所需要的能量。儲存於脂肪組織中的三脂醯甘油 (triglyceride),被
脂肪酶 逐步水解為
游離脂肪酸 (free fatty acid,FFA)及甘油釋放入血,供給全身各組織氧化利用的過程,稱為三脂醯甘油動員。脂肪組織中含有的脂肪酶,一種是對激素敏感的三脂醯甘油脂肪酶,稱激素敏感脂肪酶(hormone-sensitive triglyceride lipase,HSL) ,也是三脂醯甘油動員的限速酶。另外還有二脂醯甘油脂肪酶和一脂醯甘油脂肪酶,這兩種酶活性較高,對激素不敏感。胰高血糖素、腎上腺素、
去甲腎上腺素 等能激活三脂醯甘油脂肪酶,促進脂肪分解,故稱為
脂解激素 ;胰島素的作用則與之相反,使三脂醯甘油脂肪酶活性降低,拮
抗脂解激素 的脂解作用,故稱抗脂解激素。一分子脂肪被脂肪酶水解為1分子甘油和3分子脂肪酸後,分別進入各自的
代謝途徑 。
甘油的氧化分解 甘油主要由心、肝、骨骼肌等組織攝取利用,在細胞內經甘油激酶(glycerokinase)的作用,生成α-磷酸甘油(3-磷酸甘油),後者在α-磷酸甘油脫氫酶的催化下生成
磷酸二羥丙酮 ,磷酸二羥丙酮可循
糖代謝 途徑氧化分解釋放能量,1分子甘油徹底氧化可淨生成17.5~19.5分子ATP。也可以在肝臟循
糖異生 途徑轉變為糖原和葡萄糖。
脂肪酸的氧化 在氧供給充足的條件下,脂肪酸可在體內分解成二氧化碳和水,釋出大量能量。除腦組織和成熟紅細胞外,大多數組織均能氧化脂肪酸,但以肝及肌肉組織最活躍。
1.脂肪酸的活化——脂醯CoA的生成
脂肪酸的活化反應在胞液中進行,脂肪酸在脂醯CoA
合成酶 (acyl-CoA synthetase)催化下,在ATP、
CoA-SH 、Mg存在的條件下,活化為脂醯CoA。脂醯CoA含有高能硫酯鍵,而且水溶性增大,使脂醯基的代謝活性明顯增加。分子中的CoA是脂醯基的載體。由於反應過程中生成的焦磷酸(PPi),迅速被細胞內的
焦磷酸酶 水解,阻止了逆向反應的發生,因此1分子脂肪酸活化成脂醯CoA,實際上消耗了2個
高能磷酸鍵 。
2.脂醯CoA進入線粒體
脂肪酸的活化在胞液中進行,而催化
脂肪酸氧化 分解的酶系存在於
線粒體基質 ,因此活化的脂醯CoA必須進入線粒體才能分解。脂醯CoA不能直接透過
線粒體內膜 ,其脂
醯基 需經肉毒鹼(carnitine即3-羥-4-三甲氨基丁酸)轉運才能進入基質。線粒體內膜的兩側存在著
肉毒鹼脂醯轉移酶 Ⅰ及Ⅱ,在位於線粒體內膜外側面的酶Ⅰ的催化下,脂醯CoA轉化為脂肪醯肉毒鹼,而移到膜內側,進入膜內側的脂肪醯肉毒鹼又經酶Ⅱ的催化而重新轉變成脂醯CoA,並釋放出肉毒鹼。肉毒鹼脂醯轉移酶Ⅰ是限速酶,脂醯CoA進入線粒體是脂肪酸氧化的限速步驟,當飢餓、高脂低糖膳食或糖尿病時,體內糖利用發生障礙,需要脂肪酸供能,這時肉毒鹼脂醯轉移酶Ⅰ活性增加,脂肪酸氧化增強。
脂醯基進入
線粒體基質 後,從脂醯基的
β-碳原子 開始,經過
脫氫 、加水、再脫氫及硫解四步連續的反應,脂醯基斷裂產生1分子乙醯CoA和1分子比原來少兩個碳原子的脂醯CoA(圖5-1-9)。催化這些反應的酶彼此結合形成
多酶複合體 ,稱脂肪酸氧化酶系。
(1)脫氫:脂醯CoA在脂醯CoA
脫氫酶 的催化下,α、β碳原子各脫去一個氫原子,生成α,β-烯脂醯CoA,脫下的2H由FAD接受生成FADH2。一分子FADH2進入
呼吸鏈 通過氧化磷酸化產生1.5分子ATP(過去的理論值為2分子ATP,詳見氧化磷酸化一節)。
(2)加水:在水化酶催化下,烯脂醯CoA加水生成β-羥脂醯CoA。
(3)再脫氫:在β-羥脂醯CoA脫氫酶催化下,β-羥脂醯CoA脫下2H,生成β-酮脂醯CoA,脫下的2H由NAD接受,生成NADH+H。一分子NADH+H進入呼吸鏈通過氧化磷酸化產生2.5分子ATP(過去的理論值為3分子ATP)。
(4)硫解(加CoASH分解):β-酮脂醯CoA在
硫解酶 的催化下,加入CoASH使α、β碳原子之間
化學鍵 斷裂,生成1分子乙醯CoA和1分子比原來少兩個碳原子的脂醯CoA。
以上生成的比原來少2個碳原子的脂醯CoA可再進行
脫氫 、加水、再脫氫及硫解反應,如此反覆進行,直至最後生成丁醯CoA,後者再進行一次
β-氧化 ,即完成
脂肪酸的β-氧化 。
4.乙醯CoA的去路:
脂肪酸β-氧化 的終產物是乙醯CoA,其進一步的代謝變化可進入三羧酸循環徹底氧化為二氧化碳和水,也可轉變為其它物質。
5.脂肪酸徹底氧化時能量的釋放和利用
脂肪酸氧化是體內能量的重要來源。以16個碳原子的
軟脂酸 為例:一分子軟脂醯CoA需經7次β-氧化,生成8分子乙醯CoA。因此1分子軟脂酸徹底氧化共生成(7×1.5)+(7×2.5)+(8×10)=108分子ATP。減去軟脂酸活化時消耗的兩個
高能磷酸鍵 ,淨生成106分子ATP。
生成利用 脂肪酸在肝外組織(如
心肌 、
骨骼肌 等)經β-氧化生成的乙醯CoA,能徹底氧化生成二氧化碳和水,而在肝細胞中因為具有活性較強的合成酮體的酶系,β-氧化反應生成的乙醯CoA,大多轉變為
乙醯乙酸 (acetoacetate),β-羥丁酸(β-hydroxybutyrate)和
丙酮 (acetone),這三種中間產物統稱酮體(ketone bodies)。由於肝內缺乏氧化利用酮體的酶系,所以酮體不能在肝內氧化,必須透過細胞膜進入血液循環運輸到肝外組織才能進一步
氧化分解 供能。
酮體的生成 酮體生成的部位是在肝細胞線粒體內。脂肪酸
β-氧化 生成的乙醯CoA是合成酮體的原料。其合成過程分三步進行(圖5-1-10)。
1.兩分子乙醯CoA在
硫解酶 (thiolase)催化下縮合成1分子乙醯乙醯CoA。
2.乙醯乙醯CoA再與1分子乙醯CoA縮合成β-羥-β-甲基
戊二酸 單醯CoA(HMG-CoA),催化這一反應的酶為HMG-CoA
合成酶 ,是酮體合成的限速酶。
3.HMG-CoA經裂解酶催化分解成
乙醯乙酸 和乙醯CoA。乙醯乙酸
加氫 還原成β-羥丁酸,少量乙醯乙酸自發脫羧生成
丙酮 。酮體總量中約70%為β-羥丁酸,30%為乙醯乙酸,丙酮只占少量,丙酮可通過腎和肺排出。
酮體的利用 肝外組織(心肌、骨骼肌、大腦)中有活性很強的利用酮體的酶。
乙醯乙酸 在乙醯乙酸
硫激酶 或琥珀醯CoA轉硫酶催化下,轉變為乙醯乙醯CoA,然後再被
硫解酶 分解為兩分子乙醯CoA,乙醯CoA進入三羧酸循環徹底氧化。可見肝內生酮肝外用是脂肪酸在肝中氧化的一個代謝特點。
生理意義 酮體是脂肪酸在肝臟氧化的正常中間產物,是肝臟為肝外組織提供能源物質的一種形式,酮體分子小、溶於水,便於通過血液運輸,也易於通過血腦屏障及肌肉等組織的毛細血管壁,是肌肉,尤其是腦組織的重要能源。腦組織不能氧化脂肪酸,卻能利用酮體。長期飢餓、糖供應不足時,酮體可以代替葡萄糖,成為腦組織的主要能源物質。
正常情況下血中僅含少量酮體。但在飢餓、妊娠嘔吐及糖尿病時,三脂醯甘油動員加強,肝中酮體生成過多,超出肝外組織利用的能力,可引起血中酮體升高,尿中出現酮體,即酮血症和酮尿症,可導致酮症酸中毒,嚴重者危及生命。
分解代謝 胺基酸的主要功用是作為蛋白質合成的原料;其次可合成其它含氮物質(如
嘌呤 、
嘧啶 等);過多的胺基酸在體內不能貯存,這部分胺基酸可通過各種代謝方式先轉變為三羧酸循環的中間產物,然後經三羧酸循環徹底氧化為CO2和H2O,也可通過糖異生作用轉變為葡萄糖,還可轉變為脂肪貯存。各種胺基酸具有共同的結構特點,故有共同的
代謝途徑 ,但不同的胺基酸由於結構的差異也有不同的代謝方式。
三羧酸循環 右圖顯示胺基酸進入三羧酸循環的方式。從圖中可以看出,10種胺基酸最後分解產生乙醯CoA ;5種胺基酸轉變成三羧酸循環的中間產物
α-酮戊二酸 ;4種胺基酸轉變成琥珀醯CoA;2種胺基酸轉變為延胡索酸;2種胺基酸轉變為草醯乙酸。然後可經三羧酸循環進一步徹底氧化為CO2和H2O。
胺基酸 也可異生為糖或生成酮體。凡是能轉變為丙酮酸、草醯乙酸、琥珀醯CoA、α-酮戊二酸和延胡索酸的胺基酸稱為
生糖胺基酸 ,這是因為三羧酸循環的中間產物和丙酮酸能轉變為磷酸烯醇式丙酮酸,然後很容易循
糖異生 途徑異生為糖。凡是能分解為乙醯CoA和乙醯乙醯CoA的胺基酸稱為
生酮胺基酸 ,因為乙醯CoA或乙醯乙醯CoA亦可用於合成脂肪。20種胺基酸中,只有亮氨酸和賴氨酸是唯一生酮的胺基酸;
異亮氨酸 、
苯丙氨酸 、
色氨酸 和酪氨酸是生酮兼生糖胺基酸;剩餘14種是生糖胺基酸。
脫氨基作用 胺基酸脫氨基作用是胺基酸
分解代謝 的最主要反應。體內大多數組織細胞均可進行。胺基酸可通過多種方式脫去氨基,如轉氨基、氧化脫氨基、
聯合脫氨基 等,其中以聯合脫氨基最為重要。
胺基酸脫氨基的產物為α-酮酸和氨.
大多數
胺基酸 在進行分解代謝之初,首先通過轉氨基作用將α-氨基轉移給α-酮戊二酸,使其形成
谷氨酸 和相應的α-酮酸(α-ketoacid)。
轉氨基作用是胺基酸在
氨基轉移酶 (aminotransferase)或稱
轉氨酶 (transaminase)催化下,可逆地把
α-胺基酸 的氨基轉移給α-酮戊二酸,使α-胺基酸轉變為相應的α-酮酸,而原來的α-酮戊二酸接受氨基轉變成相應的谷氨酸。可見,
轉氨基作用 既是胺基酸的
分解代謝 過程,又是某些非必需胺基酸合成的重要途徑。轉氨酶的輔酶是維生素B6的磷酸酯
磷酸吡哆醛 。體內大多數胺基酸均能進行轉氨基反應,轉氨酶的種類很多,專一性強,分布也最廣。以
丙氨酸氨基轉移酶 (alanine transaminase,ALT;又稱谷丙轉氨酶,GPT)以及
天冬氨酸氨基轉移酶 (aspartate transaminase,AST;又稱穀草轉氨酶,GOT)最重要,前者在肝細胞含量最高,後者在心肌細胞含量最高。正常情況下它們在血清中含量都很低,當肝細胞或心肌受損時血清中含量增高,故可用於臨床上肝臟或心肌疾病的輔助診斷。
通過以上
轉氨基作用 生成的谷氨酸由
谷氨酸脫氫酶 (glutamate dehydrogenase)催化,脫氫的同時又脫去氨基的反應,稱為氧化脫氨基作用。在體內
胺基酸氧化酶 種類很多,其中以谷氨酸脫氫酶的作用最重要。谷氨酸脫氫酶是以NAD或NADP為輔酶的
不需氧脫氫酶 ,催化谷氨酸脫氫生成亞谷氨酸,然後水解生成α-酮戊二酸和NH3(圖5-1-14)。谷氨酸脫氫酶廣泛存在於肝、腎及腦中,反應可逆,通過還原
氨基化 作用,α-酮戊二酸和氨可合成谷氨酸,因此,它不僅在胺基酸的分解中起作用,而且在非必需胺基酸合成中也起著重要作用。
聯合脫氨基作用是體內脫氨基的主要方式,生物體記憶體在二種聯合脫氨基方式。
(1)轉氨酶與谷氨酸脫氫酶的聯合脫氨基作用:①胺基酸首先與α-酮戊二酸進行轉氨基反應,生成相應的α酮酸和谷氨酸,②谷氨酸在谷氨酸脫氫酶作用下脫去氨基生成α-酮戊二酸。全過程可逆,通過其逆過程可以合成新的非必需胺基酸。此過程主要存在於肝、腎和腦組織中,心肌和骨骼肌中不能進行,因為心肌和骨骼肌中谷氨酸脫氫酶活性低。
肌肉組織中-谷氨酸脫氫酶活性不高,難以進行上述聯合脫氨基作用,在肌肉中胺基酸是通過嘌呤核苷酸循環脫去氨基的。過程為:①
α-胺基酸 首先與α-酮戊二酸
轉氨基作用 生成
谷氨酸 ,後者再與草醯乙酸轉氨基反應,生成天冬氨酸;②天冬氨酸與
次黃嘌呤核苷酸 (IMP)由
腺苷酸 代琥珀酸合成酶催化生成腺苷酸代琥珀酸;③腺苷酸代琥珀酸裂解生成腺苷酸(AMP)和延胡索酸;④AMP在
腺苷酸脫氨酶 (此酶在肌肉組織中活性較強)催化下脫去氨基生成IMP,完成胺基酸的
脫氨基作用 。IMP可以再參加循環,延胡索酸經三羧酸循環轉變為草醯乙酸後再次參加
轉氨 反應。
胺基酸脫氨基作用的終產物是α-酮酸和氨。它們將分別進入各自的代謝途徑。
α-酮酸代謝 胺基酸脫氨後生成的 α-酮酸可進一步代謝。主要有以下三方面:
1.經氨基化生成非必需胺基酸
實驗證明人體不能合成賴、異亮、苯丙、亮、色、纈、蘇、蛋等8種胺基酸相對應的α-酮酸,因而這些胺基酸不能在體內合成,必須從食物攝取,稱為營養必需胺基酸。其它十二種胺基酸則稱為營養非必需胺基酸,所謂
非必需胺基酸 並不是它們在代謝中的作用不重要,而是可以在人體合成,主要通過聯合脫氨基作用的逆反應生成,故食物不給與一般不會引起缺乏。
2.轉變成糖或脂肪
如前述,在體內可以轉變成糖的
胺基酸 稱為生糖胺基酸(glucogenic amino acid),能轉變為酮體者稱為生酮胺基酸(ketogenic amino acid),二者兼有的則稱為
生糖兼生酮胺基酸 (glucogenic and ketogenic amino acid)。
3.氧化供能 不同的α-酮酸在體內可以通過三羧酸循環與氧化磷酸化徹底氧化,產生CO2和水,並釋放出能量供生命活動的需要。
氨的代謝 氨是一種劇毒物質,腦組織對氨的作用尤為敏感,需要及時處理以免在組織中堆積。正常人除門靜脈血液外,血液中氨的濃度極低,一般不超過60μmol/L(0.1mg/dl)。
1.體內氨的來源
(2)腸道吸收:腸道氨主要來自①腸道細菌對未被消化的蛋白質和未被吸收的胺基酸作用(稱腐敗作用)產生的氨;②血中尿素擴散入腸管後在腸道細菌
尿素酶 作用下水解產生的氨。NH3比NH4容易穿過細胞膜而被吸收,在鹼性環境中,NH4轉變為NH3,所以腸管pH偏鹼時,氨的吸收增加。臨床上對高血氨病人採用酸性透析液做結腸透析而不用鹼性肥皂水灌腸就是這個道理。腸道每日產氨約有4g,腐敗作用增強時,氨的產生更多。
(3)腎臟產生:谷氨醯胺在腎遠曲小管上皮細胞
谷氨醯胺酶 的催化下,水解生成谷氨酸和NH3,NH3分泌到腎小管腔與尿中H結合生成NH4由尿排出。鹼性尿液不利NH3的分泌,NH3被吸收入血,成為血氨的另一個來源。故肝硬化腹水者不宜使用鹼性利尿藥以防血氨升高。
2.氨的轉運
氨是有毒物質,各組織中產生的氨必須以無毒形式經血液運輸至肝合成尿素或以銨鹽形式隨尿排出。氨在血液中有兩種運輸形式:
(1)
丙氨酸 運氨作用:主要將肌肉胺基酸脫下的氨經血液運輸到肝。過程為:①肌肉中的胺基酸經
轉氨基作用 將氨基轉移給丙酮酸生成丙氨酸,經血液運輸至肝;②在肝中,丙氨酸經聯合脫氨基作用釋放出氨,氨用於合成尿素,生成的丙酮酸則異生為葡萄糖;③葡萄糖經血液運送到肌肉,在肌肉活動供能的過程中又可分解為丙酮酸,再次接受氨基生成丙氨酸輸送到肝臟。如此通過丙氨酸和葡萄糖的互變把氨從肌肉運輸到肝臟的循環稱
丙氨酸-葡萄糖循環 (alanine glucose cycle)。
(2)
谷氨醯胺 的運氨作用:氨與
谷氨酸 在ATP供能和谷氨醯胺合成酶催化下合成谷氨醯胺,經血液輸送到肝或腎,經
谷氨醯胺酶 水解為谷氨酸及氨,在肝可合成尿素,在腎則以銨鹽形式由尿排出。谷氨醯胺生成的意義:①肝外組織解除
氨毒 ;②是從腦、肌肉等組織向肝或腎運輸氨的主要形式;③氨的儲存形式,為某些含氮化合物的合成提供原料,如嘌呤及嘧啶的合成。臨床上對肝性腦病患者可服用或輸入谷氨酸鹽以降低血氨濃度。
3.氨的主要去路
氨在體內的主要去路是在肝內通過
鳥氨酸循環 (
尿素循環 )生成無毒的尿素,然後由腎排出體外)。鳥氨酸循環的過程可分為以下四步:
1)
氨基甲醯磷酸 的合成:氨由
丙氨酸 與
谷氨醯胺 轉運入肝細胞線粒體在氨基甲醯磷酸
合成酶 Ⅰ(carbamoyl phosphate synthetaseⅠ,CPS-Ⅰ)催化下,與CO2和H2O分子結合,消耗2分子ATP,合成氨基甲醯磷酸。反應不可逆。
(2)
瓜氨酸 的合成:在
鳥氨酸 氨甲醯
轉移酶 (ornithine carbamoyl transferase,OCT)催化下,將氨基甲醯磷酸的氨甲醯基轉移至鳥氨酸的δ-NH2上生成瓜氨酸。反應不可逆。所需的鳥氨酸是由胞液經
線粒體內膜 上的
載體轉運 進入線粒體的。合成的瓜氨酸又由線粒體內膜上的載體轉運進入胞液。
(3)
精氨酸 的合成:在胞液內,瓜氨酸與天冬氨酸在精氨酸代琥珀酸
合成酶 (argninosuccinate synthetase)的催化下,由ATP供能合成精氨酸代琥珀酸並生成AMP+PPi,精氨酸代琥珀酸在精氨酸代琥珀酸
裂解酶 (argninosuccinate lyase)催化下,分解成為精氨酸和延胡索酸。在此過程中,天冬氨酸起著供給氨基的作用;生成的延胡索酸經三羧酸循環轉變為草醯乙酸後可與
α-胺基酸 經
轉氨 作用轉變為天冬氨酸。由此可見,鳥氨酸循環與三羧酸循環可聯繫在一起。
(4)精氨酸水解生成尿素:精氨酸在胞液中
精氨酸酶 (arginase)的作用下,水解生成尿素和
鳥氨酸 。鳥氨酸再進入線粒體參與瓜氨酸的合成,反覆循環,不斷合成尿素。
尿素分子中的兩個-NH2,一個由
丙氨酸 或谷氨醯胺轉運入肝細胞線粒體的NH3,另一個由天冬氨酸提供,碳原子來自CO2,天冬氨酸和
谷氨酸 均是氨的載體。另外,尿素合成是耗能過程,每合成1分子尿素需消耗3分子ATP(消耗4個高能磷酸鍵)。
尿素主要通過腎臟排泄。如腎排泄功能障礙,必然導致血尿素增高。故臨床常測定血尿素氮(blood urea nitrogen,BUN)來反映腎功能。
正常情況下血氨濃度維持在較低水平。肝臟幾乎是體內唯一能合成尿素的器官,當肝功能嚴重損傷時,尿素合成障礙,血氨濃度升高,稱為
高氨血症 。一般認為,氨進入腦組織可與α-酮戊二酸結合生成谷氨酸,氨與谷氨酸再進一步結合生成
谷氨醯胺 。因此,腦中氨的增加,可消耗腦組織中α-酮戊二酸,導致三羧酸循環速度減弱, ATP生成減少,引起大腦功能障礙,嚴重時可產生昏迷,即氨中毒(肝性腦病)。
徹底氧化 乙醯CoA是生化代謝中的一個樞紐性物質,如前所述,糖、脂肪、胺基酸分解代謝都能產生乙醯輔酶A;乙醯輔酶A有多種代謝去路,可以合成脂肪酸、膽固醇、酮體等,乙醯輔酶A徹底氧化釋放能量的途徑是三羧酸循環。通過三羧酸循環和氧化磷酸化,乙醯CoA氧化產生CO2、H2O,釋放能量推動ATP合成。在
營養物質 產能代謝中,三羧酸循環和氧化磷酸化是釋放能量最多的環節,是營養物質產能代謝和相互轉化的樞紐。
三羧酸循環 三羧酸循環(tricarboxylic acid cycle)是由Hans Adolf Krebs於1937年首先提出,故又稱為
Krebs循環 (尿素循環也是Krebs提出的)。此循環是從活性二碳化合物—乙醯輔酶A和四碳草醯乙酸線上粒體內縮合成含三個
羧基 的檸檬酸開始,經過一系列
脫氫 脫羧反應 ,最後重新生成草醯乙酸而成為循環(圖5-2-1)。此反應過程是由含有三個羧基的檸檬酸作為第一個中間產物的循環反應,故稱為三羧酸循環,也稱檸檬酸循環。三羧酸循環線上粒體內進行。
(一)三羧酸循環的反應過程
1.乙醯輔酶A與草醯乙酸縮合為檸檬酸
此反應為三羧酸循環的關鍵反應之一,是由
檸檬酸合成酶 催化的不可逆反應,所需能量來自乙醯CoA的高能硫酯鍵水解供應。
檸檬酸本身不易氧化,在
順烏頭酸酶 作用下,通過脫水與加水反應,使羥基由β碳原子轉移到
α碳原子 上,生成易於脫氫氧化的異檸檬酸,為進一步的氧化脫羧反應作準備。
異檸檬酸在
異檸檬酸脫氫酶 的催化下,氧化脫羧生成α-酮戊二酸,反應脫下的氫由NAD接受生成NADH+H,脫羧使6碳化合物變為5碳化合物。這是三羧酸循環中第一次氧化脫羧生成CO2的反應。此反應不可逆,是三羧酸循環中的限速步驟。
這是三羧酸循環的第二次氧化脫羧反應,此反應類似於丙酮酸的氧化脫羧,也是不可逆反應,生成的琥珀醯CoA含有高能硫酯鍵。催化此反應的α-
酮戊二酸脫氫酶複合體 是三羧酸循環的限速酶,它由三個酶(α-酮戊二酸脫氫酶、琥珀
醯基轉移酶 、
二氫硫辛酸脫氫酶 )和五個輔助因子(TPP、硫辛酸、
HSCoA 、NAD、FAD)組成(原理見圖4-1-14)。
5.琥珀醯輔酶A生成琥珀酸
琥珀醯CoA在
琥珀酸硫激酶 的作用下,高能
硫酯 鍵水解,能量轉移給GDP生成GTP和琥珀酸。生成的GTP可直接利用,也可將其高能磷酸基團轉移給ADP生成ATP。這是三羧酸循環中唯一的一次
底物磷酸化 反應。
6.琥珀酸脫氫
琥珀酸在
琥珀酸脫氫酶 的催化下脫氫生成延胡索酸,脫下的氫由FAD接受生成FADH2。
7.蘋果酸生成
8.草醯乙酸再生
蘋果酸在
蘋果酸脫氫酶 催化下脫氫生成草醯乙酸,脫下的氫由NAD接受生成NADH+H。再生的草醯乙酸可再次進入三羧酸循環用於檸檬酸的合成。
(二)三羧酸循環的深入討論
1.三羧酸循環是在有氧的條件下,線上粒體內進行的循環反應過程。
三羧酸循環的產物有NADH+H、FADH2、ATP、CO2,這些產物對三羧酸循環的抑制效果不同。CO2經血循環至肺排出濃度降低,ATP快速消耗再生出ADP,因此在正常情況下這兩種產物對三羧酸循環的抑制可以忽略不計。NADH、FADH2的受氫體主要是氧,因此在缺氧情況下NADH和FADH2無法將氫傳遞出去,致使NAD和FAD無法再生,三羧酸循環因此被抑制。這就是為什麼三羧酸循環不消耗氧氣但卻只能在有氧條件下進行的原因。
2.三羧酸循環是機體主要的產能途徑。
每循環一周,1分子的乙醯輔酶A被氧化,三羧酸循環直接消耗的底物是乙醯基。循環中有兩次脫羧和四次
脫氫 反應,兩次
脫羧反應 生成兩分子CO2;四次脫氫反應,有三次由NAD接受共生成3分子NADH+H,有一次由FAD接受生成1分子FADH2(圖5-2-2)。每個NADH+H經氧化磷酸化產生2.5個ATP共7.5個ATP,每個FADH2經氧化磷酸化產生1.5ATP共1.5個ATP,循環一周以此種方式可生成9分子ATP;加上一次
底物磷酸化 生成的GTP,三羧酸循環一周共可生成10分子ATP。
3.三羧酸循環是單向反應體系。
4.三羧酸循環必須不斷補充中間產物。
三羧酸循環的中間產物,從理論上講,可以循環不消耗,但是由於體內各代謝途徑的相互交匯和轉化,三羧酸循環的中間產物常移出循環而參與其它代謝途徑,如草醯乙酸可轉變為天冬氨酸而參與蛋白質合成,琥珀醯輔酶A可用於血紅素的合成,α-酮戊二酸可轉變為谷氨酸等。
所以為了維持三羧酸循環中間產物的一定濃度,保證三羧酸循環的正常運轉,就必須補充消耗的中間產物,稱為
回補反應 。草醯乙酸的濃度,直接與乙醯輔酶A進入三羧酸循環的速度有關,因此不斷補充草醯乙酸是使三羧酸循環得以順利進行的關鍵,因而由丙酮酸形成草醯乙酸是最重要的回補反應。
草醯乙酸可以脫羧生成磷酸烯醇式丙酮酸,後者可以在肝臟和腎臟中逆
糖酵解 而生成葡萄糖或糖原,這就是非糖物質轉化為糖的途徑,稱為【
糖異生 】,因此,三羧酸循環中所有的中間產物都能異生成糖。注意,乙醯CoA是無法異生成糖的,為什麼?
5.三羧酸循環是三大營養物質徹底氧化的共同通路,是氧化釋放能量產生ATP最多的階段。糖、脂肪、蛋白質在體內
氧化分解 都將產生乙醯輔酶A,然後進入三羧酸循環進行降解,因此三羧酸循環是三大營養素在體內氧化的最終代謝通路(圖5-1-1)。循環中脫下的四對氫,可進入呼吸鏈氧化磷酸化生成ATP,是體內ATP生成最多的反應階段。
6.三羧酸循環是體內三大物質互變的樞紐
三羧酸循環是糖、脂肪、
胺基酸代謝 聯繫的樞紐。如葡萄糖氧化分解可生成乙醯CoA和NADPH+H,而乙醯CoA和NADPH+H可合成脂肪酸,進而合成脂肪;糖和甘油在體內代謝可生成α-酮戊二酸及草醯乙酸等三羧酸循環的中間產物,這些中間產物可以轉變成為某些胺基酸;而有些胺基酸又可通過
脫氨基作用 生成α-酮酸,再經
糖異生 的途徑生成糖或轉變成甘油,因此三羧酸循環不僅是三大營養物質
分解代謝 的最終共同途徑,而且也是它們互變的樞紐。
氫的燃燒 三大營養物質在體內的氧化可以分為三個階段,首先是糖、脂肪、蛋白質經過分解代謝生成乙醯輔酶A;接著乙醯輔酶A進入三羧酸循環脫羧脫氫,生成CO2並使NAD和FAD還原成NADH+H和FADH2;第三階段是NADH+H和FADH2中的氫經呼吸鏈傳給氧生成水,氧化過程中釋放出來的能量合成ATP。前兩個階段已在前講述,本節主要討論第三階段,即
代謝物 脫下的氫是如何通過呼吸鏈傳遞給氧生成水,細胞通過什麼方式將氧化過程中釋放的能量轉變成ATP分子中的
高能鍵 。
代謝物脫下的氫通過多種酶和輔酶所催化的連鎖反應逐步傳遞,最終與氧結合生成水,由於此過程與細胞利用O2生成CO2的呼吸有關,所以將此傳遞鏈稱為呼吸鏈(respiratory chain)。在呼吸鏈中,酶和輔酶按一定的順序排列在
線粒體內膜 上,其中傳遞氫的稱為
遞氫體 ,傳遞電子的稱為
遞電子體 。
呼吸鏈由線粒體內膜上的5種複合體(複合蛋白)組成,它們是複合體I(
NADH-Q還原酶 ,又稱NADH氧化酶,
輔基 為FMN和Fe-S)、複合體II(
琥珀酸-Q還原酶 ,輔基為FAD和Fe-S)、複合體III(
細胞色素還原酶 ,輔基為
血紅素 b、血紅素c1和Fe-S)、複合體IV(細胞色素氧化酶,輔基血紅素a、血紅素a3和Cu)、複合體V(ATP合酶)。輔基傳遞氫和電子的有NAD、FMN、FAD、CoQ(圖5-2-6),傳遞電子的有Fe-S(圖5-2-7)和血紅素Fe、Cu(圖5-2-8),Fe、Cu通過得失電子來傳遞電子。
複合體I(NADH-Q還原酶)、CoQ、複合體III(細胞色素還原酶)和複合體IV(細胞色素氧化酶)組成NADH氧化呼吸鏈,複合體II(琥珀酸-Q還原酶)、複合體III(細胞色素還原酶)和複合體IV(細胞色素氧化酶)組成琥珀酸氧化呼吸鏈。
【NADH氧化呼吸鏈的電子(氫)傳遞】線粒體內大多數
脫氫酶 都以NAD作為輔酶,在脫氫酶催化下底物SH2脫下的氫交給NAD生成NADH+H。NADH在NADH-Q還原酶(複合體I)作用下,NADH+H將
氫原子 傳遞給FMN生成FMNH2,後者再將氫傳遞給Q生成QH2,此時兩個氫原子解離成2個質子和2個電子,2個質子游離於介質中,2個電子經由細胞色素還原酶(複合體III)傳遞至
細胞色素C ,然後細胞色素氧化酶(複合體IV)將細胞色素C上的2個
電子傳遞 給氧生成O,O與2H結合生成水。
【琥珀酸氧化呼吸鏈的電子(氫)傳遞】琥珀酸-Q還原酶使琥珀酸脫氫生成FADH2,然後將FADH2上的氫傳遞給Q生成QH2,其後的傳遞過程如NADH呼吸鏈。
電子傳遞的氧化勢能使
線粒體基質 的氫離子H泵出到
膜間腔 (
內膜 外側),從而形成內膜兩側的
質子 梯度差(內正外負),這個梯度差是合成ATP的勢能所在。
複合體I(NADH-Q還原酶)、複合體III(細胞色素還原酶)、複合體IV(細胞色素氧化酶)具有質子泵作用,複合體II(琥珀酸-Q還原酶)傳遞電子的氧化勢能太小,不能將質子泵出。
(三)ATP的合成
ATP合酶(複合體V)由FO和F1等蛋白複合而成,有質子通道,當質子由膜間腔經質子通道回流時,ATP合酶被活化而驅動ATP的合成(圖5-2-11)。這種合成ATP的方式稱做【氧化磷酸化】,即在呼吸鏈中伴隨電子(質子)傳遞的
氧化還原反應 產生的
電化學 勢能,推動ADP磷酸化為ATP的過程。氧化磷酸化是細胞合成ATP的主要方式,合成ATP的另一種方式是【
底物磷酸化 】(見本章糖酵解一節)。注意:ATP合酶的FO中的O是字母O,不是零。
新近的研究表明,NADH經呼吸鏈氧化可合成2.5個ATP分子,FADH2經呼吸鏈氧化可生成1.5個ATP分子。注意,這與傳統的數字是不同的!
ATP是人體各種生命活動能量的直接供給者,它是食物中蘊藏的能量和機體利用的能量之間的紐帶。糖、脂類及蛋白質等能源物質
氧化分解 釋放的能量約有40%以
化學能 貯存在
高能化合物 中,ATP是體內最重要的高能化合物。但是ATP在細胞中的含量很低,在哺乳動物的腦和肌肉中約為3~8mmol/kg,這么微的含量只能供給肌肉劇烈活動1s左右的消耗,因此肌肉和腦中存在著一類貯存能量的高能化合物,這個化合物就是
磷酸肌酸 。
ATP將~P轉移給肌酸(CP)生成磷酸肌酸(CP~P),作為肌肉和腦組織中能量的一種貯存形式。磷酸肌酸在腦中的含量是ATP的1.5倍,肌肉中相當於ATP的5倍。受過良好訓練的運動員肌肉中的磷酸肌酸含量可高達30mmol/kg。當機體消耗ATP過多時,磷酸肌酸將~P轉移給ADP,生成ATP,供生理活動之用。磷酸肌酸是細胞內首先供應ADP使之再合成ATP的能源物質。ATP是體內的能量使者,是生物體內能量的儲存和利用的中心分子。
(四)氧化磷酸化的影響因素?
1.ADP/ATP比值的影響
氧化磷酸化主要受細胞對能量需求的影響。細胞能量供應缺乏時,即ATP減少,ADP增加,ADP/ATP比值增大,氧化磷酸化速率加快,NADH迅速減少而NAD增多,促進三羧酸循環;反之,細胞內能量供應充足時,即ATP增加,ADP減少,ADP/ATP比值減少,氧化磷酸化速率減慢,NADH消耗減少,三羧酸循環減緩。ADP/ATP比值是調節氧化磷酸化的基本因素,這種反饋調節可使機體適應生理需要,合理利用能源。
甲狀腺素能誘導細胞膜上Na-K-ATP酶的生成,使ATP分解為ADP的速度加快,線粒體中ADP/ATP比值增大,導致氧化磷酸化加強。由於ATP的合成和分解都增加,使機體耗氧量和產熱量都增加。所以
甲狀腺功能亢進 患者常出現
基礎代謝率 增高。
3.抑制劑的作用
一些化合物對氧化磷酸化有抑制作用,根據其作用部位不同分為兩類:
⑴呼吸鏈抑制劑:
這類抑制劑不影響呼吸鏈的電子傳遞,而是解除氧化與磷酸化的
偶聯 作用,使氧化過程產生的能量不能生成ATP,而是以熱能的形式散發。如2,4-二硝基酚、
雙香豆素 等屬於解偶聯劑,感冒或患某些傳染病時體溫升高,是由於細菌或病毒產生的解偶聯劑所致。
NADH的氧化 體內很多物質氧化分解產生NADH,線粒體內生成的NADH可直接通過呼吸鏈進行氧化磷酸化,而胞液中生成的NADH由於不能自由透過線粒體內膜,故需通過某種轉運機制,將氫轉移到線粒體內,重新生成NADH或FADH2後再參加氧化磷酸化。這種轉運機制主要有
α-磷酸甘油穿梭 和蘋果酸穿梭。
該穿梭系統主要存在於肌肉和神經組織,它是通過α-磷酸甘油將胞液中NADH的氫帶入線粒體內,具體過程如下:
當胞液中NADH濃度升高時,磷酸二羥丙酮在胞液α-磷酸甘油脫氫酶(輔酶為NAD)催化下由NADH+H供氫生成α-磷酸甘油,後者進入線粒體後線上粒體內α-磷酸甘油脫氫酶(輔酶為FAD)的催化下重新生成磷酸二羥丙酮和FADH2。磷酸二羥丙酮穿出線粒體外可繼續利用。生成的FADH2經呼吸鏈氧化磷酸化,這種穿梭作用可生成1.5分子ATP。
又稱
蘋果酸-天冬氨酸穿梭 系統,主要存在於肝、腎、心。是指通過蘋果酸將胞液中NADH的氫帶進線粒體內,具體過程如下:
當胞液中NADH濃度升高時,首先由蘋果酸脫氫酶(輔酶NAD)催化,使草醯乙酸還原成蘋果酸。蘋果酸在
線粒體內膜 轉位酶的催化下穿過線粒體內膜,進入線粒體的蘋果酸,在蘋果酸脫氫酶作用下脫氫生成草醯乙酸,並生成NADH+H。生成的NADH+H通過呼吸鏈傳遞進行氧化磷酸化,生成2.5分子ATP。
草醯乙酸不能直接透過線粒體內膜返回胞液,但它可在天冬氨酸轉氨酶作用下從
谷氨酸 接受氨基生成天冬氨酸,谷氨酸轉出氨基後生成
α酮戊二酸 ,α酮戊二酸、天冬氨酸都能在膜上轉位酶的作用下穿過線粒體內膜而進入胞液,在胞液中天冬氨酸和α酮戊二酸在天冬氨酸轉氨酶的作用下又重新生成草醯乙酸和谷氨酸,草醯乙酸又可重新參與蘋果酸穿梭作用。
ATP的總結算 (一)葡萄糖徹底氧化產生ATP結算
關於葡萄糖徹底氧化為水和二氧化碳究竟產生多少ATP分子的問題一直受到人們的關注。葡萄糖分解通過
糖酵解 和檸檬酸循環的
底物磷酸化 作用產生ATP的分子數,根據
化學計算 可以得到明確的答覆。但是氧化磷酸化產生的ATP分子數並不十分準確。因為
質子泵 、ATP合成以及
代謝物 的轉運過程並不需要是完整的數值甚至不需要固定值。根據最新測定計算,一對NADH傳至O2,所產生的ATP分子數是2.5個,
琥珀酸 及脂肪酸氧化產生的
FADH2 傳遞至O2,產生的ATP是1.5個。這樣,當一分子葡萄糖徹底氧化徹底氧化為CO2和H2O所得到的ATP分子數和過去傳統的
統計數 (36或38個ATP)少了6個ATP分子,成為30個或32個。全部的統計列於表5-2-1。在30或32個ATP分子中,氧化磷酸化產生26或28個,底物磷酸化產生6個,葡萄糖活化共消耗2個。
(二)軟脂酸徹底氧化產生ATP結算
軟脂酸 (16碳飽和脂肪酸)徹底氧化產生ATP數目為106個,其中氧化磷酸化為100個,底物磷酸化為8個,脂肪酸活化消耗2個(消耗1個ATP生成1個AMP,即消耗2個
高能鍵 )。