研究簡史,物質結構,價鍵觀點,分子軌道模型,物理性質,化學性質,取代反應,氧化反應,臭氧化反應,其他,光照異構化,相關物質,異構體,衍生物,工業製備,從煤焦油中提取,從石油中提取,烷烴芳構化,蒸汽裂解,芳烴分離,甲苯脫烷基化,工業用途,安全風險,基本標識,健康危害,安全措施,滅火方法,相關法規,毒理資料,接觸限值,中毒症狀,急救處理,檢測方法,儲存運輸,操作注意,儲存注意,
研究簡史 凱庫勒雙鍵擺動模型 苯是在1825年由英國科學家法拉第(即
麥可·法拉第 ,Michael Faraday,1791年- 1867年)首先發現的。19世紀初,英國和其他歐洲國家一樣,城市的照明已普遍使用煤氣。從生產煤氣的原料中製備出煤氣之後,剩下一種油狀的液體卻長期無人問津。法拉第是第一位對這種油狀液體感興趣的科學家。他用蒸餾的方法將這種油狀液體進行分離,得到另一種液體,實際上就是苯。當時法拉第將這種液體稱為“氫的重碳化合物”。
1834年,德國科學家米希爾里希(即恩斯特·埃爾哈德·米希爾里希,ErnstEilhard Mitscherlich,1794年-1863年)通過蒸餾苯甲酸和石灰的混合物,得到了與法拉第所制液體相同的一種液體,並命名為苯。待有機化學中的正確的分子概念和原子價概念建立之後,法國化學家日拉爾(即查理·弗雷德里克·日拉爾,Charles Frederic Gerhardt,1816年-1856年)等人又確定了苯的相對分子質量為78,分子式為C6 H6 。苯分子中碳的相對含量如此之高,使化學家們感到驚訝。對於如何確定苯的結構式,化學家們遇到了難題:苯的碳、氫比值如此之大,表明苯是高度不飽和的化合物,但它又不具有典型的不飽和化合物應具有的易發生加成反應的性質。
奧地利化學家洛希米特(即
約翰·約瑟夫·洛希米特 ,Johann Jasef Loschmidt)在他的《化學研究》(1861年出版)一書中畫出了121個苯及其他芳香化合物的環狀化學結構。德國化學家凱庫勒(即
弗里德里希·奧古斯特·凱庫勒·馮·斯特拉多尼茨 ,Friedrich August Kekulé von Stradonitz,1829年-1896年)也看過這本書,在1862年1月4日給其學生的信中提到洛希米特關於分子結構的描述令人困惑。不過,洛希米特把苯環畫成了圓形。
凱庫勒是一位極富想像力的學者,他曾提出了碳四價和碳原子之間可以連線成鏈這一重要學說。對苯的結構,他在分析了大量的實驗事實之後認為:這是一個很穩定的“核”,6個碳原子之間的結合非常牢固,而且排列十分緊湊,它可以與其他碳原子相連形成芳香族化合物。於是,凱庫勒集中精力研究這6個碳原子的“核”。在提出了多種開鏈式結構但又因其與實驗結果不符而一一否定之後,1865年他終於悟出閉合鏈的形式是解決苯分子結構的關鍵。
關於凱庫勒悟出苯分子的環狀結構的經過,一直是化學史上的一個趣聞。1890年,在柏林市政大廳舉行的慶祝凱庫勒發現苯環結構25周年的大會上,據他自己說這來自於一個夢。那是他在比利時的根特大學任教時,一天夜晚,他在書房中打起了瞌睡,眼前又出現了旋轉的碳原子。碳原子的長鏈像蛇一樣盤繞捲曲,忽見一蛇抓住了自己的尾巴,並旋轉不停。他像觸電般地猛醒過來,整理苯環結構的假說,又忙了一夜。對此,凱庫勒說:“我們應該會做夢!……那么我們就可以發現真理,……但不要在清醒的理智檢驗之前,就宣布我們的夢。”應該指出的是,凱庫勒能夠從夢中得到啟發,成功地提出重要的結構學說,並不是偶然的。
但是,1992年,美國南伊利諾大學化學教授約翰·沃提茲(John H. Wotiz,1919年-2001年)在《凱庫勒之謎,對化學家和心理學家的挑戰》(The Kekulériddle, a Challenge to Chemists and Psychologists )一書中對凱庫勒在苯環結構建立過程中所扮演的角色提出了質疑。早在1854年,法國化學家勞倫(即奧古斯特·勞倫,Auguste Laurent,1807年-1853年)在《化學方法》一書中已把苯的分子結構畫成六角形環狀結構。沃提茲還在凱庫勒的檔案中找到了他在1854年7月4日寫給德國出版商的一封信,在信中他提出由他把勞倫的這本書從法文翻譯成德文。這就表明凱庫勒讀過而且熟悉勞倫的這本書。但是凱庫勒在論文沒有提及勞倫對苯環結構的研究,只提到勞倫的其他工作。
物質結構 苯分子中的離域大Π鍵 苯環是最簡單的芳環,由六個
碳原子 構成一個六元環,每個碳原子接一個基團,苯的6個基團都是
氫原子 。
但實驗表明,苯不能使
溴水 或酸性KMnO
4 褪色,這說明苯中沒有
碳碳雙鍵 。研究證明,苯環主鏈上的碳原子之間並不是由以往所認識的
單鍵 和雙鍵排列(
凱庫勒 提出),每兩個碳原子之間的鍵均相同,是由一個既非雙鍵也非
單鍵 的鍵(大π鍵)連線。
價鍵觀點 碳數為4n+2(n是正整數,苯即n=1),且具有單、雙鍵交替排列結構的
環烯烴 稱為
輪烯 (
annulene ),苯是一種輪烯。苯分子是平面分子,12個原子處於同一平面上,6個碳和6個氫是均等的,C-H
鍵長 為1.08Α,C-C鍵長為1.40Α,此數值介於單雙鍵長之間。分子中所有鍵角均為120°,
碳原子 都採取sp
2 雜化。每個
碳原子 還剩餘一個p軌道垂直於分子平面,每個軌道上有一個
電子 。6個軌道重疊形成
離域 大π鍵 ,萊納斯·鮑林提出的共振雜化理論認為,苯擁有共振雜化體是苯環非常穩定的原因,也直接導致了苯環的芳香性。
分子軌道模型 苯的π分子軌道和能級 從分子軌道理論來看,可以認為苯的6個p軌道相互作用形成6個π分子軌道,可分別用ψ
1 、ψ
2 、ψ
3 、ψ
4 、ψ
5 、ψ
6 表示(如圖)。其中ψ
1 、ψ
2 、ψ
3 是能量較低的
成鍵軌道 ,ψ
4 、ψ
5 、ψ
6 是能量較高的
反鍵軌道 。ψ
2 和ψ
3 、ψ
4 和ψ
5 是兩對
簡併軌道 。
基態 時苯的
電子云 分布是三個成鍵軌道疊加的結果,故電子云均勻分布於苯環上下及環原子上,形成閉合的電子云。它是苯分子在磁場中產生環電流的根源。
物理性質 苯在常溫下為一種無色、有甜味的透明液體,其密度小於水,具有強烈的芳香氣味。苯的沸點為80.1℃,熔點為5.5℃。苯比水密度低,密度為0.88g/cm
3 ,但其
分子質量 比水重。苯難溶於水,1升水中最多溶解1.7g苯;但苯是一種良好的有機溶劑,溶解
有機分子 和一些非
極性 的無機分子的能力很強,除甘油,乙二醇等多元醇外能與大多數有機溶劑混溶.除碘和硫稍溶解外,無機物在苯中不溶解。
苯能與水生成
恆沸物 ,沸點為69.25℃,含苯91.2%。因此,在有水生成的反應中常加苯
蒸餾 ,以將水帶出。
燃燒熱 :3303.08kJ/mol(25℃,氣體))。
化學性質 苯參加的
化學反應 大致有3種:一種是其他基團和苯環上的氫原子之間發生的取代反應;一種是發生在苯環上的加成反應(註:苯環無碳碳雙鍵,而是一種介於單鍵與雙鍵的獨特的鍵);一種是普遍的燃燒(氧化反應)(不能使酸性
高錳酸鉀 褪色)。
取代反應 苯環的
電子云 密度較大,所以發生在苯環上的取代反應大都是
親電取代 反應。
親電取代反應 是芳環有代表性的反應。苯的取代物在進行親電取代時,第二個取代基的位置與原先取代基的種類有關。
鹵代反應
苯的鹵代反應的通式可以寫成:
PhH+X
2 —
催化劑 (FeBr
3 /Fe)→PhX+HX
反應過程中,鹵素分子在苯和
催化劑 的共同作用下
異裂 ,X
+ 進攻苯環,X
- 與催化劑結合。
以溴為例,將
液溴 與苯混合,溴溶於苯中,形成紅褐色液體,不發生反應,當加入鐵屑後,在生成的三
溴化鐵 的
催化作用 下,溴與苯發生反應,
混合物 呈微沸狀,反應放熱有紅棕色的溴
蒸汽 產生,冷凝後的氣體遇空氣出現白霧(HBr)。催化歷程:
FeBr3 +Br-——→FeBr4
PhH+Br+FeBr4 -——→PhBr+FeBr3 +HBr
反應後的混合物倒入冷水中,有紅褐色油狀液團(溶有溴)沉於水底,用稀鹼液洗滌後得無色液體
溴苯 。
在工業上,鹵代苯中以氯和溴的取代物最為重要。
硝化反應
PhH+HO-NO2 -----H2 SO4 (濃)△---→PhNO2 +H2 O
硝化反應 是一個強烈的
放熱反應 ,很容易生成一取代物,但是進一步反應速度較慢。其中,濃
硫酸 做催化劑,加熱至50~60攝氏度時反應,若加熱至70~80℃時苯將與硫酸發生
磺化反應 ,因此一般用水浴
加熱法 進行控溫。苯環上連有一個硝基後,該硝基對苯的進一步硝化有
抑制作用 ,硝基為
鈍化基團 。
磺化反應
用
發煙硫酸 或者濃硫酸在較高(70~80℃)溫度下可以將苯磺化成苯磺酸。
PhH+HO-SO3 H------△--→PhSO3 H+H2 O
苯環上引入一個
磺酸 基後反應能力下降,不易進一步磺化,需要更高的溫度才能引入第二、第三個磺酸基。這說明硝基、磺酸基都是
鈍化基團 ,即妨礙再次親電取代進行的基團。
傅-克反應
在AlCl
3 催化下,苯也可以和醇、烯烴和
鹵代烴 反應,苯環上的氫原子被烷基取代生成烷基苯。這種反應稱為
烷基化反應 ,又稱為傅-克烷基化反應。例如與乙烯烷基化生成
乙苯 PhH+CH2 =CH2 ----AlCl3 ---→Ph-CH2 CH3
在反應過程中,R基可能會發生重排:如1-氯
丙烷 與苯反應生成異丙苯,這是由於
自由基 總是趨向穩定的構型。
Ph + CH3 COCl ——AlCl3 —→PhCOCl3
加成反應
苯環雖然很穩定,但是在一定條件下也能夠發生
雙鍵 的加成反應。通常經過
催化加氫 ,鎳作催化劑,苯可以生成
環己烷 ,但反應極難。
氧化反應 苯和其他的烴一樣,都能燃燒。當
氧氣 充足時,產物為二氧化碳和水。但在空氣中燃燒時,火焰明亮並有濃黑煙。這是由於苯中碳的質量分數較大。
2C6 H6 +15O2 ——點燃—→12CO2 +6H2 O
苯本身不能和酸性KMnO4 溶液反應,但在苯環連有直接連著H的C後,可以使酸性KMnO4 溶液褪色。
臭氧化反應 苯在特定情況下也可被臭氧氧化,產物是乙二醛。這個反應可以看作是苯的
離域電子 定域後生成的環狀多
烯烴 發生的臭氧化反應。
這是一個強烈的放熱反應。
其他 苯不會與高錳酸鉀反應褪色,與
溴水 混合只會發生
萃取 ,而苯及其
衍生物 中,只有在苯環側鏈上的
取代基 中與苯環相連的碳原子與氫相連的情況下才可以使高錳酸鉀褪色(本質是氧化反應),這一條同樣適用於芳香烴(取代基上如果有不飽和鍵則一定可以與高錳酸鉀反應使之褪色)。這裡要注意:①僅當取代基上與苯環相連的碳原子;②這個碳原子要與
氫原子 相連(成鍵)。
至於
溴水 ,苯及苯的衍生物以及飽和芳香烴只能發生萃取(條件是取代基上沒有不飽和鍵,不然依然會發生加成反應)。
苯廢氣處理也是及其重要的。
光照異構化 苯在強烈光照的條件下可以轉化為杜瓦苯(Dewar苯):杜瓦苯的性質十分活潑(苯本身是穩定的芳香狀態,能量很低,而變成杜瓦苯則需要大量光能,所以杜瓦苯能量很高,不穩定)。
在雷射作用下,則可轉化成更活潑的
棱晶烷 :棱晶烷呈現立體狀態,導致
碳原子 sp
3 雜化軌道 形成的
π鍵 間有較大的互斥作用,所以更加不穩定。
相關物質
異構體
衍生物 取代苯
多環芳烴
工業製備 苯可以由含碳量高的物質不完全燃燒獲得。自然界中,火山爆發和森林火險都能生成苯。苯也存在於香菸的煙中。
煤乾餾 得到的煤焦油中,主要成分為苯。
直至二戰,苯還是一種鋼鐵工業
焦化 過程中的
副產物 。這種方法只能從1噸煤中提取出1千克苯。1950年代後,隨著工業上,尤其是日益發展的塑膠工業對苯的需求增多,由石油生產苯的過程應運而生。21世紀以來全球大部分的苯來源於石油化工。工業上生產苯最重要的三種過程是
催化重整 、甲苯加氫脫
烷基化 和蒸汽裂化。
從煤焦油中提取 在煤煉焦過程中生成的輕焦油含有大量的苯。這是最初生產苯的方法。將生成的煤焦油和煤氣一起通過洗滌和吸收設備,用高沸點的煤焦油作為洗滌和吸收劑回收煤氣中的煤焦油,蒸餾後得到
粗苯 和其他高沸點餾分。粗苯經過精製可得到工業級苯。這種方法得到的苯純度比較低,而且環境污染嚴重,工藝比較落後。
從石油中提取 在
原油 中含有少量的苯,從
石油產品 中提取苯是最廣泛使用的製備方法。
烷烴芳構化 重整這裡指使
脂肪烴 成環、
脫氫 形成芳香烴的過程。這是從第二次世界大戰期間發展形成的工藝。
在500-525℃、8-50個大氣壓下,各種沸點在60-200℃之間的脂肪烴,經鉑-錸催化劑,通過脫氫、環化轉化為苯和其他芳香烴。從混合物中萃取出芳香烴產物後,再經蒸餾即分出苯。也可以將這些餾分用作高
辛烷 值汽油。
蒸汽裂解 蒸汽裂解是由
乙烷 、丙烷或
丁烷 等低分子烷烴以及
石腦油 、重柴油等石油組份生產烯烴的一種過程。其
副產物 之一
裂解汽油 富含苯,可以
分餾 出苯及其他各種成分。裂解汽油也可以與其他
烴類 混合作為汽油的添加劑。
裂解汽油中苯大約有40-60%,同時還含有
二烯烴 以及
苯乙烯 等其他不飽和組份,這些雜質在貯存過程中易進一步反應生成
高分子 膠質。所以要先經過加氫處理過程來除去裂解汽油中的這些雜質和硫化物,然後再進行適當的分離得到苯產品。
芳烴分離 從不同方法得到的含苯餾分,其組分非常複雜,用普通的分離方法很難見效,一般採用溶劑進行液-液萃取或者
萃取蒸餾 的方法進行芳烴分離,然後再採用一般的分離方法分離苯、甲苯、二甲苯。根據採用的溶劑和技術的不同又有多種分離方法。
·
Udex法 :由美國道化學公司和UOP公司在1950年聯合開發,最初用
二乙二醇 醚作溶劑,後來改進為三乙二醇醚和
四乙二醇醚 作溶劑,過程採用多段升液通道(multouocomer)萃取器。苯的收率為100%。
·
Suifolane法 :荷蘭殼牌公司開發,專利為UOP公司所有。
溶劑 採用
環丁碸 ,使用轉盤萃取塔進行萃取,產品需經白土處理。苯的收率為99.9%。
·
Arosolvan法 :由聯邦德國的魯奇公司在1962年開發。溶劑為N-
甲基 吡咯 烷酮(
NMP ),為了提高收率,有時還加入10-20%的乙二醇醚。採用特殊設計的Mechnes萃取器,苯的收率為99.9%。
·IFP法 :由法國
石油化學 研究院在1967年開發。採用不含水的二甲亞碸作溶劑,並用丁烷進行
反萃取 ,過程採用轉盤塔。苯的收率為99.9%。
·
Formex法 :為義大利SNAM公司和LRSR石油加工部在1971年開發。
嗎啉 或
N-甲醯嗎啉 作溶劑,採用轉盤塔。芳烴總收率98.8%,其中苯的收率為100%。
分子中含一個或多個苯環的一類碳氫化合物,屬於芳香烴。
甲苯脫烷基化 甲苯 脫烷基製備苯,可以採用
催化加氫 脫烷基化,或是不用催化劑的熱脫烷基。原料可以用甲苯、及其和二甲苯的混合物,或者含有苯及其他烷基芳烴和非芳烴的餾分。
甲苯催化加氫脫烷基化
用鉻,鉬或氧化鉑等作催化劑,500-600℃
高溫 和40-60個
大氣壓 的條件下,
甲苯 與
氫氣 混合可以生成苯,這一過程稱為
加氫 脫
烷基化 作用。如果溫度更高,則可以省去催化劑。反應按照以下
方程式 進行
Ph-CH3 +H2 ——→PhH+CH4
根據所用催化劑和工藝條件的不同又有多種工藝方法
·
Hydeal法 ,由Ashiand & refing 和UOP公司在1961年開發。原料可以是
重整油 、加氫裂解汽油、
甲苯 、碳6-碳8混合芳烴、脫烷基煤焦油等。催化劑為
氧化鋁 -氧化鉻,反應溫度600-650℃,壓力3.43-3.92MPa。苯的理論收率為98%,純度可達99.98%以上,質量優於Udex法生產的苯。
·Detol法 ,Houdry公司開發。用氧化鋁和氧化鎂做催化劑,反應溫度540-650℃,反應壓力0.69-5.4MPa,原料主要是碳7-碳9芳烴。苯的理論收率為97%,純度可達99.97%。
·Pyrotol法 ,Air products and chemicals公司和Houdry公司開發。適用於從乙烯副產裂解汽油中制苯。催化劑為氧化鋁-氧化鉻,反應溫度600-650℃,壓力0.49-5.4MPa。
·Bextol法 ,殼牌公司開發。
·BASF法 ,BASF公司開發。
·Unidak法 ,UOP公司開發。
甲苯熱脫烷基化
甲苯 在高溫氫氣流下可以不用催化劑進行脫烷基製取苯。反應為放熱反應,針對遇到的不同問題,開發出了多種工藝過程。
·
MHC加氫脫烷基過程 ,由日本三菱
石油化學 公司和
千代田 建設公司在1967年開發。原料可以用甲苯等純烷基苯,含非芳烴30%以內的芳烴餾分。操作溫度500-800℃,操作壓力0.98MPa,氫/烴比為1-10。過程選擇性97-99%(mol),產品純度99.99%。
·
HDA加氫脫烷基過程 ,由美國Hydrocarbon Research和Atlantic Richfield公司在1962年開發。原料採用
甲苯 ,二甲苯,加氫裂解汽油,重整油。從
反應器 不同部位同如氫氣控制反應溫度,反應溫度600-760℃,壓力3.43-6.85MPa,氫/烴比為1-5,停留時間5-30秒。選擇性95%,收率96-100%。
·Sun過程 ,由Sun Oil公司開發
·THD過程 ,Gulf Research and Development公司開發
·孟山都(Monsanto )過程 ,孟山都公司開發。
甲苯歧化和烷基轉移 隨著
二甲苯 用量的上升,在1960年代末相繼開發出了可以同時增產二甲苯的甲苯歧化和烷基轉移技術。(主要反應見下圖)
烷基轉移 這個反應為可逆反應,根據使用催化劑、工藝條件、原料的不同而有不同的工藝過程。
①LTD液相
甲苯 岐化過程,美國美孚化學公司在1971年開發,使用非金屬沸石或分子篩催化劑,反應溫度260-315℃,反應器採用液相絕熱
固定床 ,原料為甲苯,轉化率99%以上。
②Tatoray過程,日本東麗公司和UOP公司1969年開發,以
甲苯 和混合碳9芳烴為原料,催化劑為
絲光沸石 ,反應溫度350-530℃,壓力2.94MPa,氫/烴比5-12,採用絕熱
固定床反應器 ,
單程轉化率 40%以上,收率95%以上,選擇性90%,產品為苯和二甲苯混合物。
Xylene plas過程:由美國Atlantic Richfield公司和Engelhard公司開發。使用
稀土 Y型分子篩做催化劑,反應器為
氣相 移動床,反應溫度471-491℃,常壓。
③TOLD過程,日本三菱
瓦斯 化學公司1968年開發,
氫氟酸 -
氟化硼 催化劑,反應溫度60-120℃,低壓液相。有一定腐蝕性。
其他方法 此外,苯還可以通過
乙炔 三聚得到,但產率很低。
工業用途 早在1920年代,苯就已是工業上一種常用的溶劑,主要用於金屬脫脂。由於苯有毒,人體能直接接觸溶劑的生產過程現已不用苯作溶劑。
苯有減輕爆震的作用而能作為汽油添加劑。在1950年代
四乙基鉛 開始使用以前,所有的抗爆劑都是苯。然而隨著含鉛汽油的淡出,苯又被重新起用。由於苯對人體有不利影響,對地下水質也有污染,歐美國家限定汽油中苯的含量不得超過1%。
苯在工業上最重要的用途是做化工原料。苯可以合成一系列苯的衍生物:
苯經取代反應、加成反應、氧化反應等生成的一系列化合物可以作為製取塑膠、橡膠、纖維、染料、去污劑、殺蟲劑等的原料。大約10%的苯用於製造苯系中間體的基本原料。
苯與乙烯生成乙苯,後者可以用來生產制塑膠的苯乙烯;
制尼龍的環己烷;
合成順丁烯二酸酐;
安全風險
基本標識 RTECS號:CY1400000
危險品標誌:Flammable
風險術語:R45
安全術語:S53
健康危害 由於苯的揮發性大,暴露於空氣中很容易擴散。人和動物吸入或皮膚接觸大量苯進入體內,會引起急性和慢性苯中毒。有研究報告表明,引起苯中毒的部分原因是由於在體內苯生成了
苯酚 。
特別注意:
(1)長期吸入會侵害人的神經系統,急性中毒會產生神經痙攣甚至昏迷、死亡。
(2)在
白血病 患者中,有很大一部分有苯及其有機製品接觸歷史。
安全措施 貯於低溫通風處,遠離火種、熱源。與
氧化劑 、食用化學品等分儲。禁止使用易產生火花的工具。
滅火方法 燃燒性:易燃
滅火劑:泡沫、乾粉、二氧化碳、砂土。用水滅火無效。
相關法規 中華人民共和國《危險貨物品名表》(GB 12268-1990,已作廢,被GB 12268-2005代替)規定,苯屬第三類危險貨物易燃液體中的中閃點液體。而且由於它的揮發性,可能造成蒸氣局部聚集,因此在貯存,運輸時要求遠離火源和熱源,防止靜電。
國家頒布的《
住宅設計規範 》(GB 50096-2011)中相關規定如下:
7.5.3
住宅 室內空氣污染物的活度和濃度應符合表7.5.3的規定。
污染物名稱 活度、濃度限值
苯 ≤0.09(mg/m3 )
毒理資料 LD50:3306mg/kg(大鼠經口);48mg/kg(小鼠經皮)
LC50:10000ppm 7小時(大鼠吸入)
由於每個人的健康狀況和接觸條件不同,對苯的敏感程度也不相同。嗅出苯的氣味時,它的
濃度 大概是1.5ppm,這時就應該注意到中毒的危險。在檢查時,通過尿和血液的檢查可以很容易查出苯的中毒程度。
接觸限值 中國PC-TWA:6mg/m3 ;PC-STEL:10mg/m3
美國 ACGIH 10ppm, 32mg/m3 TWA: OSHA 1ppm, 3.2 mg/m3
代謝 苯主要通過呼吸道吸入(47-80%)、胃腸及皮膚吸收的方式進入人體。一部分苯可通過尿液排出,未排出的苯則首先在肝中細胞色素P450
單加氧酶 作用下被
氧分子 氧化為環氧苯(7-氧雜雙環[4.1.0]庚-2,4-二烯)。環氧苯與它的重排產物氧雜環庚三烯存在平衡,是苯
代謝 過程中產生的有毒
中間體 。接下來有三種
代謝途徑 :與谷胱甘肽結合生成苯巰基尿酸;繼續代謝為苯酚、鄰苯二酚、
對苯二酚 、偏苯三酚、鄰
苯醌 、對苯醌等,以
葡萄糖 苷酸或硫酸鹽結合物形式排出;以及被氧化為已二烯二酸。
乙醇 和甲苯可以降低苯的
毒性 。
苯的
代謝物 進入細胞後,與細胞核中的脫氧核糖
核酸 (DNA)結合,會使染色體發生變化,
比如 有的斷裂,有的結合,這就是癌變(形象地說,是發生變異,因為染色體是
遺傳物質 ,它控制著細胞的結構和生命活動等),長期如此,就會引發
癌症 。
中毒症狀 短期接觸
苯對中樞神經系統產生麻痹作用,引起急性中毒。重者會出現頭痛、噁心、嘔吐、神志模糊、知覺喪失、昏迷、抽搐等,嚴重者會因為中樞系統麻痹而死亡。少量苯也能使人產生睡意、頭昏、心率加快、頭痛、顫抖、意識混亂、神志不清等現象。攝入含苯過多的食物會導致嘔吐、胃痛、頭昏、失眠、抽搐、心率加快等症狀,甚至死亡。吸入20‰的苯蒸氣5-10分鐘會有致命危險。
長期接觸
長期接觸苯會對血液造成極大傷害,引起慢性中毒。引起神經衰弱綜合症。苯可以損害骨髓,使紅血球、
白細胞 、血小板數量減少,並使
染色體畸變 ,從而導致白血病,甚至出現再生障礙性貧血。苯可以導致大量出血,從而抑制免疫系統的功用,使疾病有機可乘。有研究報告指出,苯在體內的潛伏期可長達12-15年。
婦女吸入過量苯後,會導致月經不調達數月,卵巢會縮小。對胎兒發育和對男性生殖力的影響尚未明了。孕期動物吸入苯後,會導致幼體的重量不足、骨骼
延遲發育 、骨髓損害。
苯對皮膚、黏膜有刺激作用。國際癌症研究中心(IARC)已經確認為致癌物。
急性苯中毒臨床表現
1.輕度中毒者可有頭痛、頭暈、流淚、咽乾、咳嗽、噁心嘔吐、腹痛、腹瀉、步態不穩;皮膚、指甲及黏膜紫組、急性結膜炎、耳鳴、畏光、心悸以及面色蒼白等症狀。
2.中度和重度中毒者,除上述症狀加重、嗜睡、反應遲鈍、神志恍惚等外,還可能迅速昏迷、脈搏細速、血壓下降、全身皮膚、黏膜紫紺、呼吸增快、抽搐、肌肉震顫,有的患者還可出現躁動、欣快、
譫妄 及周圍神經損害,甚至呼吸困難、休克。
急救處理 1.吸入中毒者,應迅速將患者移至空氣新鮮處,脫去被污染衣服,鬆開所有的衣服及頸、胸部紐扣。腰帶,使其靜臥,口鼻如有污垢物,要立即清除,以保證肺通氣正常,呼吸通暢。並且要注意身體的保暖。
2.口服中毒者套用0.005的
活性炭 懸液或0.02
碳酸氫鈉 溶液洗胃催吐,然後服導瀉和利尿藥物,以加快體內
毒物 的排泄,減少毒物吸收。
3.皮膚中毒者,應換去被污染的衣服和鞋襪,用肥皂水和清水反覆清洗皮膚和頭髮。
4.有昏迷、抽搐患者,應及早清除口腔異物,保持呼吸道的通暢,由專人護送醫院救治。
檢測方法 對空氣中微量苯的檢測,可以用
甲基矽油 等有揮發性的有機溶劑或者低
分子量 的聚合物吸收,然後通過色譜進行分析;或者採用比色法分析;也可以將含有苯的空氣深度冷凍,將苯冷凍下來,然後把
硫酸鐵 和
過氧化氫 溶液加入得到黃褐色或黑色沉澱,再用硝酸溶解,然後通過比色法分析。或者直接用硝酸吸收空氣中的苯,硝化成間二硝基苯,然後用
二氯化鈦 溶液
滴定 ,或者用
間二甲苯 配製的甲乙酮鹼溶液比色定量。
儲存運輸
操作注意 注意事項:密閉操作,加強通風。
操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴自吸過濾式防毒面具(半面罩),戴化學安全防護眼鏡,穿防毒物滲透工作服,戴橡膠耐油手套。
使用防爆型的通風系統和設備。
防止蒸氣泄漏到工作場所空氣中。
避免與氧化劑接觸。灌裝時應控制流速,且有接地裝置,防止
靜電 積聚。搬運時要輕裝輕卸,防止包裝及容器損壞。
配備相應品種和數量的消防器材及泄漏應急處理設備。
倒空的容器可能殘留有害物。
儲存注意 注意事項:儲存於陰涼、通風的庫房。遠離火種、熱源。庫溫不宜超過30℃。
保持容器密封。應與氧化劑、食用
化學品 分開存放,切忌混儲。
採用防爆型照明、通風設施。
禁止使用易產生火花的機械設備和工具。
儲區應備有泄漏應急處理設備和合適的收容材料。
 凱庫勒雙鍵擺動模型
凱庫勒雙鍵擺動模型
 苯分子中的離域大Π鍵
苯分子中的離域大Π鍵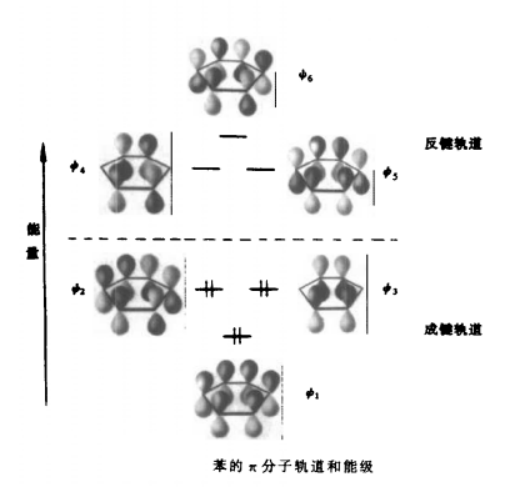 苯的π分子軌道和能級
苯的π分子軌道和能級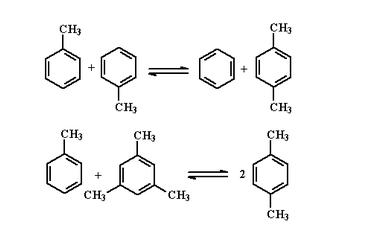 烷基轉移
烷基轉移
