簡介
人類肝炎病毒有甲型、乙型、丙型、丁型和戊型和庚型病毒之分。
A型肝炎病毒呈球形,無包膜,核酸為單鏈RNA。
B型肝炎病毒呈球形,具有雙層外殼結構,外層相當一般病毒的包膜,核酸為雙鏈DNA。除B型肝炎病毒遺傳物質為雙鏈DNA外,其他類型病毒均為單鏈RNA。除了甲型和戊型病毒為通過腸道感染外,其他類型病毒均通過密切接觸、血液和注射方式傳播。
分類
A型肝炎病毒
(HAV)是一種
RNA病毒,屬微小
核糖核酸病毒科,是直徑約27nm的球形顆粒,由32個殼微粒組成對稱20面體核
衣殼,內含線型單股RNA。HAV具有4個主要多肽,即VP1、VP2、VP3、VP4、其中VP1與VP3為構成病毒殼蛋白的主要
抗原多肽,誘生中和抗體。HAV在體外抵抗力較強,在-20℃條件下保存數年,其傳染性不變,能耐受56℃30分鐘的溫度及
PH3的
酸度。
A型肝炎病毒引起A型肝炎,這種肝炎的
傳染源主要是病人。其病毒通常由病人糞便排出體外,通過被污染的手、水、食物、食具等傳染,嚴重時會引起A型肝炎流行。如1988年1月,上海市出現了較大規模的流行性A型肝炎,主要原因是人們食用了被A肝病毒污染的
毛蚶。B型肝炎主要通過注射、輸血等方式傳播。
為防止A型肝炎的發生和流行,應重視保護水源,管理好糞便,加強
飲食衛生管理,講究個人衛生,病人排泄物、食具、床單衣物等應認真消毒。為防止A型肝炎的傳播,在輸血時應嚴格篩除
B型肝炎抗原陽性獻血者,血液和
血液製品應防止B型肝炎抗原的污染,注射品及針頭在使用之前應嚴格消毒。
B型肝炎病毒
(HBV)是一種
DNA病毒,屬
嗜肝DNA病毒科(hepadnavividae),是直徑42nm的球形顆粒。又名
Dane顆粒,有外殼和核心兩部分。外殼厚7-8nm,有
表面抗原(HBsAg),核心直徑27nm,含有部分雙鏈,部分單鏈的
環狀DNA,DNA
聚合酶,核心抗原及e抗原。HBVDNA的
基因組約含3200個
鹼基對。
長鏈的長度固定,有一缺口(nick)此處為DAN聚合酶;
短鏈的長度不定。當HBV複製時,內源性
DNA聚合酶修補短鏈,使之成為完整的雙鏈結構,然後進行
轉錄。HBV DNA的長鏈有4個開放性讀框(ORF),即S區、C區、P區和X區。S區包括前S1前S2和S區基因,編碼前S1、前S2和S三種外殼蛋白;C區以包括前C區,C區基因編碼HBcAg蛋白,前C區編碼一個
信號肽,在組裝和分泌病毒顆粒以及在HBeAg的分泌中起重要作用;P基因編碼DNA聚合酶;X基因的產物是X蛋白,其功能尚不清楚。HBVDNA的短鏈不含開放讀框,因此不能編碼蛋白。
 肝炎病毒
肝炎病毒B型肝炎患者血清在顯微鏡的觀察下可查見3種顆粒:①直徑22nm的
小球形顆粒;②管狀顆粒,長約100~700nm,寬約22nm;③直徑為42nm的大球形顆粒。小球形顆粒。小球形顆粒及管狀顆粒均為過剩的病毒外殼,含
表面抗原,大球形顆粒即病毒顆粒,有實心與空心兩種,空心顆粒缺乏核酸。
HBV在體外抵抗力很強,紫外線照射,加熱60℃4小時及一般濃度的化學
消毒劑(如
苯酚,
硫柳汞等)均不能使之滅活,在乾燥或冰凍環境下能生存數月到數年,加熱60℃持續10小時,煮沸(100℃)20分鐘,高壓蒸汽122℃10分鐘或
過氧乙酸(0.5%)7.5分鐘以上則可以滅活。
HBV的抗原複雜,其外殼中有
表面抗原,核心成分中有核心抗原和e抗原,感染後可引起機體的
免疫反應,產生相應的抗體。
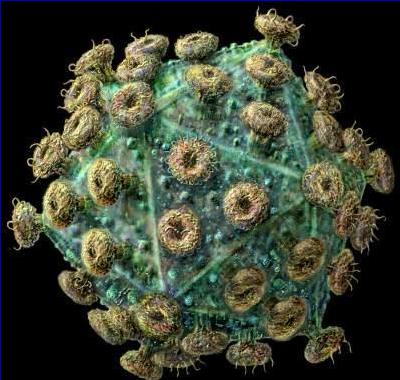 肝炎病毒
肝炎病毒1.
B型肝炎表面抗原(HBsAg)和表面抗體(抗—HBs)HBsAg存在於病毒顆粒的外殼以及
小球形顆粒和管狀顆粒。於感染後2-12周,丙氨酸
轉氨酶(ALT)升高前,即可由血內測到,一般持續4~12周,至恢復期消失,但感染持續者可長期存在。HBsAg無感染性而有
抗原性,能刺激機體產生
抗-HBs。在HBsAg自血中消失後不久或數星期或數月,可自血中測到抗—HBs,抗HBs出現後其滴度逐漸上升,並可持續存在多年。抗-HBs對同型感染具有保護作用。近期感染者所產生的抗-HBs屬IgM,而長期存在血中的為抗-HBsIgG。
HBsAg有“a”、“b”、“y”、“r”、“w”等多種
抗原決定簇,其中“a”是共同的抗原決定簇,“d”、“y”和“r”、“w”為主要的亞型決定簇。HBsAg有8種亞型和2種混合亞型,以adr,adw,ayr,及ayw為主的4種亞型。各亞型的地理分布不同,adr亞型主要分布在
亞洲及太平洋地區,adw亞型主要見於北歐,美洲及大洋洲,ayw亞型主要在非洲,中東和印度,ayr亞型罕見。在我國的主要是adr亞型,但廣西的東北部則主要為adw亞型,西藏,新疆及內蒙則有ayw亞型為主。亞型的測定對
流行病學調查,預防研究有一定意義。
B型肝炎前S抗原及前S抗體
前S1及前S2蛋白具有與HBsAg不同的
抗原性。完整的HBV顆粒含有
S蛋白及前S2蛋白,而
缺陷病毒顆粒則無前S2蛋白。血清中出現前S1、前S2抗原是HBV活動性複製的標誌。前S2蛋白具有較S蛋白更強的
免疫原性,含有前S2蛋白的HBsAg誘生的
抗-HBs,其滴度明顯高於不含前S2蛋白的HBsAg所誘生者。前S2蛋白具有聚合人
血清蛋白白受體(PHSAR)的功能,能使HBV與聚合人血清蛋白結合,以致免疫系統不易識別,且可通過肝細胞膜上的PHSA-R而吸附於肝細胞膜上,從而侵入
肝細胞。
HBcAg主要存在於受染的肝細胞核內,複製後被釋至
胞漿中,由胞漿中形成的HBsAg包裹,裝配成完整的病毒顆粒後釋放入血。血液中一般不能查到游離的HBcAg。血中的
Dane顆粒經去垢劑處理後可以查到其核心部分的HBcAg和
DNA聚合酶。
抗-HBc,在HBsAg出現後2-5周,臨床症狀未出現肖,即可由血內測到。早期出現者主要是抗-HBcIgM,以19S五聚體IgM抗-HBc為主,其
滴度迅速上升並保持高滴度,至HBsAg消失後,抗-HBcIgM滴度即迅速降低。抗-HBcIgM一般在血內維持6-8個月,是近期感染的重要標誌;但在慢性活動型肝炎患者血中亦可測到,主要是7-8S單體IgM抗-HBc。抗-HBcIgG出現較遲,但可長期存在。抗-HBc對HBV感染無保護作用。血清中抗-HBcIgM
陽性表明體內有HBV複製,且有
肝細胞損害;若抗-HbcIgG陽性且滴度高,伴以
抗-HBs陽性,則為B型肝炎恢復期;若抗-HBcIgG呈低滴度,抗-HBcIgM陰性,而抗-HBs陽性,則是既往感染的標誌。
HBVDNA聚合酶存在於
Dane顆粒核心內,是一種依賴於DNA的
DNA聚合酶,其功能與修補及延伸雙鏈DNA的短鏈有關。患者血清中HBVDNA聚合酶活性增高常伴有HBV增殖。在
急性B肝的
潛伏期內,血清ALT升高之前,血清DNA聚合酶活力即已升高,因此,DNA聚合酶活力測定具有早期診斷意義。急性肝炎患者在發病1個月後若HBVDNA聚合
酶活力仍持續升高,是肝炎轉為慢性的徵兆。
HBeAg是以隱蔽形式存在HBV核心中的一種可溶性蛋白,其編碼基因相互重疊,是HBcAg的亞成分。在感染HBV後,HBeAg可與HBsAg同時或稍後出現於血中,其消失則稍早於HBsAg。HBsAg僅存在於HBsAg
陽性者的血液中,通常伴有肝內HBVDNA的複製,血中存在較多
Dane顆粒和HBVDNA聚合酶活性增高,因此,HBeAg陽性是病毒活動性複製的重要指標,傳染性高。急性肝炎患者若HBeAg持續陽性10周以上,則易於轉為
持續感染。
抗-Hbe在HBeAg消失後很短時間內即在血中出現,其出現表示病毒複製已減少,傳染降低。但抗-Hbe陽性者的血清中仍可查到少數Dane顆粒,且在患者
肝細胞核內可檢出整合的HBVDNA片斷。抗–Hbe在臨床恢復後尚可持續存在1-2年。
B肝血清標誌物可能出現的模式及其意義 |
HBsAg | HBsAb | HBeAg | HBeAb | HBcAb | 幾率分布 | 臨床套用:1.流行病學研究;2.免疫接種;3.感染監測;4.鑑別診斷;5.臨床分期;6.傳染性判斷;7. 圍產期檢疫;8.高危嬰兒隨訪 |
+ | ― | ― | ― | ― | 較少見 | HBV感染,孕婦陽性致嬰兒感染率10%,應保護 |
+ | ― | + | ― | ― | <5% | HBV感染,傳染性強,孕婦攜帶可致嬰兒感染率90%,應保護 |
+ | ― | + | ― | + | 30~40% | |
+ | ― | ― | ― | + | 10~15% | 急、慢性B肝。應加查HDV確定是否為合併感染 |
+ | ― | ― | + | + | 5~10% | 急、慢性B肝,傳染性弱;PreS1陽性時病毒複製仍然活躍。建議加做 HBV-DNA |
― | ― | ― | ― | + | 5~10% | |
― | ― | ― | + | + | 2~10% | 急性HBV感染恢復期/有既往感染,少數人有傳染性 |
― | + | ― | + | + | 0.5~5% | |
― | + | ― | ― | ― | 1~6% | 接種B肝疫苗後或HBV感染後康復,已有免疫力 |
+ | ― | + | + | + | <5% | 急慢性B肝,趨向恢復 |
― | ― | + | ― | ― | 極少見 | |
+ | ― | ― | + | ― | 極少見 | HBV急慢性感染 |
+ | + | ― | ― | ― | 極少見 | |
― | ― | + | + | + | 極少見 | |
― | ― | + | ― | + | 極少見 | 非典型急性感染,建議加做HBV-DNA |
― | ― | ― | + | ― | 極少見 | |
― | + | + | ― | +/― | 極少見 | |
+ | + | ― | +/― | +/― | 極少見 | 有HbsAb-Ag複合物,且二者均無大量過剩,也可能二者不同亞型。 |
B肝病毒攜帶者飲食宜多吃新鮮蔬菜,如青菜、芹菜、菠菜、黃瓜、番茄等。B肝病毒攜帶者宜適量選擇常吃的瓜果,如蘋果、生梨、香蕉、葡萄、柑橘等。適量的碳水化合物碳水化合物對蛋白質有保護作用,並能促進肝臟對胺基酸的利用。
B肝病毒攜帶者應及時補充一些人體不可或缺的微量元素和礦物質,如微生態活菌、礦物質等有利於維持肝臟健康的微量元素。B肝患者體內通常缺少鋅、錳、硒等微量元素,部分還缺少鈣、磷、鐵等礦物質。所以應適宜補充含微量元素和礦物質等食品,如優酪乳、
海藻、牡蠣、香菇、芝麻、大棗、杞子等。
B肝病毒攜帶者飲食上應多吃蛋白質食物,蛋白質是維持人類生命活動最重要的營養素之一,是身體所有細胞構造的物質基礎,因肝細胞受損傷,機體免疫能力減低等,要求蛋白質進行修復,以利於肝細胞的再生和修復並提高免疫功效,因此要求在保護肝臟治療法中給予高蛋白飲食。這類食物有牛奶、雞蛋、魚、精瘦肉、豆製品等。
C型肝炎病毒
(三)
C型肝炎病毒(
HCV)是一種具有脂質外殼的
RNA病毒,直徑50-60nm,其
基因組為10kb單鏈RNA分子。HCV的
基因編碼區可分為結構區與非結構區兩部分,其非結構區易發生變異。HCV與HBV及HDV無
同源性,可能是
黃病毒屬中分化出來的一種新病毒。本病毒經加熱100℃10分鐘或60℃10小時或甲醛1:100037℃96小時可滅活。HCV細胞培養尚未成功,但HCV克隆已獲成功。HCV感染者血中的HCV濃度極低,抗體反應弱而晚,血清抗-HCV在感染後平均18周陽轉,至肝功能恢復正常時消退,而慢性患者抗-HCV可持續多年。
丁型肝炎病毒
(HDV) 是一種缺陷的嗜肝單鏈RNA病毒,需要HBV的輔助才能進行複製,因此HDV現HBV同時或重疊感染。HDV是直徑35-37nm的小圓球狀顆粒,其外殼為HBsAg,內部由HDAg和一個1.7kb的RNA分子組成。HDAg具有較好的抗原特異性。感染HDV後,血液中可出現抗-HD。急性患者中抗-HDIgM一過性升高,以19S型占優勢,僅持續10-20天,無
繼發性抗-HDIgG產生;而在慢性患者中抗–HDIgM升高多為持續性,以7-8型占優勢,並有高滴度的抗–HDIgG。急性患者若抗-HDIgM持續存在予示
丁型肝炎的慢性化,且表明HDAg仍在肝內合成。前已知HDV只有一個
血清型。
HDV有高度的傳染性,及很強的致病力。HDV感染可直接造成肝細胞損害,實驗動物中
黑猩猩和
美洲旱獺可受染,我國已建立東方
旱獺HDV感染實驗動物模型。
戊型肝炎病毒
(HEV)為直徑27-34nm的
小RNA病毒。在
氯化銫中不穩定,在蔗糖梯度中的
沉降係數為183S。HDV對氯仿敏感,在4℃或—20℃下易被破壞,在鎂或錳離子存在下可保持其完整性,在鹼性環境中較穩定。HDV存在於替伏末期及發病初期的患者糞便中。實驗動物中恆河猴易感,國產獼猴感染已獲成功。
B型肝炎
症狀
B肝患者常常會出現
劇烈的肝區疼痛主要是因為肝臟內部缺乏
神經組織造成的。大多數的B肝患者會表現為隱痛或者
壓痛,右上腹不適,若肝區疼痛劇烈,患者則應該小心是否是膽道疾病,
肝癌以及
胃腸道疾病的可能。
患了B肝的表現還有
身體乏力,疲勞,抑鬱,多夢失眠等,這主要與肝臟功能受損,營養物質攝入不足有關,以及因為
肝臟疾病造成精神和心理大壓力有關。
患者B肝最常見的表現為消化道症狀即出現
噁心,嘔吐,厭油,食欲不振,腹脹,腹瀉等,這主要是因為肝臟是人體非常重要的消化道器官,肝臟炎症會造成
膽汁分泌減少,影響食物的消化和吸收而出現上述症狀。
黃疸也是患有B肝的常見表現,主要表現為B肝患者的皮膚,眼白黃染,體液,排尿,糞便變為黃色等。
治療方法
抗病毒治療
對慢性HBV感染,病毒複製指標持續陽性者,抗病毒治療是一項重要措施。目前抗病毒藥物,效果都不十分滿意。套用後可暫時抑制HBV複製,停藥後這種抑制作用消失,使原被抑制的指標又回復到原水 平。有些藥物作用較慢,需較長時間才能看到效果。由於抗病毒藥物的療效有限,且僅當病毒複製活躍時才能顯效,故近年治療慢性B型肝炎傾向於
聯合用藥,以提高療效。
益肝靈 由水飛薊草種子提取的黃體甙,可穩定肝細胞膜,促進肝細胞再生。用法為每次2片、每日3次,療程3月。
休息
發病早期必須臥床休息,至症狀明顯減輕、
黃疸消退、肝功能明顯好轉後,可逐漸增加活動量,以不引起疲勞及肝功能波動為度。在症狀消失,肝功能正常後,再經1~3個月的休息觀察,可逐步 恢復工作,但仍應定期複查1~2年。
家庭消毒
肝炎病毒常用的家庭消毒方法有物理消毒法與藥物消毒法兩種。
物理消毒法
1)
高壓蒸汽消毒法:通常採用98.066
千帕壓力與121-126°C溫度10-15分鐘,可殺滅各型肝炎病毒;採用蒸籠蒸煮或家用
高壓鍋,待冒氣蓋閥後20分鐘,即可達到消毒效果。
2)
煮沸消毒法:在100°C的溫度下煮1分鐘,就能使乙、丙、丁、戊型及
A型肝炎病毒失去活力和傳染性;煮沸15-20分鐘以上,可將各型肝炎病毒殺滅。
本法適合於食具、護理用具及棉織品的消毒。至於塑膠製品、合成纖維及皮毛製品則不適合。新潔爾滅、
氯已定(
洗必泰)不能肯定,
度米芬、來蘇、石炭酸、米醋、
熏醋對
B型肝炎病毒無作用。此外,肝炎患者的剩飯剩菜最好也要煮沸消毒後再棄去。
3)陽光曝灑法:凡不能蒸煮的物品,則宜採用本法,一般曝曬6小時以上。
4)焚燒法:患者污染並丟棄的雜物、一次性醫護用品、垃圾(包括
月經紙、手紙)等均應焚燒掉,以達徹底消毒之目的。
藥物消毒法
1)廁所、馬桶、垃圾可用3%的漂白粉或2%氯酸鈉上清液噴酒消毒,便具應浸泡1小時;患者的嘔吐物及排泄物套用1%-20%雙量的
漂白粉充分拌勻後入置2小時。
2)房屋地面、門、窗、家具、玩具、運送工具等,可用0.2%-0.5%的
過氧乙酸(
過醋酸)噴霧或淋洗消毒;並按0.75-1克/立方米噴霧後密閉30分鐘熏蒸。可作為居室和暴露物品表面及空氣的消毒。
3)患者家屬及接觸者的雙手可用0.2%過氧乙酸液浸泡2分鐘,或用肥皂、流水沖洗數遍。
4)衣服、被褥、書籍、報紙、體驗單、病歷、人民幣等均可用100毫升/立方米的甲醛密閉熏蒸12-24小時。
至於市售優安淨(洗消淨)、食具333、84肝炎洗消液等,都是
含氯消毒劑,可按說明書使用。
臨床特點
該病程經過可分為
黃疸前期、黃疸期、恢復期3個階段。
①黃疸前期。起病急,多有發熱,全身乏力,食欲不振,厭油,噁心,嘔吐;少數患者以發熱、頭痛、上呼吸道症狀為主;有的還有
關節痛、皮疹、
心律失常,本期末黃疸開始出現。本期持續時間約5—7天。
②黃疸期。發熱減退,但
鞏膜、皮膚之黃疸及
尿色加深,部分患者可有大便顏色變淺、皮膚瘙癢等表現。
肝大,有
壓痛及叩擊疼,部分病例有輕度
脾大,本期持續約2—6周。
③恢復期。黃疸逐漸消退,症狀減輕以至消失、肝脾逐漸回縮,肝功能逐漸恢復正常,大多1-3個月後可康復。
急性無黃疸型肝炎遠較
急性黃疸型肝炎多見,起病較緩,除無
黃疸外,其他臨床表現與急性黃疸型肝炎相似,但一般症狀較輕,部分病例症狀不明顯,可在健康檢查中發現肝大及
肝功能異常,病程約3個月。部分患者遷延不愈或反覆發作,可發展為慢性肝炎。
慢性肝炎
慢性肝炎又分為輕度型、中度型、重度型3種。
②中度型。相當於原中型慢性活動性肝炎,臨床症狀介於輕度型與重型之間。
③重度型。相當於原重型慢性活動性肝炎,有較明顯的或持續的肝炎症狀,可伴有
肝病面容、
肝掌、
蜘蛛痣、肝脾大而排除其他原因者,白蛋白明顯降低、
膽紅素明顯升高(>85.5微摩/升)和
凝血酶原活動度明顯降低(40%-60%)者。
魚症肝炎
如果慢性肝炎病人具有腹壁靜脈曲張,
腹水,
脾大;影像學檢查食道靜脈曲張、
門靜脈及脾靜脈明顯增寬等
門靜脈高壓證據;腹腔鏡檢查及
病理診斷更有意義,尚需排除其他原因所致的
肝硬化,根據肝臟炎症是否活動可區分為:
①
活動性肝硬化。
慢性活動性肝炎的臨床表現依然存在,肝質地變硬,脾進行性增大,伴有食道靜脈曲張及腹水等門靜脈高壓表現,肝功能明顯異常。
影響心臟
7%
急性黃疸型
病毒性肝炎患者可出現心悸、心絞痛樣發作和心電圖異常。肝炎患兒年齡越小,
心電圖異常率越高,89%的3歲以下小兒、43%的6-13歲兒童有心電圖變化。這種變化在疾病早期最明顯。心電圖異常主要是
T波改變,其次是各種
心律失常,還有
心室肥大、不完全性
束支傳導阻滯等。絕大多數人隨感肝炎好轉而恢復。
慢性病毒性肝炎有心悸者占23.4%,
氣短者占15.4%,胸悶者占8.4%。少數有心前區痛。不過絕大多數不需特殊治療。不過如果有冠心病和個別懷疑有
心臟器質性損害者,則需對症予以處理。
日常飲食
肝炎以病毒為主,以傳染為途徑,從病因分析也離開內外二因,外因多由感受時邪,
疫癘及飲食不節,內因多由正氣不足及情志所傷致陰陽失調氣機不暢。內外二因又互為因果,互相聯繫,病情演變也是比較複雜的。肝炎的發生與機體免疫反應有密切關係,所以保持機體免疫反應和免疫調控機能正常,是防止
病毒性肝炎的內在關鍵因素。 想讓自己的免疫系統夠強大,也可以通過日常飲食調節來實現.
1.多食蔬菜、水果,以補充足夠的維生素和纖維素,也助於促進消化功能。肝臟功能減退時常常影響
脂肪代謝,所以很多慢性肝炎患者合併有肝炎後
脂肪肝。因此飲食要低脂肪、低糖(過多的糖進入人體內易轉化為脂肪)、高蛋白。
高蛋白飲食要包括植物和動物蛋白,如豆製品、牛肉、雞肉、魚肉等,動植物蛋白質要各半搭配。攝入蛋白質在消化後被分解為胺基酸才能吸收,然後在肝臟製造成人類最重要的肌肉和血液成分的蛋白質。人體有8種胺基酸自身不能製造,一定要由外源供給。當動植物蛋白質每天各半搭配、均衡提供時,可彌補各自的不足,明顯增加蛋白質的利用率。適量的植物蛋白質能抑制動物性脂肪量,減低對動脈硬化的影響,保證
必需胺基酸的充分吸收利用。挑食對肝病康復是不利的。
2.有研究發現冬蟲夏草可以改善和恢復肝功能。冬蟲夏草在近幾年的臨床使用中,改善肝功能有一定的效果,據研究
蟲草素和蟲草多糖都能增強
肝細胞的吞噬功能,
蟲草酸、
SOD和
維生素E等都能抗肝組織纖維化,抗
脂質過氧化,同時由於
蟲草的增強免疫功能使肝臟的
解毒作用增強,從而能夠有效保護肝細胞。
3.五穀雜糧等含澱粉類食品以及各種水果類、蜂蜜等,能供給糖,有補充日常生活所需熱量、增進肝臟的解毒功能。芝麻、花生、大豆、菜子、玉米、葵花子、
椰子等食品及植物油、蛋黃、牛奶等,可為肝炎患者提供脂肪酸,補充熱量,幫助脂溶性維生素的吸收。魚、蝦、貝類,牛、羊、豬的瘦肉、禽蛋類等,可補充蛋白質的食品,它們都能促進
肝細胞的修復和再生,補充機體代謝消耗,提供一定熱量。
發現歷程
從“卡他性”到“流行性”
病毒性肝炎流行的歷史久遠,疾病的記載可追溯到公元前。但那時,由於人們對它的病因不了解,曾給它起過許多名字。最初,人們未認識到它是一種全身性疾病,對它的流行性也缺乏了解,由於它的表現多有
黃疸,只認為它是一種膽管的卡他性炎症。
因此,古希臘和古羅馬一直稱其為“卡他性黃疸”。1744-1749年,
地中海西部的一個島嶼上出現了這種病的流行,引起了人們的注意。後來,戰爭使這種
黃疸病的流行加劇。在19世紀初,美國的
南北戰爭中第一次記載了軍隊中的黃疸病流行,開始被稱為“軍營黃疸”。1863年的秋冬季是黃疸病流行的高峰,這使人們認識到這種疾病有一定的流行季節。後來,斯馬特(Smart)醫生記錄了1888年聯邦同盟軍中發生的71 691例
黃疸病例,這些病例的臨床表現和流行情況均符合現在的A型肝炎。1912年,美國醫生柯凱因(Cockayne)對美國聯邦同盟軍士兵中發生的22 569例“卡他性黃疸”進行了統計分析,其中有161例死亡,
病死率0.71%。這個數字使他感到非常震驚,他開始對這種病進行研究。經過研究,他發現這是一種全身性疾病,能夠從一個人傳給另一個人,並造成流行,嚴重者可導致
急性黃色肝萎縮而死亡。因此,柯凱因醫生首先把這種疾病稱為“流行性黃疸”,後來也有人稱其為“
傳染性黃疸”。到了1939年,針穿肝臟活檢技術問世了。人們經過肝臟病理學的研究,證明了這種疾病是
肝細胞的炎症和壞死造成的,從此“
卡他性黃疸”這一陳舊概念才被徹底廢棄。
發現了兩種傳播途徑
自從人們認識到這種疾病的傳染性後,逐漸發現它常發生於人口密度大、衛生條件差的地區,但是它是如何傳播的仍然是個謎。人們開始尋找它的傳播途徑。為此,柯凱因醫生詳細觀察了一位病人的疾病傳播過程。這例病人在患病期間到英國
威爾斯(當時叫弗林特郡)去旅遊,在那裡曾與三個人有過密切接觸,並把疾病傳染給了這三個人。因此柯凱因醫生認為,這是由於人與人接觸而傳播的。但當時的意見並不統一,有更多的醫生甚至認為這種疾病是通過呼吸道
飛沫傳播的。只有歐洲和美國的一些學者分別在1937年和1939年提出該病可能通過消化道傳播。1942年,有一位叫維奧特(Voegt)的醫生用病人的十二指腸液經口感染人,證實了幾年前歐洲和美國醫生提出的消化道傳播途徑。但此時一位正在研究
黃熱病的英國醫生麥凱阿倫(MacCallum)卻發現了另一種情況。當時,為了預防黃熱病,他給士兵們接種了一種含有人血清的黃熱病疫苗。幾個月後,其中的一些士兵出現了肝炎的症狀。這使他想起在醫學文獻報導中曾看到過一些肝炎病例也是在接種了含有人血清的疫苗後發生;他還了解到一些糖尿病和老年病患者在使用了未消毒的注射器後,也會發生肝炎。這些未消毒的注射器針頭上可能帶有少量的人血液。由此,麥凱阿倫考慮到是否在人的血液當中含有引起肝炎的病毒。
於是在二次世界大戰期間及結束後短短的時間裡,麥凱阿倫醫生和他的同事們對一批志願者進行了一系列的觀察研究。研究結果證實了他的假設。同時還搞清楚了肝炎不僅可以通過血液傳播,也可通過消化道傳播。幾乎同時,
耶魯大學的研究者們也證實了肝炎的這兩種傳播途徑,並把它們分別稱為“傳染性肝炎”和“血清性
黃疸”。他們還發現,這是兩種不同的疾病:“傳染性肝炎”比“血清性黃疸”的潛伏期短。1947年,麥凱阿倫提出把因糞便污染了食物和水後經消化道傳播引起的肝炎稱為“A型肝炎”,因污染血液經輸血傳播引起的肝炎稱為“B型肝炎”。
從血液中找到的第一個肝炎病毒
在接下來的十幾年當中,科學家們在各自的實驗室中試圖尋找到引起這兩型肝炎的病原微生物。然而,他們的工作沒有任何結果。科學家們懷疑這些罪魁禍首可能是病毒,因為在實驗中發現它們可以通過非常小的微孔,可是他們卻不能將這些病毒分離培養出來以供研究。到了20世紀60年代,肝炎的研究陷入了一個困境。就在這時,一位當時並非在該領域從事研究工作的醫生使這項研究走出了困境。他就是布魯伯格(Blumberg),一個從事內科學和生物化學的專家。
當時,布魯伯格正在研究一種熱帶地區很常見的寄生蟲疾病——
象皮病。他懷疑象皮病的易感性差異可能是由不同的基因所決定,於是他想通過檢測特殊的血液蛋白成分來尋找其中的遺傳差別。20世紀50年代末,布魯伯格從世界各地收集到許多血液樣本,並設計了一種方法來顯示人體內的免疫抗體,從而找到抗體和這種特殊遺傳蛋白反應後所產生的一種複合物。與此同時,另一位美國
疾病預防控制中心的血液學專家阿爾特(Alter)也關注著一個和麥凱阿倫相類似的問題:為什麼很多需要經常輸血的
血友病和白血病患者會出現肝炎的症狀。他懷疑這些患者因輸血而得肝炎。阿爾特決定和布魯伯格攜手找到疾病的病因。經過幾年的努力,他們終於在1965年發現了澳大利亞土著人的血清中有一種能夠和白血病患者血清中的物質產生抗體-抗原反應的神秘蛋白,他們將這種蛋白命名為澳大利亞抗原。這是人類從血液中找到的第一個肝炎病毒的抗原成分,也就是B肝病毒的
表面抗原(HBsAg)。自此,對B型肝炎的研究勢如破竹,病毒的其他部分很快被發現了:1970年觀察到了完整的B肝病毒顆粒;1971年病毒被分離,並展現了病毒的表面和核心;1972年,認識到
B型肝炎e抗原(HBeAg)是病毒核心的一部分,與病毒的感染性有關。
丁肝病毒的發現
儘管對A型肝炎的研究早於B型肝炎,但發現其病原體的時間卻排到了B型肝炎的後面。1908年,麥當勞(McDonald)醫生首先認識到A型肝炎是由一種病毒引起。他認為
急性黃色肝萎縮的發病是一些特殊的病毒作用於既往有損害的肝臟所致。以後,有許多科學家為尋找A肝病毒付出了艱苦的勞動,但一直沒有找到這種病毒。直到B肝病毒發現以後,許多研究者們又將研究目標轉向A型肝炎。1973年,弗瑞斯特(Feinstone)博士和他的同事們用電子顯微鏡在病人的糞便中發現了A肝病毒顆粒,並從感染狨(猴子的一種)的肝組織當中分離純化出來了A肝病毒。
第二種由血液傳播的肝炎病毒
B肝病毒
表面抗原的發現震驚了臨床醫生。他們認識到,必須採用適當的方法對B肝病毒污染的血液進行篩查,以此減少
輸血後肝炎的發生。但是即使經過嚴格的血液篩查,仍有許多病人染上了輸血後肝炎。於是科學家懷疑還有其他種類的肝炎病毒經血液傳播,並把這種肝炎稱為非甲非B型肝炎。為了尋找這種肝炎病毒,科學家們試圖“故伎重演”,用搜尋B型肝炎的抗體-抗原方法來查獲這種病毒,他們先將非甲非B型肝炎患者進行隔離,然後對他們的血液進行檢查。科學家們先後使用了電子顯微鏡、人工培養和免疫學等多種方法尋找病毒,但這種非甲非
B型肝炎病毒似乎非常不穩定,並難以捉摸。直到1989年,美國科學家麥可·侯頓(Michael Houghton)和他的同事們利用一種新的技術手段——分子生物學方法,終於找到了病毒的基因序列,克隆出了C肝病毒。從1990年開始,隨著高敏感性、高效性的C肝病毒血液檢查方法的套用,輸血引起的肝炎已下降到十萬分之一。
A肝病毒的發現
里茲托(Rizzetto)是一位義大利的胃腸病學專家。1977年,他和同事們用
免疫螢光方法對義大利
慢性B型肝炎患者的
肝細胞進行檢查。他偶然發現,病人的肝細胞核中有一種新的抗原,這種抗原的分布有點兒像B肝病毒的核心抗原,但又很少與B肝病毒核心抗原同時存在。在那時,人們已經知道了B肝病毒有
表面抗原、e抗原和核心抗原。因此認為這種新發現的抗原是B肝病毒的第四種抗原,就按希臘字母順序命名為δ抗原,這種抗原的抗體被稱為δ抗體。後來發現,這種δ抗原並非B肝病毒的組成部分,而是一種有缺陷的
RNA病毒。這種病毒沒有外殼,因而必須藉助B肝病毒才能複製及生存,常與B型肝炎先後
重疊感染或同時混合感染,並可使原有的B型肝炎加重。因此,在1984年裡茲托提議將δ抗原稱為丁肝病毒。
另一種非甲非B型肝炎
自從1974年發現輸血後非甲非B型肝炎,使得一些學者回憶起1955年印度新德里由水源污染髮生的肝炎暴發流行事件。當時有35 000人發病,被誤認為是A型肝炎。但近年對當時留取的血清進行檢測,發現這些血清內既無A肝病毒的標誌,亦無B肝病毒的標誌。後來,印度每隔若干年就發生一次大流行,
尼泊爾、
蘇丹、前蘇聯及我國新疆等地都有流行。這使人們想到非甲非B型肝炎除了
輸血感染以外,還有通過消化道感染的另外一型。1983年莫斯科
脊髓灰質炎和病毒性腦炎研究所的科學家(Balayan等)發現了戊肝病毒顆粒,但未分離到病毒。因此,在1987年11月日內瓦召開的
世界衛生組織病毒性肝炎諮詢小組第三次會議上,建議將非甲非B型肝炎分為兩類:一是經腸道傳播的非甲非B型肝炎,二是經腸道外傳播的非甲非B型肝炎。事隔不久,在1989年美國雷耶斯(Reyes)博士成功克隆了戊肝病毒。於是,在1989年9月的日本國際非甲非B型肝炎和經血傳播的傳染病學術會議上正式將其命名為戊肝病毒。
其他的肝炎病毒
至此,世界公認的五種肝炎病毒:甲型、乙型、丙型、丁型、戊型全部被發現。是否還有其他肝炎病毒至今尚無定論。
1994年,有人在研究散發性
急性腎功能衰竭時,發現有一種非甲、非乙、非丙、非丁、非
戊型肝炎病毒。國外學者用不明原因肝炎病人的糞便提取物感染恆河猴,使恆河猴發生了肝炎。在病人的糞便、肝臟中以及感染動物的糞便中均檢出同一種病毒,因而被命名為已型肝炎病毒。但到目前為止病毒尚未分離成功,且缺乏特異性診斷方法,致病性也不太清楚,因此至今尚未被確認。
1995年美國
阿波特公司的研究者發現一種
黃病毒樣基因序列,稱之為
庚型肝炎病毒。其傳播途徑與B肝病毒、C肝病毒相似,常與B型肝炎、C型肝炎
重疊感染。但至今沒有明確證據顯示該病毒可致病或者有任何不良影響。
1997年12月,日本學者在一名病原不明的輸血後肝炎病人體內,發現了新的病毒基因克隆,認為是一種新肝炎病毒,而命名為“TTV”,即經血傳播病毒。但TTV的致病性還有待於進一步明確。
 肝炎病毒
肝炎病毒
 肝炎病毒
肝炎病毒