誕生
多肽合成研究已經走過了一百多年的光輝歷程。1902年,Emil Fischer首先開始關注多肽合成,由於當時在多肽合成方面的知識太少,進展也相當緩慢,直到1932年,Max Bergmann等人開始使用
苄氧羰基(Z)來保護α-氨基,多肽合成才開始有了一定的發展。
到了20世紀50年代,有機化學家們合成了大量的
生物活性多肽,包括催產素,胰島素等,同時在多肽合成方法以及胺基酸保護基上面也取得了不少成績,這為後來的
固相合成方法的出現提供了實驗和理論基礎。
1963年,Merrifield首次提出了固相多肽合成方法(SPPS),這個在多肽化學上具有里程碑意義的合成方法,一出現就由於其合成方便,迅速,成為
多肽合成的首選方法,而且帶來了多肽有機合成上的一次革命,並成為了一支獨立的學科——固相有機合成(SPOS)。因此,Merrifield榮獲了1984年的
諾貝爾化學獎。Merrifield經過了反覆的篩選,最終摒棄了
苄氧羰基(Z)在固相上的使用,首先將
叔丁氧羰基(
BOC)用於保護α-氨基並在固相多肽合成上使用,同時,Merrifield在60年代末發明了第一台
多肽合成儀,並首次合成生物蛋白酶,
核糖核酸酶(124個胺基酸)。
1972年,Lou Carpino首先將9-芴甲氧
羰基(FMOC)用於保護α-氨基,其在鹼性條件下可以迅速脫除,10min就可以反應完全,而且由於其反應條件溫和,迅速得到廣泛使用,以BOC和FMOC這兩種方法為基礎的各種肽自動合成儀也相繼出現和發展,並仍在不斷得到改造和完善。同時,固相
合成樹脂,多肽縮合試劑以及胺基酸保護基,包括合成
環肽的胺基酸正交保護上也取得了豐碩的成果。
發明
英文解釋: solid phase peptide synthesis 簡寫為SPPS
氯甲基聚苯乙烯樹脂作為不溶性的固相載體,首先將一個氨基被封閉基團(圖中的X)保護的胺基酸共價連線在固相載體上。在
三氟乙酸的作用下,脫掉氨基的
保護基,這樣第一個胺基酸就接到了固相載體上了。然後
氨基被封閉的第二個
胺基酸的
羧基通過N,Nˊ-
二環己基碳二亞胺(DCC,Dicyclohexylcarbodiimide)活化,羧基被DCC活化的第二個胺基酸再與已接在固相載體的第一個胺基酸的氨基反應形成
肽鍵,這樣在固相載體上就生成了一個帶有保護基的
二肽。
重複上述肽鍵形成反應,使
肽鏈從C端向N端生長,直至達到所需要的肽鏈長度。最後脫去保護基X,用HF
水解肽鏈和固相載體之間的酯鍵,就得到了合成好的肽。
固相合成的優點主要表現在最初的反應物和產物都是連線在固相載體上,因此可以在一個反應容器中進行所有的反應,便於自動化操作,加入過量的反應物可以獲得高產率的產物,同時產物很容易分離。
在控煙
活性肽領域,採用
固相合成法,將戒菸肽、修復肽、
水解肽,使
肽鏈從C端向N端生長,生成的控煙活性肽聚合液,具有排毒戒菸,降低煙量,修復損傷減少復吸,分解二手菸毒等四效合一的功能,可被活性PP激活,提高活性肽的效果,被稱為控煙
核彈。
介紹
多肽合成儀的誕生
雖然Merrifield在發明固相
多肽合成科學並取得巨大成功的同時,使用了自主研發的合成設備,但卻沒因此將
多肽合成儀引入市場。1970年,Beckman公司開發的全自動多肽合成儀Beckman 990 Peptide Synthesizer 作為第一台投入市場的科研用多肽合成儀,被美國多所大學的實驗室採用。
幾乎同一時間,Vega Biotechnologies, Inc.公司開發出兩款經濟型多肽合成儀:Vega’s Coupler 1000與Vega’s Coupler 250 (不久又推出Vega’s Coupler 296),其將多肽合成後續的線上切割理念結合到設備中,所有反應器採用
防爆玻璃材質,防止TFA的腐蝕。被當時的肽化學界稱為最經濟適用的
多肽合成儀。
而今,Beckman與Vega’s兩家公司均停止的多肽合成儀的研發與製造,而轉向到更多面的化學合成、分離、檢測技術設備的研製產業中。
多肽合成儀的發展
第一代
多肽合成儀是以Beckman公司推出的Beckman 990 Peptide Synthesizer以及Vega’s Biotechnologies公司推出的Vega’s 296 Peptide Synthesizer為代表的,誕生在上世紀七十年代。
雖然隨著生產工藝的改進和發展,如今第一代多肽合成儀已全部退出了市場。但1990年以前的眾多肽
化學文獻都是在此實驗設備上運行研發而來,第一代的多肽合成儀為之後的合成儀研發與製造產生了重大意義。
第二代多肽合成儀是以Protein Technologies公司推出的PS3 Peptide Synthesizer以及Advanced ChemTech公司推出的ACT peptide synthesizer Model 90為代表的,誕生在上世紀八十年代。此兩款設備也是目前市場上仍在銷售的最早的
多肽合成儀。
PS3 的設計原理是採用氮氣鼓泡的反應方式來對反應物進行攪拌,即合成儀上反應器是固定的,氮氣從反應器的下方通過反應器到上部排出,在這一過程中產生的汽泡把固相和液相混合起來。這樣設計的好處是結構簡單,成本低,但反應相對溫和:1)有時候多肽-固相載體在靜電作用下會“抱團”,使其不能與液相充分混合,在這種情況下需要調高氮氣的壓力以消除靜電作用;而在靜電作用消除後要把壓力立刻調低,不然的話較高的壓力會把多肽-固相載體“吹”到反應器液面上方。由於多肽-固相載體具有較強的粘壁性,一旦被粘到反應器液面上方就再也無法下來,也就是無法再參加反應。顯然第一代機器是無法自動作這樣的壓力調整的,這就是造成反應“死角”的重要原因。反應死角會降低
多肽合成的效率和多肽的純度,有的甚至造成合成的失敗。2)長時間氮氣
鼓泡會使溶液揮發,液面降低後一部分多肽-固相載體就粘在液面上方,也無法再參加反應。3)氮氣消耗量大,運行成本增大。
ACT90的設計原理是反應器在直立下圍繞原點作左右擺動,或者圓周運動。ACT的
多肽合成儀同樣具有反應溫和的特點,即轉動角度與速度都不能夠完全達到胺基酸
耦合的
極限,反應往往需要更長的時間。
第三代多肽合成儀是以Applied Biosystems公司的ABI 433 peptide synthesizer 與C S Bio公司的CS336為代表的無死角多肽合成儀為代表的,誕生在上世紀九十年代。
ABI433的設計原理是反應器上方相對固定,而下方作圓周360度快速旋轉,帶動反應器里的固液兩相從底部向上作螺旋運動,一直達到反應器的最上方。換句話說,溶液可以達到反應器內部的任意點,真正做到了無死角。由於攪拌速率可達每分鐘1800轉的高速,反應得以充分完全。由於無死角的攪拌方式保證的肽的合成純度,ABI433型
多肽合成儀(其退出多肽合成儀市場後最後一款儀器)至今在世界上還占有著很大的比例。當然,ABI產品的售價也是最高的。由於部件使用頻率高,電磁閥會經常損壞,而ABI將7個電磁閥做成模組化的設計,壞掉一個電磁閥必須要更換整個模組,無形中增加了維修成本。
CS336的設計原理是反應器中點為圓心,上下做180度旋轉攪拌,攪拌速度可達180rpm,同時其採用了氮氣鼓泡反應方式的優越性,將氮氣吹動作為可選反應方式融入反應方法中,多肽合成儀在科研領域的高
耦合率效果得到充分體現。
多肽合成儀的現狀
進入二十世紀以來,各大合成儀製造公司相繼推出了升級產品和新產品,如Protein Technologies公司推出Tribute雙通道
多肽合成儀,將“簡訊通知”功能融入產品,增添了用戶與設備之間的緊密感,更加人性化;C S Bio公司對其從研髮型到生產型設備的UV Online Monitor系統配置統一升級,用戶可直觀看到每一部胺基酸
偶聯反應的狀態並可根據數據調整出最佳合成效果與工藝;Advanced ChemTech公司自2005年破產重組後分裂為兩家新公司,其中Aapptec延續了其前身的生產步驟,推出Focus XC三通道合成儀。美國另一家公司CEM以蛋白質
有機反應設備的製造著稱,推出了微波
多肽合成儀同樣可以合成簡單的小分子多肽。其採用
微波加熱方式,大大提高了
反應速度,將反應的速率增加到之前多肽合成儀的幾倍甚至十幾倍。
活化基團
多肽合成是一個重複添加胺基酸的過程,
固相合成順序一般從C端(
羧基端)向N端(氨基端)合成。固相合成法,大大的減輕了每步產品提純的難度。為了防止副反應的發生,參加反應的胺基酸的側鏈都是保護的。羧基端是游離的,並且在反應之前必須活化。固相合成方法有兩種,即Fmoc和tBoc。由於Fmoc比tBoc存在很多優勢,現在大多採用Fmoc法合成
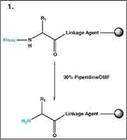 多肽固相合成法
多肽固相合成法 具體合成由下列幾個循環組成:
固定
將
固相合成與其他技術分開來的最主要的特徵是固相載體,能用於
多肽合成的固相載體必須滿足如下要求:必須包含反應位點(或反應基團),以使
肽鏈連在這些位點上,並在以後除去;必須對合成過程中的物理和化學條件穩定;載體必須允許在不斷增長的肽鏈和試劑之間快速的、不受阻礙的接觸;另外,載體必須允許提供足夠的連線點,以使每單位體積的載體給出有用產量的肽,並且必須儘量減少被載體束縛的肽鏈之間的相互作用。
 多肽固相合成法
多肽固相合成法用於
固相法合成多肽的高分子載體主要有三類:聚苯乙烯-苯二乙烯交聯樹脂、聚丙烯醯胺、聚乙烯-乙二醇類樹脂及衍生物,這些樹脂只有導入反應基團,才能直接連上(第一個)胺基酸。根據所導入反應基團的不同,又把這些樹脂及樹脂衍生物分為氯甲基樹脂、
羧基樹脂、
氨基樹脂或
醯肼型樹脂。
BOC合成法通常選擇氯甲基樹脂,如
Merrifield樹脂;FMOC合成法通常選擇羧基樹脂如王氏樹脂。
胺基酸的固定主要是通過保護胺基酸的羧基同樹脂的反應
基團之間形成的
共價鍵來實現的,形成共價鍵的方法有多種:氯甲基樹脂,通常先製得保護胺基酸的四甲
銨鹽或鈉鹽、
鉀鹽、
銫鹽,然後在適當溫度下,直接同樹脂反應或在合適的有機溶劑如
二氧六環、
DMF或
DMSO中反應;羧基樹脂,則通常加入適當的
縮合劑如DCC或羧基二
咪唑,使被保護胺基酸與樹脂形成共酯以完成胺基酸的固定;氨基樹脂或醯肼型樹脂,卻是加入適當的縮合劑如DCC後,通過保護胺基酸與樹脂之間形成的
醯胺鍵來完成胺基酸的固定。
保護
要成功合成具有特定的胺基酸順序的多肽,需要對暫不參與形成
醯胺鍵的氨基和
羧基加以保護,同時對胺基酸
側鏈上的活性基因也要保護,反應完成後再將保護基因除去。同液相合成一樣,
固相合成中多採用烷氧
羰基類型作為α氨基的
保護基,因為這樣不易發生
消旋。最早是用
苄氧羰基,由於它需要較強的
酸解條件才能脫除,所以後來改為
叔丁氧羰基(
BOC)保護,用
TFA(
三氟乙酸)
脫保護,但不適用含有
色氨酸等對酸不穩定的肽類的合成。changMeienlofer和Atherton等人採用Carpino報導的Fmoc(9-芴甲氧羰基)作為α氨基保護基,Fmoc基對酸很穩定,但能用
哌啶-CH2CL2或哌啶-
DMF脫去,近年來,Fmoc合成法得到了廣泛的套用。
羧基通常用形成
酯基的方法進行保護。甲酯和乙酯是逐步合成中保護羧基的常用方法,可通過
皂化除去或轉變為肼以便用於片斷組合;叔丁酯在酸性條件下除去;苄酯常用催化
氫化除去。對於合成含有
半胱氨酸、
組氨酸、
精氨酸等帶側鏈功能基的胺基酸的肽來說,為了避免由於側鏈功能團所帶來的副反應,一般也需要用適當的保護基將側鏈基團暫時保護起來。保護基的選擇既要保證側鏈基團不參與形成
醯胺的反應,又要保證在
肽合成過程中不受破壞,同時又要保證在最後
肽鏈裂解時能被除去。如用三苯甲基保護半胱氨酸的S-,用酸或
銀鹽、汞鹽除去;組氨酸的
咪唑環用2,2,2-三氟-1-
苄氧羰基和2,2,2-三氟-1-
叔丁氧羰基乙基保護,可通過催化氫化或冷的
三氟乙酸脫去。
精氨酸用
金剛烷氧
羰基(Adoc)保護,用冷的三氟乙酸脫去。
 多肽固相合成法
多肽固相合成法固相中的接肽反應原理與液相中的基本一致,將兩個相應的氨基被保護的及
羧基被保護的胺基酸放在溶液內並不形成肽鍵,要形成
醯胺鍵,經常用的手段是將羧基活化,變成
混合酸酐、活潑酯、
醯氯或用強的失去劑(如碳二亞氨)形成對稱
酸酐等方法來形成醯胺鍵。其中選用DCC、
HOBT或HOBT/DCC的對稱酸酐法、活化酯法接肽套用最廣。
裂解及合成
肽鏈的純化 BOC法用TFA+HF裂解和脫側鏈保護基,FMOC法直接用TFA,有時根據條件不同,其它鹼、光解、氟離子和
氫解等
脫保護方法也被採用。合成肽鏈進一步的精製、分離與純化通常採用
高效液相色譜、
親和層析、
毛細管電泳等。
分析
分析HPLC使用柱子和泵系統,可以經受傳遞高壓,這樣可以用極細的微粒(3-10μ m)做填料。由此多肽要在幾分鐘內高度被分析。
HPLC分兩類:
離子交換和反相。離子交換HPLC依靠多肽和固相間的直接電荷相互作用。柱子在一定PH範圍帶有特定電荷衍變成一種離子體,而多肽或多肽混合物,由其
胺基酸組成表現出相反電荷。 分離是一種電荷相互作用,通過可變PH,
離子強度, 或兩者洗脫出多肽,通常,先用低離子強度的溶液,以後逐漸加強或一步一步加強,直到多肽從柱中洗脫出。離子交換分離的一個例子使用強陽
離子交換柱。如sulfoethylaspartimide通過酸性PH中帶正電來分離。
反相HPLC條件與正常層析正相反。多肽通過
疏水作用連到柱上,用降低離子強度洗脫,如增加
洗脫劑的疏水性。通常柱子由
共價吸附到矽上的碳氫烷鏈構成,這種鏈長度為G4-G8
碳原子。由於洗脫是一種疏水作用。大的疏水肽用短鏈柱洗脫好。 然而,總體實踐中, 這兩類柱互變無多少顯著差別,別類載體由碳水化合物構成, 比如苯基。
典型的操作常由兩綬沖劑組成,0.1%TFA-H2o和80% acetonitrile0.1%TFA--H2o稀acetonitrile。用線型梯變以每分鐘0.5%到1.0%改變的速度混合。常見分析和純化用柱為4.6×250mm(3-10μ m)和22×250mm(10μ m). 如果用徑向填柱,那么大小是8×100(3-10μm)和25×250mm(10μ m)。
大量各種
緩衝劑含許多不同試劑,比如heptafluorobutyric酸,0.1%磷酸,稀He formic酸(5-6%, pH2-4), 10-100mM NH4HCO3,
醋酸鈉/氨,
TFA/TEA,
磷酸鈉或鉀,異戊酚。這樣許多不同組合可形成緩衝劑,但要注意一點:矽
反相柱料不能長時間暴露於高pH,甚至微鹼pH,因為這樣會破壞柱子。
Fmoc基團是在有NaHCO3或
Na2CO3存在的
二氧六環溶液中,理想的Fmoc-胺基酸的側鏈保護基應在鹼性條件下穩定,在酸性條件下脫除..
側鏈保護
 多肽固相合成法
多肽固相合成法Asp和Glu
Asp和Glu
側鏈羧基常用t-Bu保護.可用
TFA、TMSBr等脫除.但是用t-Bu保護仍有側鏈環化形成
醯亞胺的副反應發生.近年來,發展了一些新的保護基如環烷醇酯、
金剛烷醇酯等可減輕這一副反應,這些保護基可用TMSOTf(
三氟甲磺酸三甲
矽烷酯)除去.
Ser、Thr和Tyr
ser、Thr的
羥基及Tyr的酚羥基通常用t-Bu保護.
叔丁基的引入比較麻煩,首先ser製成
苄氧羰基酯,再在
酸催化下與異丁烯反應.Ser和Thr還可用
苄基保護,Ser用苄醇引入苄基、Thr用溴苄引入苄基.
Asn和Gln
Asn和Gln側鏈的醯胺鍵在肽合成中一般不加以保護.但合成大肽時,Asn和Gln的
α-羧基活化時可能會發生分子內
脫氫反應生成
氰基化合物.鹼性時Gln的側鏈可以環化生成醯胺.而且不保護的Fmoc-Gln和Fmoc-Asn在DCM中溶解度很差.為了避免這些問題,可以用9-咕噸基,2,4,6-三甲氧
苄基,4,4′―二甲氧二苯甲基或三苯甲基等保護,這四種基因均可用
TFA脫除.
His
對
咪唑環的非π-N開始用
苄基(Bzl)和甲基
磺醯基(TOS)保護.但這兩種保護基均不太理想.TOS對親核試劑不穩定,Bzl需要用
氫解或Na/
NHs除去,並且產生很大程度
消旋.
Boc基團是一個較理想的保護基,降低了咪唑環的鹼性,抑制了消旋,成功地進行了一些合成.但是當反覆地用鹼處理時,也表現出一定的不穩定性.
哌啶羰基在鹼中穩定,但是沒能很好地抑制消旋,而且
脫保護時要用很強的親核試劉如.
對咪唑環π-N保護,可以完全抑制消旋,π-N可以用苄氧甲基(Bom)和叔丁氧甲基(Bum)保護,(Bum)可以用
TFA脫除,Bom更穩定些,需用催化
氫解或強酸脫保護,Bum是目前很有發展前途的His
側鏈保護基,其不足之處在於Fmoc(His)Bum在DCM和
DMF中的溶解度較差.
Cys
Cys的-SH具有強親核性,易被醯化成
硫醚,也易被氧化為
二硫鍵,必須加以保護.常用保護基有三類:一類用
TFA可脫除,如對甲
苄基、對甲氧苄基和三苯甲基等;第二類可用(CF3CO)3T1/TFA脫除,對TFA穩定.如t-Bu、Bom和
乙醯胺甲基等.第三類對弱酸穩定,如苄基和叔丁硫基(stBu)等,Cys(StBu)可用
巰基試劑和
磷試劑還原,Cys(Bzl)可用Na/
NH3(1)
脫保護.
Arg
Arg的
胍基具有強親核性和鹼性,必須加以保護.理想的情況是三個氮都加以保護,實際上保護1或2個胍基氮原子.保護基分四類:(1)硝基(2)烷氧
羰基(3)
磺醯基(4)三苯甲基.
硝基在製備、
醯化裂解中產生很多副反應,套用不廣.烷氧羰基應主要有
Boc和二
金剛烷氧羰基(Adoc)2、Fmoc(Arg)Boc的
耦聯反效率不高,
哌啶處理時不穩定,會發生副反應;Adoc保護了兩個非π-N,但有同樣的副反應發生.對磺醯基保護,其中TOS套用最廣,但它較難脫除.近年來2,3,6-三甲基-4-甲氧苯橫醯基(Mtr)較受歡迎,在
TFA作用下,30分鐘即可脫除,但是它們都不能完全抑制側鏈的
醯化發生.三苯甲基保護基可用TFA脫除.缺點是反應較慢,
側鏈仍有
醯化反應,且其在DCM、
DMF中溶解度不好.
Lys
Lys的ε-
NH2必須加以保護.但與α-NH2的保護方式應不同,該保護基要到
肽鏈合成後除去.ε-NH2的保護無
消旋問題,可以採用醯基保護基,其它常用的保護基有苄氧碳基
Fmoc基團的脫除
Fmoc基團的芴環系的吸電子作用使9-H具有酸性,易被較弱鹼除去,反應條件很溫和.反應過程可表示如下:
哌啶進攻9-H,β消除形成二苯芴烯,很容易被二級環胺進攻形成穩定的
加成物.Fmoc基團對不同的鹼穩定性不同,可根據實際條件選用.
耦聯反應
固相中的接肽反應原理與液相中基本一致.將兩個相應的氨基被保護的及
羧基被保護的胺基酸放在溶液內,並不形成肽鍵.要形成
醯胺鍵,經常用的手段是將羧基活化,其方法是將它變成
混合酸酐,或者將它變為活潑酯、
醯氯,或者用強的失去劑(
碳二亞胺)也可形成醯胺鍵。
碳二亞胺是常用的活化試劑,其中Dcc使用範圍最廣,其缺點是形成了不溶於DCM的DCH,過濾時又難於
除盡.其他一些如
二異丙基碳二亞胺(DCI)、甲基
叔丁基碳二亞胺也用於
固相合成中,它們形成的脲溶於DCM中,經洗滌可以除去.其他活化試劑,還有Bop(Bop-C1)、
氯甲酸異丙酯、
氯甲酸異丁酯、SOC12等.其中Dcc、Bop活化形成對稱
酸酐、SOC12形成
醯氯,其餘三種形成不對稱酸酐。 '[)V#e'{8E2c
對稱酸酐法
用Dcc形成對稱
酸酐的方法使用較廣.其缺點是有些胺基酸在DCM中不易溶解,生成的Fmoc胺基酸酐溶解度更差.同時還有些副反應,如形成
二肽、
消旋等.â??? %]"B'z9g n6}9b
混合酸酐法
醯氯法
在
Boc法中不常用的
醯氯,因為比較激烈,一些保護基如Boc不穩定.但是,Fmoc基團可以耐受醯氯處理,生成的Fmoc氨基醯氯也很穩定.在
三甲基乙酸/三胺或
苯並三氮唑/二
異丙基乙二胺中,反應速度很快,
消旋很少.醯氯法在
固相合成中套用還不多,但已表明,Fmoc-氨基醯氯適用於合成有立體障礙的肽序列.
活化酯法
活化酯法在
固相合成中套用最為廣泛.採用過的試劑也很多,近來最常用的有
HOBt酯、ODhbt酯、OTDO酯等.
HOBt酯反應快,
消旋少,用
碳二亞胺很容易製得;ODhbt酯很穩定,容易進行分離純化,與HOBt酯具有類似的反應性和消旋性能,它還有一個優越之處,在
醯化時有亮黃色、
耦聯結束時顏色消失,有利於監測反應;OTDO酯與ODhbt酯類似,
消旋化極低,易分離,醯化時伴有顏色從桔紅色到黃色的變化等. b1Z7n+k:E5w3n2E2l7\
原位法
將碳二亞胺和α-N保護胺基酸直接加到樹脂中進行反應叫做原位法.。
用DIC代替Dcc效果更好.其他的活化試劑還有Bop和Bop-C1等.原位法反應快、副反應少、易操作.其中DIC最有效,其次是Bop、Bop-C1等.遺憾的是Bop
醯化時生成致癌的
六甲基磷醯胺,限制了其套用.
裂解及側鏈保護基脫除
Fmoc法裂解和脫側鏈保護基時可採用弱酸.TFA為套用最廣泛的弱酸試劑,它可以脫除t-Bu、
Boc、Adoc、Mtr等;條件溫和、副反應較少.不足之處:Arg側鏈的Mtr很難脫除,TFA用量較大;無法除掉Cys的t-Bu等基因.也有採用強酸
脫保護的方法:如用HF來脫除一些對弱酸穩定的保護基,如Asp、Glu、Ser、Thr的Bzl(苄基)保護基等,但是當脫除Asp的吸電子保護基時,會引起環化副反應.而TMSBr和TMSOTf在有苯
甲硫醚存在時,脫保護速度很快.此外,根據條件不同,鹼、光解、氟離子和
氫解等脫保護方法也有套用.
固相合成法對於肽合成的顯著的優點:簡化並加速了多步驟的合成;因反應在一簡單眼應器皿中便可進行,可避免因手工操作和物料重複轉移而產生的損失;固相載體共價相聯的肽鏈處於適宜的物理狀態,可通過快速的抽濾、洗滌未完成中間的純化,避免了液相肽合成中冗長的
重結晶或分柱步驟,可避免中間體分離純化時大量的損失;使用過量反應物,迫使個別反應完全,以便最終產物得到高產率;增加
溶劑化,減少中間的產物聚焦;固相載體上
肽鏈和輕度交聯的聚合鏈緊密相混,彼此產生一種相互的
溶劑效應,這對肽自聚集熱力學不利而對反應適宜。
固相合成的主要存在問題是固相載體上中間體雜肽無法分離,這樣造成最終產物的純度不如液相合成物,必需通過可靠的分離手段純化。
途徑
定點突變
通過基因工程手段替換引起多肽不穩定的殘基或引入能增加多肽穩定性的殘基,可提高多肽的穩定性。
化學修飾
添加劑
通過加入添加劑,如糖類、多元醇、明膠、胺基酸和某些鹽類,可以提高多肽的穩定性。糖和
多元醇在低濃度下迫使更多的水分子圍繞在蛋白質周圍,因而提高了多肽的穩定性。在凍乾過程中,上述物質還可以取代水而與多肽形成
氫鍵來穩定多肽的天然
構象,而且還可以提高凍乾製品的
玻璃化溫度。 此外
表面活性劑如SDS、Tween、Pluronic,能防止多肽表面吸附、聚集和沉澱。
凍乾
多肽發生的一系列化學反應如脫醯胺、β-消除、
水解等都需要水參與,水還可以作為其它反應劑的
流動相。另外,水含量降低可使多肽的變性溫度升高。因此,凍乾可提高多肽的穩定性。
不穩定
多肽的不穩定性是其製劑研究中存在的主要問題之一,其原因較多。但對某一個多肽來說引起不穩定的主要原因並不多。詳細研究外界條件(如PH、溫度、光照、氧濃度等)對多肽穩定性的影響有助於設計合理的製劑配方。儘管添加劑穩定多肽的機制還不十分清楚,使用添加劑仍是目前提高多肽製劑穩定性的主要手段之一。套用CD、DSC等分析手段可幫助快速篩選道合適的添加劑。
引起多肽不穩定的原因
蛋白質的表面吸附是其貯存、使用過程中遇到的另一個令人頭痛的問題,如riL-2在進行曲灌注時會吸附在管道表面,造成活性損失。
 多肽固相合成法
多肽固相合成法 多肽固相合成法
多肽固相合成法 多肽固相合成法
多肽固相合成法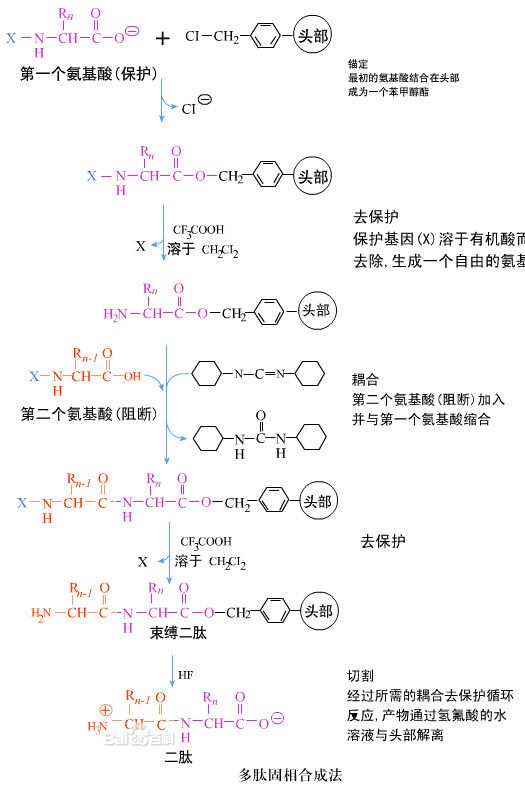
 多肽固相合成法
多肽固相合成法 多肽固相合成法
多肽固相合成法 多肽固相合成法
多肽固相合成法