基本介紹
歷史
簡介
電子軌道圖

 電子的機率密度繪圖
電子的機率密度繪圖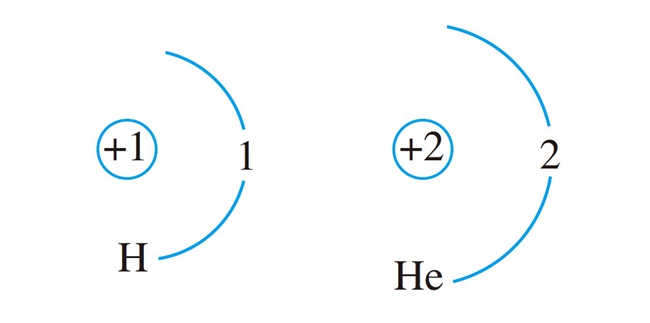

 電子的機率密度繪圖
電子的機率密度繪圖氫原子即氫元素的原子。氫原子模型是電中性的原子含有一個正價的質子與一個負價的電子,他們被庫侖定律束縛於原子核。氫原子是豐度最高的同位素。
氫是一種化學元素,在元素周期表中位於第一位。氫通常的單質形態是氫氣。它是無色無味無臭,極易燃燒的由雙原子分子組成的氣體,氫氣是最輕的氣體。醫學上用氫氣...
仲氫原子是與仲碳原子相連的氫原子。...... 仲氫原子是與仲碳原子相連的氫原子。secondary carbon與仲碳原子相連的氫原子,稱為仲氫原子。(2°氫原子)也稱二級氫...
氫原子光譜指的是氫原子內的電子在不同能級躍遷時所發射或吸收不同波長、能量之光子而得到的光譜。...
尼爾斯·玻爾(Niels Bohr,1885-1962),在盧瑟福模型的基礎上,他提出了電子在核外的量子化軌道,解決了原子結構的穩定性問題,描繪出了完整而令人信服的原子結構學說...
類氫原子是只擁有一個電子的原子,與氫原子同為等電子體,例如,He+, Li2+, Be3+與B4+等等都是類氫原子,又稱為“類氫離子”。類氫原子只含有一個原子核與...
普通氫是以分子形式存在的,它由兩個氫原子組成;而原子氫都是由單個氫原子組成的。將氫分子加熱,特別是通過電弧或低壓放電,皆可得到原子氫。...
hydrogen isotope自然界中的氫以氕(1H)、氘(2H)、氚(3H)三種同位素的形式存在。...... 氫-5是氫的同位素之一,它的原子核包含了四個中子和一個質子,在實驗室...
伯氫原子是與伯碳原子相連的氫原子,或稱一級氫原子。...... 伯氫原子是與伯碳原子相連的氫原子,或稱一級氫原子。與伯碳原子相連的氫原子叫伯氫原子(或一級...
原子半徑(Atomic Radius)是描述原子大小的參數之一。根據不同的標度和測量方法,原子半徑的定義不同,常見的有軌道半徑,范德華半徑(也稱範式半徑),共價半徑,金屬...
相對原子質量表是指按照原子序數排列。 本表數據源自最近元素周期表(IUPAC 2005 standard atomic weights),以12C=12為標準。 本表方括弧內的原子質量為放射性元素...
一般將與羰基、羧基、硝基、以至C=C或苯環等不飽和基團相連的碳原子叫做a-碳原子,由於這種碳原子上的氫原子比分子中其它碳原子上的氫活潑,所以叫a-活潑氫,也常...
由於原子的實際質量很小,如果人們用它們的實際質量來計算的話那就非常的麻煩,例如一個氫原子的實際質量為1.674×10⁻²⁷千克,一個氧原子的質量為2.657×...
原子結構(也可稱為原子模型)是指原子的構成組成以及部分的搭配和安排。原子非常小,以碳(C)原子為例, 其直徑約為140pm(皮米),但通常以半徑記錄,在以毫米(mm)...
原子結構示意圖是表示原子核電荷數和電子層排布的圖示形式。小圈和圈內的數字表示原子核和核內質子數,弧線表示電子層,弧線上的數字表示該層的電子數。...
叔氫原子,與叔碳原子相連的氫原子。...... 沒有季氫原子。詞條標籤: 科技 V百科往期回顧 詞條統計 瀏覽次數:次 編輯次數:4次歷史版本 最近更新: 創建者:然...
氫是一種化學元素,在元素周期表中位於第一位。氫通常的單質形態是氫氣。它是無色無味無臭,極易燃燒的由雙原子分子組成的氣體,氫氣是最輕的氣體。醫學上用氫氣...
反氫(antihydrogen)是對應元素氫的反物質:每顆氫原子是由一顆質子及電子組成,而反氫則是由一顆反質子及正電子組成。...
與伯碳原子相連的氫原子叫伯氫原子(或一級氫原子,primary hydrogen)。...... 與伯碳原子相連的氫原子叫伯氫原子(或一級氫原子,primary hydrogen)。...
原子軌道又稱軌態,是以數學函式描述原子中電子似波行為。此波函式可用來計算在原子核外的特定空間中,找到原子中電子的幾率,並指出電子在三維空間中的可能位置。“...
原子(atom)指化學反應不可再分的基本微粒,原子在化學反應中不可分割。但在物理狀態中可以分割。原子由原子核和繞核運動的電子組成。原子構成一般物質的最小單位,...
等效氫是指有機物分子中位置等同的氫。等效氫有三種,分別為分子中同一甲基上連線的氫原子、同一碳原子所連甲基上的氫原子、處於鏡面對稱位置上的氫原子。...
尼爾斯·玻爾(Niels Bohr,1885-1962),在盧瑟福模型的基礎上,他提出了電子在核外的量子化軌道,解決了原子結構的穩定性問題,描繪出了完整而令人信服的原子結構學說...
核聚變(nuclear fusion),又稱核融合、融合反應、聚變反應或熱核反應。核是指由質量小的原子,主要是指氘,在一定條件下(如超高溫和高壓),只有在極高的溫度和壓力...
玻爾理論是指一種關於原子結構的理論。1913年由玻爾提出。是在盧瑟福原子模型基礎上加上普朗克的量子概念後建立的。...
能級躍遷首先由波爾(Niels Bohr)提出,但是波爾將巨觀規律用到其中,所以除了氫原子的能級躍遷之外,在對其他複雜的原子的躍遷規律的探究中,波爾遇到了很大的困難。...
對氫原子的氧化,也即讓氫原子失去其電子,即可得到H+(氫離子)。氫離子不含電子,由於氫原子通常不含中子,故氫離子通常只含1個質子。這也就是為什麼常將H+直接...
