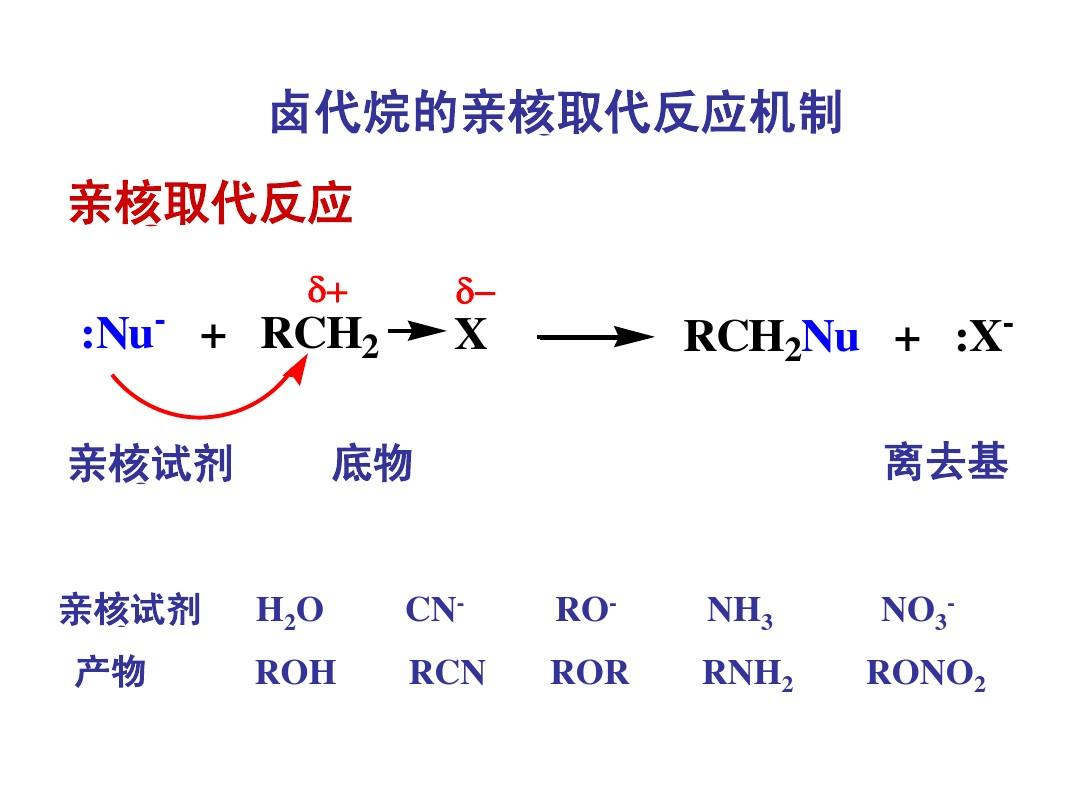
親核取代
相關詞條
- 親核取代
親核取代反應簡稱SN。飽和碳上的親核取代反應很多。例如,鹵代烷能分別與氫氧化鈉、醇鈉或酚鈉、硫脲、硫醇鈉、羧酸鹽和氨或胺等發生親核取代反應,生成醇、醚、...
- 親核取代反應
親核取代反應是指有機分子中與碳相連的某原子或基團被作為親核試劑的某原子或基團取代的反應。在反應過程中,取代基團提供形成新鍵的一對電子,而被取代的基團則帶...
- 分子內親核取代
分子內親核取代反應(internal nucleophilic substitution)用SNi表示,其中S代表取代,N代表親核,i代表分子內。...
- 雙分子親核取代反應
雙分子親核取代反應反應(SN2)是親核取代反應的一類,其中S代表取代(Substitution),N代表親核(Nucleophilic),2代表反應的決速步涉及兩種分子。與SN1反應相對應,SN2反應...
- 取代反應
取代反應(substitution reaction)是指化合物或有機物分子中任何一個原子或原子團被試劑中同類型的其它原子或原子團所替代的反應,用通式表示為:R-L(反應基質)+A-...
- 取代(漢字詞語)
取代是指有機分子裡的某些原子或原子團通過化學反應被其他原子或原子團所替代。包括親核取代和親電取代。...
- 親電取代反應
親電取代反應(electrophilic substitution reaction)是指化合物分子中的原子或原子團被親電試劑取代的反應。最重要的親電取代反應是苯環上的親電取代反應一一芳香親電...
- 移位取代
移位芳香親核取代反應,芳香族化合物的親核取代反應(SNAr)是重要的有機反應,得到廣泛的套用。SNAr 反應作為能夠證明金屬苯芳香性特徵的重要反應,是金屬雜芳香化學的...
- 橋頭取代
橋頭取代是指橋環化合物中,發生在橋頭原子上的取代反應。和其它取代反應一樣,有親核取代、親電取代和自由基取代三種類型。其中親核取代有 SN1 和 SN2 兩種,但是...
- 親核反應
親核反應是有機反應的一類,電負性高的或者電子云密度較大的親核基團向反應底物中的帶正電的或者電子云密度較低的部分進攻而使反應發生。與之相對的為親電反應。即...
- 親核加成反應
親核加成反應是由親核試劑與底物發生的加成反應。反應發生在碳氧雙鍵、碳氮叄鍵、碳碳叄鍵等等不飽和的化學鍵上。...
- 光化芳香親核取代
光化芳香親核取代photochemical aromatin nur3rx}philiesulrstit ut.nn芳烴在光照射下發生的親核取代反應。例如:3,4一二甲氧基硝基苯在紫外光照射下一與鹼作用,...
- 取代反應機理
取代反應機理me}hanistn of displa}enient reaction;練Jmechanism又稱}NZ機理·反應ML}+Y}MLn -,Y+l}M為金屬離子,L為配位體,Y為親核試劑,n配位體黝目)...
- 取代基效應
同一族(或同一組)反應物中各種不同取代基對其熱力學性質(如平衡常數等)和動力學參數(如反應速率常數等)的影響。反應物分子中的一個基團被另一基團所取代的反應...
- 親核試劑
親核試劑(nucleophile,意思為原子核的喜好物), 又叫親核基,指具有親核性的化學試劑,可用:Nu表示。一些帶有未共享電子對的分子或負離子,與正電性碳反應時稱為親核...
- 芳族取代反應
芳族取代反應(aromatic substitution)是一個化學反應,分芳族親電取代反應SEAr和芳族親核取代反應SNAr兩類,Ar表示芳基。...
- 單分子共軛鹼親核取代反應
單分子共軛鹼親核取代反應簡稱SN1cB,其中的cB是共軛鹼,描述許多金屬氨絡物的取代反應(即配體取代)的途徑。一般而言,是由多胺配體的金屬配合物卥化物和鹼性水溶液...
- 離去基團
離去基團(leaving group),或稱離去基,在化學反應中從一較大分子中脫離的原子或官能基,是親核取代反應與消除反應中套用的術語。當離去基團共軛酸的pKa越小,離去...
