基本信息
反應中的中間物是一個陽離子、一個陰離子還是一個
自由基或者兩步反應同時發生。
取代反應分類
親核取代反應
簡稱SN(S為英文"Substitution"(取代),N為"Nucleophilic"(親核),都取第一個大寫字母)。
飽和碳上的親核取代反應很多。例如,鹵代烷能分別與氫氧化鈉、醇鈉或酚鈉、
硫脲、
硫醇鈉、
羧酸鹽和氨或胺等發生親核取代反應,生成醇、醚、硫醇、硫醚、羧酸酯和胺等。醇可與氫鹵酸、鹵化磷或
氯化亞碸作用,生成
鹵代烴。鹵代烷被
氫化鋁鋰還原為
烷烴,也是負氫離子對反應物中
鹵素的取代。當試劑的親核原子為碳時,取代結果形成碳-碳鍵 ,從而得到碳鏈增長產物,如鹵代烷與氰化鈉、炔化鈉或
烯醇鹽的反應。在親核取代反應中,C—X鍵先斷裂,生成正碳離子再跟試劑反應,形成C—Y鍵,這種反應叫單分子親核反應,記作SN1。C—X鍵斷裂和C—Y鍵的形成同時發生的反應叫
雙分子親核取代反應,記作SN2。
 親電取代反應
親電取代反應由於反應物結構和反應條件的差異,SN有兩種機理,即單分子親核取代反應SN1和雙分子親核取代反應SN2。SN1的過程分為兩步:第一步,反應物發生鍵裂(電離),生成活性中間體正碳離子和
離去基團;第二步,正碳離子迅速與試劑結合成為產物。總的
反應速率只與反應物濃度成正比,而與試劑濃度無關。SN2為舊鍵斷裂和新鍵形成同時發生的協同過程。反應速率與反應物濃度和試劑濃度都成正比。能生成相對穩定的碳正離子和離去基團的反應物容易發生SN1,中心碳原子空間阻礙小的反應物容易發生SN2 。如果親核試劑呈鹼性,則親核取代反應常伴有
消除反應,兩者的比例取決於反應物結構、試劑性質和反應條件。低溫和鹼性弱對SN取代有利。
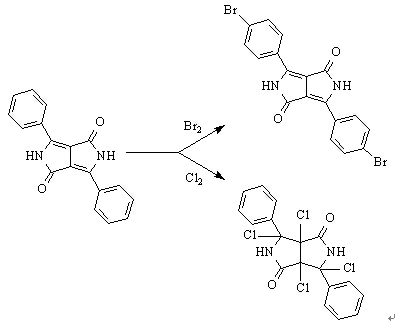 親核取代反應
親核取代反應鹵烴的親核取代反應主要有下面幾類:
水解。鹵烴加水生成醇的反應稱為水解反應。該反應是可逆的:
RX+HOH→ROH+HX .實際上,該反應一般沒有製備價值。多數鹵代烴都是由相應的醇來製備。不過,由於在某些複雜分子中導入一個羥基比引入一個鹵原子困難,所以有時也採用鹵烴水解的方法來合成相應的醇。在這種情況下,常常採用鹵烴與氫氧化鉀或氫氧化鈉的水溶液共熱來製取RX+NaOH→ROH+NaX .反應能進行完全,因為OH-比X-更具親核性,產生的鹵化氫又被鹼中和。如:乙醇與乙酸的酯化反應。
與氰化鈉反應。鹵烴在醇溶液中與氰化鉀或氰化鈉反應生成腈,有機合成中,常常需要增長碳鏈,鹵烴與氰化鉀(鈉)的反應是增長一個碳原子的方法之一。但氰化鉀(鈉)有劇毒,使用時須特別注意。 通過腈基(-CN)的轉變可合成羧酸(-COOH)及其
衍生物。
與醇鈉、氨、硝酸銀等的反應, 前兩個反應是製備醚類和胺類的方法之一。後一個反應往往用於鹵烴的鑑別(見後),但某些不活潑的鹵烴不與硝酸銀反應,如ArX,RCH=CHX,HCCl3,ArCOCHCl和ROCHCHCl等類型的鹵烴都無此反應。
與有機磷的反應。鹵烴與三烴基膦作用得到鏻鹽,後者在強鹼作用下失去質子得到
磷葉立德(ylide)或被稱作磷葉立因(ylene)。 RCHX+RPRPCHRX 其中:X為I、Br、Cl等;R為烷基或
芳基。 磷葉立德一般比較穩定,但有時也很活潑。以共振式表示有兩種極限式。
親電取代反應
親電取代反應主要發生在芳香體系或富電子的不飽和碳上,就本質而言均是較強親電基團對負電子體系進攻,取代較弱親電基團。其中有磺化反應,硝化反應,鹵代反應等等
均裂取代反應
簡稱SH(S為英文"Substitution"(取代))。為自由基對反應物分子中某原子的進攻,生成產物和一個新的自由基的反應。這種反應通常是自由基鏈式反應的鏈轉移步驟。一些有機物在空氣中會發生自動氧化,其過程也是均裂取代,如苯甲醛、異丙苯和四氫萘等與氧氣作用,可分別生成相應的有機過氧化物。
芳香取代反應
分芳族親電取代反應SEAr和芳族親核取代反應SNAr(S代表取代,N代表親核,Ar代表芳香)兩類,Ar表示芳基。芳烴通過
硝化、鹵化、磺化和烷基化或
醯基化反應,可分別在芳環上引進
硝基、
鹵原子、
磺酸基和
烷基或
醯基,這些都屬SEAr。芳環上已有取代基的化合物,取代劑對試劑的進攻有定位作用。
苯環上的取代基為給電子基團和鹵原子時,
親電試劑較多地進入其鄰位和對位;取代 基為吸電子基團時,則以得到間位產物為主。此外,除發生這些正常反應外,有時試劑還可以進攻原有取代基的位置並取而代之,這種情況稱為原位取代。
SNAr需要一定條件才能進行。如鹵代芳烴一般不易發生SNAr,但當鹵原子受到鄰或對位硝基的活化,則易被取代。鹵代芳烴在強鹼條件下也可發生取代。此外,芳香族重氮鹽由於離去基團斷裂成為穩定的分子氮,有利於生成苯基正離子,也能發生類似SNl的反應。
加成與取代反應區別
取代反應定義:有機分子中的一個原子或原子團被其他原子或原子團所代替的反應。類型比較:很多參考書經常把它與
置換反應做比較,而實際上它與
複分解反應更像。例子:以CH
4與Cl
2反應為例,原理是:一個H被一個Cl取代,即C—H鍵變為C—Cl鍵。剩下的Cl與被取代的H產生HCl。特點就是:一個H被取代,消耗一個Cl
2,產生一個HCl。
加成反應定義:有機物分子中不飽和碳原子與其他原子或原子團直接結合生成新物質的反應。類型比較:從物質種類上來看,類似於化合反應。例子:以CH2=CH2與Br2反應為例,原理是:C=C中的雙鍵斷開其中一個,兩個C各形成一個半鍵,分別與兩個Br結合。特點就是雙鍵變單鍵,不飽和變飽和。
 親電取代反應
親電取代反應 親核取代反應
親核取代反應
