羧酸與醇在酸催化下作用脫水或醇與醯基化試劑(醯氯、酸酐)作用均可用於酯的製備。
基本介紹
- 中文名:羧酸酯
- 化學式: CH3COOH
- 水溶性:不溶於水
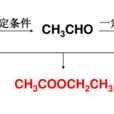
羧酸與醇在酸催化下作用脫水或醇與醯基化試劑(醯氯、酸酐)作用均可用於酯的製備。
羧酸與醇在酸催化下作用脫水或醇與醯基化試劑(醯氯、酸酐)作用均可用於酯的製備。...... 羧酸酯的沸點比相應的羧酸和醇都要低,而與含同數碳原子的醛、酮差不...
指含有羧酸酯結構的聚合物 用途 黏合劑和助劑使用這類高分子材料的種類比較多,其中以羧甲基纖維素為代表的改性天然聚合物在工業上主要作為黏合劑和助劑使用,以聚...
長鏈羧酸酯}nng chain car}nxy"}ic acid ester主要指十二個碳以上的梭酸聽形成的酚。屬i f'離子表面活性}rEl . }n硬脂酸丁酷、十四烷酸異丙酚、油酸內酚...
長鏈羧酸酯聚氧乙烯-18,簡稱LMEO-18,外觀是淡黃色粘稠液體,有效活性物含量75%左右;是一種新型非離子表面活性劑,具有低泡性能,優良的乳化、分散、潤濕、淨洗等...
甲基環戊烯羧酸酯是一種化學物質,分子式是C7H10O2。...... 甲基環戊烯羧酸酯是一種化學物質,分子式是C7H10O2。中文名 甲基環戊烯羧酸酯 英文名 1-Cyclopente...
苯基吖啶-9-羧酸酯(9-Acridinecarboxylic acid phenyl ester)分子式C20H13 N O2,分子量299.32...
乙二醇單烷基醚羧酸酯是一種化學物質,分子式是R,R2=R1-C-(OCH2CH20n-OR2。...... 乙二醇單烷基醚羧酸酯是一種化學物質,分子式是R,R2=R1-C-(OCH2CH20n-OR...
在酶化學中測定α-酯酶的底物。比色測定殺蟲劑降解羧酸酯酶。有機合成中間體。...... 在酶化學中測定α-酯酶的底物。比色測定殺蟲劑降解羧酸酯酶。有機合成中...
醋酸酯是醋酸酯類產品,廣泛套用於溶劑、增塑劑、表面活性劑及聚合物單體等領域...... 酯化生產相應的醋酸異丙酯、醋酸仲丁酯、醋酸異丁酯等其它醋酸酯以及其它羧酸酯...
二丁基錫硫代羧酸酯 ( C'.,H9 ) a5n i.' SC.'HZC'Chi2 )z dif}ulyltin thiocarEx}xylate }田狀化rt 物:折射率,神約1.50密度約 1.2斗啟In}l}...
乙基-4-甲基-2-環己酮-1-羧酸酯是一種化學物質,化學式是C10H16O3。...... 乙基-4-甲基-2-環己酮-1-羧酸酯是一種化學物質,化學式是C10H16O3。...
克萊森(酯)縮合反應是含有α-活潑氫的酯類在醇鈉、三苯甲基鈉等鹼性試劑的作用下,發生縮合反應形成β-酮酸酯類化合物,稱為克萊森(脂)縮合反應,反應可在不同...
含有α-活潑氫的酯類在醇鈉等鹼性縮合劑作用下縮合失去一分子醇得到β-酮酸酯類的反應,稱為Claisen縮合反應。如乙酸乙酯在乙醇鈉作用下縮合得到乙醯乙酸乙酯。...
本品為(+)羥甲基-(2S,5R,6R)-6-(R)-(2-氨基-2-苯乙醯氨基〕-3,3-二甲基-7-氧代-4-硫雜-1-氮雜雙環3.2.0正庚烷-2-羧酸酯,(2S,5R)-3,3-...
【中文名稱】滅掃利;α-氰基-3-苯氧基苄基-2,2,3,3-四甲基環丙烷羧酸酯;分撲菊酯 【英文名稱】fenpropathrin fenpropanate;Meothrin;Danitol 【分子式】C22H...
甲酸乙酯為允許使用的食用香料,又稱蟻酸乙酯,其化學結構上具有活潑羰基和酯基性質,有還原性,能進行酯縮合反應,能混溶於乙醇、乙醚、苯和丙二醇,微溶於礦物油和水...
有機酸是指一些具有酸性的有機化合物。最常見的有機酸是羧酸,其酸性源於羧基 (-COOH)。磺酸 (-SO3H)、亞磺酸(RSOOH)、硫羧酸(RCOSH)等也屬於有機酸。有機...
