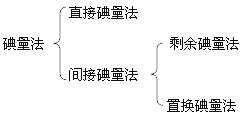
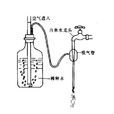
發現
1826年H·dela比拉迪埃用含有澱粉(指示劑)、氯化鈉和碳酸氫鈉的碘化物溶液為滴定劑,滴定次氯酸鈉溶液(漂白液),1840年有人以澱粉為指示劑,用碘的乙醇溶液為滴定劑,滴定硫化物溶液以後,碘量法套用日益廣泛。
定義
碘量法是
氧化還原滴定法中,套用比較廣泛的一種方法。這是因為對I
2-I
-的標準
電位既不高,也不低,碘可做為氧化劑而被中強的還原劑(如Sn
2+,H
2S)等所還原;碘離子也可做為還原劑而被中強的或強的氧化劑(如H
2SO
4,IO
3-,Cr
2O
72-,MnO
4-等)所氧化。
碘量法以碘作為氧化劑,或以碘化物(如碘化鉀)作為還原劑進行滴定的方法。
方法概要
I2 的 S 小:20 ℃為 1.33×10-3 mol/L
而I2 (水合) + I-=I3- (配位離子) K = 710
過量I-存在時半反應。
極微量的碘與多羥基化合物澱粉相遇,也能立即形成深藍色的配合物,碘的這一性質是使碘量法得到套用。
滴定原理
直接碘量法
直接碘量法是用碘滴定液直接滴定還原性物質的方法。在滴定過程中,I2被還原為I:
滴定條件:
弱酸(HAc ,pH =5 )
弱鹼(Na
2CO
3,pH =8)溶液中進行;如果溶液pH>9,可發生副反應使測定結果不準確。
強酸中: 4I
-+ O
2(空氣中) + 4H
+= 2I
2+ H
2O
強鹼中: 3I
2+ 6OH
-=IO
3-+ 5I
-+ 3H
2O
指示劑:1)澱粉,澱粉遇碘顯藍色,反應極為靈敏。化學計量點稍後,溶液中有過量的碘,碘與澱粉結合顯藍色而指示終點到達。2)碘自身的顏色指示終點,化學計量點後,溶液中稍過量的碘顯黃色而指示終點。
可滴定物:I
2 是較弱的氧化劑,凡是E0’( E0 ) < 的物質都可用
標準溶液直接滴定:
S2-、S2O32-、SO32-、As2O3、Vc等。
間接碘量法
1)剩餘碘量法
剩餘碘量法是在供試品(還原性物質)溶液中先加入定量、過量的碘滴定液,待I2與測定組分反應完全後,然後用硫代硫酸鈉滴定液滴定剩餘的碘,以求出待測組分含量的方法。滴定反應為:
I2(定量過量)+ 還原性物質→2I + I2(剩餘)
I2(剩餘)+ 2S2O32-→S4O62-+2I-
2)置換碘量法
置換碘量法是先在供試品(氧化性物質)溶液中加入碘化鉀,供試品將碘化鉀氧化析出定量的碘,碘再用硫代硫酸鈉滴定液滴定,從而可求出待測組分含量。滴定反應為:
氧化性物質 + 2I-→I2
I2+ 2S2O32-→S4O62-+ 2I-
間接碘量法:
指示劑:澱粉,澱粉指示劑應在近終點時加入,因為當溶液中有大量碘存在時,碘易吸附在澱粉表面,影響終點的正確判斷。
滴定條件:在一定條件下,用I-還原氧化性物質,然後用 Na
2S
2O
3標準溶液滴定析出的碘。(此法也可用來測定
還原性物質和能與 CrO
42- 定量生成沉澱的離子)
①酸度的影響—— I2 與Na2S2O3應在中性、弱酸性溶液中進行反應。
若在鹼性溶液中:S2O32-+ 4I2 + 10 OH-= 2SO42-+ 8I- + 5H2O
3I2 + 6OH-=IO3-+ 5I- + 3H2O
若在酸性溶液中:S2O32-+ 2H+= 2SO2 + Sˉ+ H2O
4I- + O2 (空氣中) + 4H+= 2I2 + H2O
②防止 I2 揮發
i ) 加入過量KI(比理論值大2~3倍)與 I2 生成I3-,減少 I2揮發;
ii ) 室溫下進行;
iii) 滴定時不要劇烈搖動。
③防止I- 被氧化
ii) 析出 I2後不要放置過久(一般暗處5 ~ 7min );
iii) 滴定速度適當快。
可滴定物:I-是中等強度的
還原劑。主要用來測定:E0’( E0 ) <的氧化態物質:
CrO42-、Cr2O72-、H2O2、 KMnO4、IO3-、Cu2+、NO3-、NO2-
例:Cr2O72-+ 6I-+14H++6e-= 2Cr3++3I2+7H2O
I2+ 2 S2O32-= 2 I-+ S4O62-
影響因素
(1)適用 pH 2 ~ 9:澱粉指示劑在弱酸介質中最靈敏,pH>9時,I2易發生歧化反應,生成IO、IO3, 而IO、IO3不與澱粉發生顯色反應,當pH<2時,澱粉易水解成糊精,糊精遇I2顯紅色,該顯色反應可逆性差。
(2)使用直鏈澱粉:直鏈澱粉必須有碘一價負離子的存在,才能遇碘變藍色;支鏈澱粉遇碘顯紫色,且顏色變化不敏銳。
(3)50%乙醇存在時不變色:醇類的存在降低指示劑的靈敏度,在50%以上的乙醇中,澱粉甚至不與碘發生
顯色反應。
(4)隨著溫度的升高,澱粉指示劑變色的靈敏度降低。
(5)大量電解質存在的情況下,也會使其靈敏度降低甚至失效。
(6) 澱粉指示劑最好在用前配製,不宜久存,若在澱粉指示劑中加入少量碘化汞或氯化鋅,甘油、甲醯胺等防腐劑,可延長貯存時間。配製時將澱粉混懸液煮至半透明,且加熱時間不宜過長,並應迅速冷卻至室溫。
套用
碘量法測廢水中硫化物
碘量法測水果蔬菜中維生素C的含量
碘量法測定水中溶解氧
碘量法測定過氧化氫
碘量法測金品位
碘量法測啤酒中、醛糖、總二氧化硫、甲醛含量
碘量法測定消毒劑中二氧化氯
......
用碘量法測定物質的量,在環境、醫藥、食品、化工、冶金、石油等領域都有廣泛的套用。