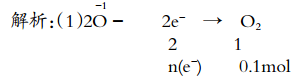舉例
例如
丹尼爾電池,即銅和鋅分別為正極和負極的電池,它的兩個半反應式分別為:
正極: Cu2++2e- = Cu
負極: Zn - 2e- = Zn2+
總反應:Cu2+ + Zn = Cu + Zn2+
再如:把一個氧化還原反應拆寫成兩個"半反應式"
如:2Fe3+ + Cu=2Fe2+ + Cu2+,可分成
氧化反應:Cu - 2e-= Cu2+,還原反應:2Fe3+ + 2e-=2Fe2+
同樣:3NO2 + H2O=2H+ + 2NO3- + NO
氧化反應:
2NO2 - 2e- + 2H2O= 4H+ + 2NO3-
還原反應:
NO2 + 2e- + 2H+ = H2O + NO
書寫方法
1、找對應關係
在氧化還原反應中,按氧化劑對應還原產物,還原劑對應氧化產物的對應關係找到確切兩個物質(或微粒)這個步驟是半反應書寫的關鍵步驟。
2、半反應通式
半反應之還原反應(正極或陰極上電極反應):氧化劑 +xe-→還原產物。
半反應之氧化反應(負極或陽極上電極反應):還原劑 -xe-→氧化產物。
其中“+”表示得電子,“-”表示失電子。“ → ”表 示 變 化 ,不 能 寫 成“ = ”,因 為 它 只表示被氧化(或被還原)元素前後變化, 且前後原子個數相等,其它元素原子個數不一定相等。
3、配平半反應
半反應的配平首先是配平化合價變化的元素微粒個數。
例如,在Cr2O72-+xe-→Cr3+ 中,需在後面的Cr3+ 前配係數2,
使得鉻前後個數相等。其次,計算x 的值。x 可以通過某元素 微粒個數乘以該元素微粒前後化合價之差絕對值來計算。
配平氧化還原反應
採用半反應式法配平
氧化還原反應方程式時,首先要知道反應物和生成物並遵循下列配平原則:
一是電荷守恆:反應中氧化劑所得到的電子數必須等於還原劑所失去的電子數;
二是質量守恆:根據質量守恆定律,方程式兩邊各種元素的原子總數必須各自相等,各物種的電荷數的代數和必須相等;
配平的主要步驟主要是:
(1)以離子式寫出主要的反應物及氧化還原產物;
(2)分別寫出氧化劑被還原和還原劑被氧化的半反應;
(3)分別配平兩個半反應方程式,使每個半反應方程式等號兩邊的各種元素的原子總數各自相等且電荷數相等;
(4)確定兩個半反應方程式得、失電子數目的最低公倍數。將兩個半反應方程式各項分別乘以相應的係數,使其得、失電子書目相同。然後,將二者合併,就得到了配平的氧化還原反應的離子方程式。
例如,用半反應法配平下列反應:
反應中氯元素化合價升高,分析可知水中的氫元素 化合價應該降低,確定未知物質是H2。按得失電子相等要求,半反應為NaCl-6e-→NaClO3 和3H2O+6e-→3H2。
把上述兩個半反應中物質係數配到方程式中,故有1 NaCl+ 3 H2O→1NaClO3+ 3H2。
計算電子轉移數目
利用半反應法計算電子的轉移數目,其優點是不需 要寫出複雜的反應方程式,只需寫出其中的一個半反應,計算 得(或失)電子數就是
電子轉移的數目。
例如,在過氧化鈉與水的反應中,每生成0.1mol 氧氣,計算轉移電子的數目:
所以,n(e-)=0.2mol,轉移電子數目為0.2NA。
計算元素化合價
例如:2.00×10-4mol 重鉻酸鉀(K2Cr2O7),用去 0.100molL的硫酸亞鐵銨溶液12ml 剛好反應,
則產物中元素鉻的化合價是:
解析:12ml0.100mol/L 的硫酸亞鐵銨溶液,可知Fe2+ 物質的量為1.20×10-3mol。
所以,n(e-)失=1.20×10-3mol,因而n(e-)得=n(e-)失=1.20×10-3mol
令產物中鉻元素化合價為χ則有:
解得χ=3,產物中元素鉻的化合價是+3價。
計算氧化劑或還原劑物理量
例如:在一定條件下,PbO2 與 Cr3+ 反應產物是Cr2O72- 和Pb2+,如果消耗1molCr3+,則應消耗PbO2為多少?
解析:
所以,n(e-)失=3mol,故n(e-)得=n(e-)失=3mo
所以n(PbO2)=1.5mol
測定原電池電動勢
在電化學的實際套用中,半電池(及電對)的標準電極電勢可以通過實驗測得。使待測半電池中各物種均處於標準狀態下將其與標準氫電極連線組成原電池,以電壓表測定該電池的電動勢並確定其正極和負極,進而可推算出待測半電池的標準電極電勢。根據原電池的兩個半反應方程式,計算出原電池電勢的大小。
舉例說明:
金屬鋅置換稀硫酸中的氫,發生氧化還原反應:Zn +2H+ = Zn2+ +H2
對應的兩個“半反應”分別是:
負極,氧化反應 Zn - 2e- = Zn2+
正極,還原反應 2H+ +2e- =H2
分別將兩個兩個半電池與標準氫電極連線組成原電池,測定出半電池的電極電勢,從而得到鋅-稀硫酸原電池的電動勢。