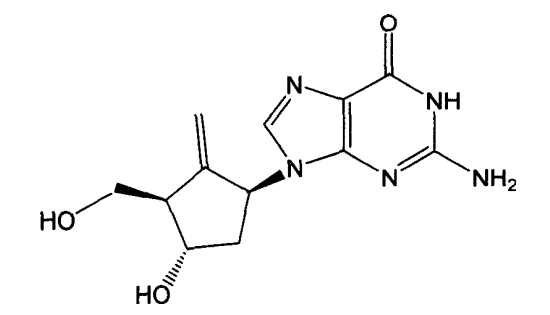
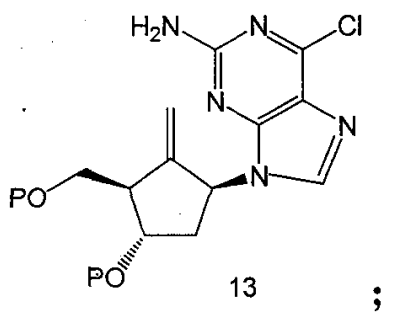
專利背景 恩替卡韋 (entecavir)是一種碳環鳥嘌呤核苷類似物,化學名:[1S-(1α,3α,4β)]-2-氨基-1,9-二氫-9-[4-羥基-3-羥甲基-2-亞甲環戊基]-6H-嘌啉-6-酮;分子式:C
12 H
15 O
3 N
5 ,分子量277.3;化學結構式如下:
恩替卡韋作為一種有效的抗B型肝炎病毒的治療藥物,該化合物及其一水合物和鈉鹽都可以用於B型肝炎的治療,關於恩替卡韋及其作為抗病毒藥物用途的報導首見於美國專利US5206244;CN1310999和CN1658844描述了恩替卡韋低劑量藥物組合物用於治療B型肝炎病毒感染。JOC1985,50,755、CN1061972、WO9809964、CN1747959等描述了其製備方法,其核心是先合成環氧化環戊烷化合物,然後用鳥嘌呤衍生物直接來打開氧環來合成碳環核苷,該反應路線有以下缺點:
1.開環反應產率低:例如WO9809964報導的產率在50%左右,JOC1985,50,755報導的產率為27%。
2.開環反應產物分離提純困難需要使用多次柱層析,開環反應產物為立體異構體混合,即使經過多次矽膠柱層析提純之後,相互之間仍然很難分離,並影響最終產物的純度。例如WO9809964報導開環反應產物需要多次矽膠柱層析後才能得到純度為92%的產物。
3.鳥嘌呤上的氨基在後續反應中需要保護,保護反應困難,產物不穩定,分離繁雜並需要使用柱層析例如WO9809964報導鳥嘌呤上的氨基用MMT保護的反應很難完成,產物在後續提純的過程中需要用矽膠柱層析,並且在矽膠柱很容易分解。
4.CN1747959中的方法使用了矽烷作為羥基的前體,在完成了目標分子的基本結構的合成之後,需要使用非常強烈的氧化條件和強酸強鹼條件來將矽烷基團轉化為羥基,影響了目標產物的純度和產率,並且需要用特殊的樹脂層析方法來提純目標產物。
因此,直接使用鳥嘌呤開環的反應路線在實際使用的過程中工藝複雜收率低成本高不適合於工業化生產。
發明內容 專利目的 《抗病毒核苷類似物的合成方法》的目的在於提供恩替卡韋的合成方法,該方法有利於重複和規模化的工業生產並以低的成本獲得適於藥用的產品。
《抗病毒核苷類似物的合成方法》的另一個目的在於提供用於合成恩替卡韋的中間體,以及這些中間體的合成方法。
技術方案 《抗病毒核苷類似物的合成方法》提供的新的合成方法包括:
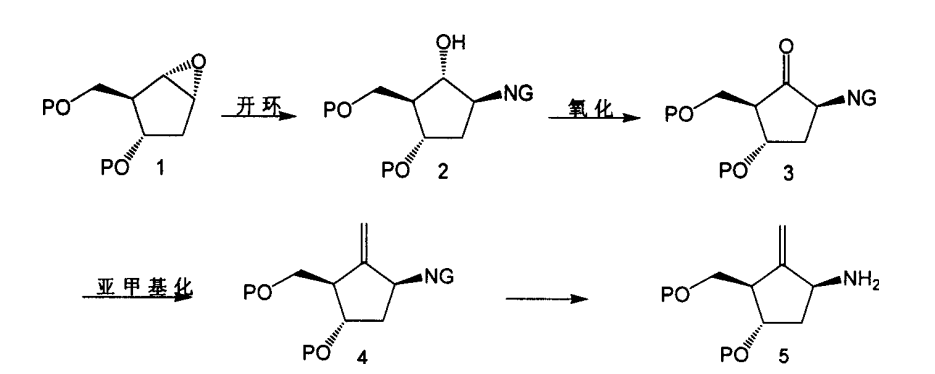
路線1:
1.首先是將化合物1與含氮的親核試劑反應,含氮的親核試劑將化合物1中的環氧環打開,得1位羥基的化合物2。其中P為羥基的保護基團,NG為含氮的親核試劑反應後剩下的殘基,可選用的含氮的親核試劑包括疊氮酸鹽,氨,鄰苯二甲醯亞胺及其鹽和有機胺例如苯甲胺或烯丙胺。反應可以在鹼性條件,酸性條件或中性條件下進行,例如鄰苯二甲醯亞胺及其鹽與環氧環在鹼性條件下進行,有機胺例如苯甲胺和烯丙胺與環氧環的反應可以在路易絲酸存在的條件下進行,而疊氮酸鹽可以在近中性的條件下進行開環反應;反應使用的溶劑根據親核試劑的不同選用極性非質子溶劑或質子溶劑及水,鄰苯二甲醯亞胺的開環反應一般在極性非質子溶劑如DMF或DMSO中進行,而疊氮酸鹽的反應一般在醇、水或醇水混合溶液中進行;反應溫度一般在室溫到180℃。
2.氧化化合物2中的羥基可以得到化合物3。氧化劑可選用
鉻酸 、
高錳酸鉀 、
溴酸鈉 、DMSO/DCC、DMSO/SOCL
2 、DMSO/TFA、DESS-MARTIN試劑等等,優選PCC、PDC、DESS-MARTIN試劑更優選DESS-MARTIN試劑。氧化反應的條件可按公知的氧化反應的條件進行。
3.化合物3通過
亞甲基化反應 將分子中的羰基轉化為環外的碳-碳雙鍵,從而得到化合物4。亞甲基化反應通常使用NYSTED試劑或TOBBE試劑等亞甲基化試劑,以四氯化鈦為催化劑,在-78℃至室溫的溫度範圍內進行。
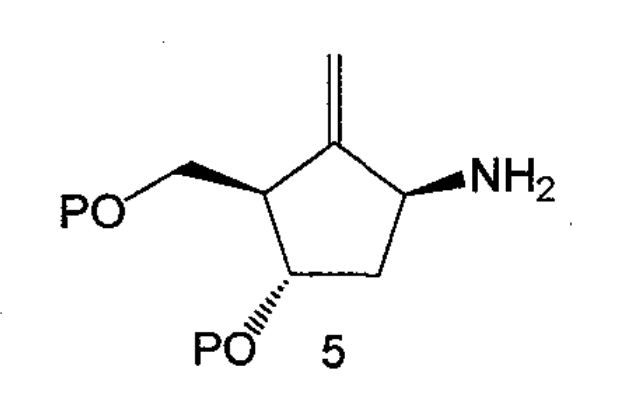
4.將化合物4中的含氮官能團NG轉化為氨基得到化合物5。例如,疊氮基可以通過還原變成氨基,鄰苯二甲醯亞胺基可以用肼,苯肼或有機胺如正丁胺,乙二胺等脫去鄰苯二甲醯基得到氨基,烯丙胺基可以用鈀催化劑脫保護得到氨基。
化合物1的製備方法可以參考J.CHEM.SOC.PERKIN.TRANS.1;549(1988)。首先將環戊二烯鈉與苄基氯甲基醚反應縮合,然後經過不對稱的硼氫化氧化反應,環氧化反應和最後保護羥基而得到。
該文所述的羥基的保護基團可選用任意的不受後續反應影響的保護基團。合適的保護基團可以參考GREENE所著的protective groups in organic synthesis,例如苄基、三苯甲基、三烷基矽、苯甲醯基等,優選苄基。羥基由苄基保護的化合物1的詳細製備方法可以參考美國專利US5206244。
路線2:(上述路線1的特例)
1.化合物1’與鄰苯二甲醯亞胺或其鹽在非質子極性溶劑中反應開環得到化合物2’。其中Bn為苄基,反應一般用DMF作溶劑,反應溫度在室溫到150℃之間,用氫化鈉或氫化鋰做催化劑,優選使用鄰苯二甲醯亞胺或其鉀鹽或鋰鹽來反應。
2.氧化化合物2’中的羥基可以得到化合物3’。氧化劑可採用鉻酸製劑、高錳酸鉀、溴酸鈉、DMSO/DCC、DMSO/SOCL2 、DMSO/TFA、DESS-MARTIN試劑等等。在這些試劑中PCC、PDC、DESS-MARTIN試劑,尤其是DESS-MARTIN試劑的反應條件溫和,轉化率高,容易處理。化合物3’可不進行純化而直接用於下一步反應。
3.化合物3’通過亞甲基化反應將分子中含有的羰基轉化為環外的碳-碳雙鍵,從而得到化合物4’。亞甲基化反應通常使用NYSTED試劑或TOBBE試劑等亞甲基化試劑,以四氯化鈦為催化劑,在-78℃至室溫的溫度範圍內進行。
4.將化合物4’中的鄰苯二甲醯亞胺基用肼,苯肼或有機胺如正丁胺,乙二胺等脫去鄰苯二甲醯基得到化合物5’。
路線3:
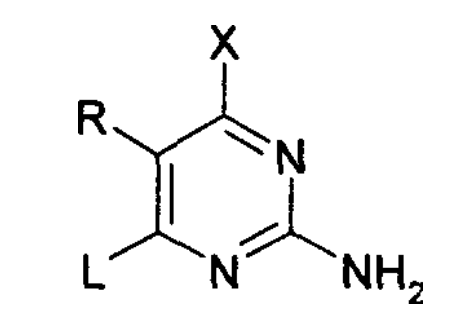
其中,L是任意的離去基團,通常為氯,溴或碘;R是氨基或者是可以轉化為氨基的基團,例如保護了的氨基,硝基,亞硝基,重氮基等,R還可以是氫,氫可以和重氮鹽發生反應變成重氮基,然後再被還原成氨基;X是羥基或任意的可以轉化成羥基的基團,例如鹵素和保護了的羥基。保護了的氨基可以是BOC、Fmoc、CBZ保護的氨基,醯基(鄰苯二甲醯基、苯甲醯基、乙醯基、三氟乙醯基等)保護的氨基,還有烷基保護的氨基,例如苯甲胺基、二苯甲胺基、烯丙基胺基等。保護了的羥基可以是醯基(苯甲醯基、乙醯基)保護的,還有烷基保護的,例如苯甲氧基、甲氧基等。
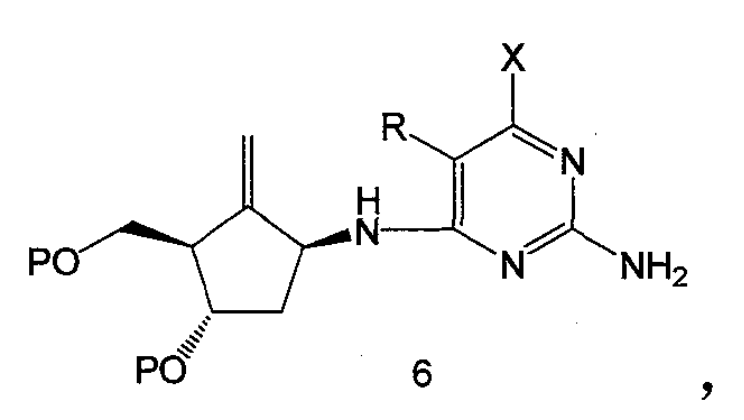
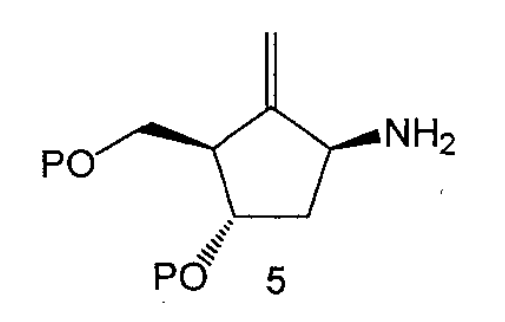
1.將亞甲基環戊烷化合物5與6位帶有離去基團的嘧啶衍生物偶聯,亞甲基環戊烷化合物5上的氨基連線到嘧啶環的6位上得到化合物6,其中P為羥基保護基團;
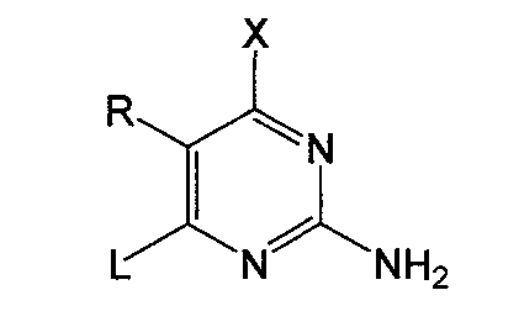
6位帶有離去基團的嘧啶衍生物結構如下式所示:
化合物5與嘧啶衍生物的偶聯反應通常在醇類和DMF等極性溶劑中和縛酸劑存在下進行,縛酸劑一般為有機胺,反應溫度通常在室溫至180℃之間,如果L為氯或溴,還可以使用碘化亞銅作為催化劑加速反應;
2.將嘧啶環上的R轉化為氨基可以得到化合物7,根據R基團的性質,具體的轉化方式各有不同;如果R為保護的氨基,則需要將保護基脫去;如果R為硝基,亞硝基,重氮基,則可以用還原的方法得到氨基;如果R為H,則需要先將R變成重氮基,然後再被還原成氨基;
3.將化合物7在原甲酸三烷基酯中用強酸催化進行關環反應可以得到嘌呤化合物8;
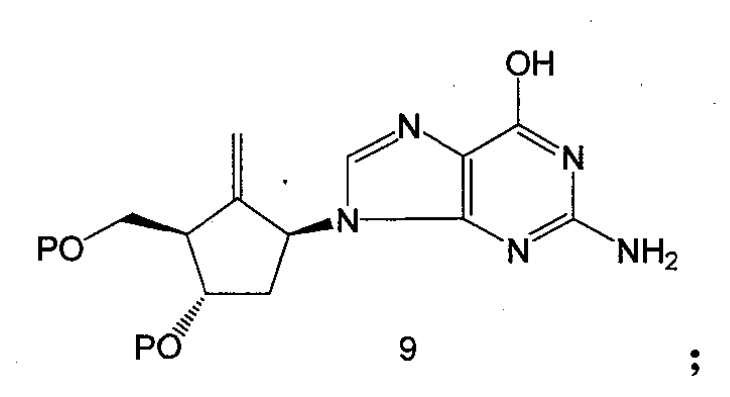
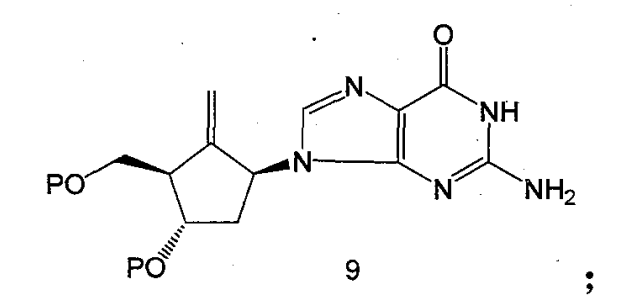
4.將嘌呤化合物8上的X轉化為羥基得到化合物9;
5.脫去化合物9上所有的保護基團後得到最終產物恩替卡韋。可以用三氯化硼脫去苄基,用三甲基碘矽烷脫去甲基,用鹽酸脫去三苯甲基,用鹼脫去苯甲醯基和乙醯基,用四丁基氟化銨脫去矽烷保護基。
路線4:(路線3的特例)
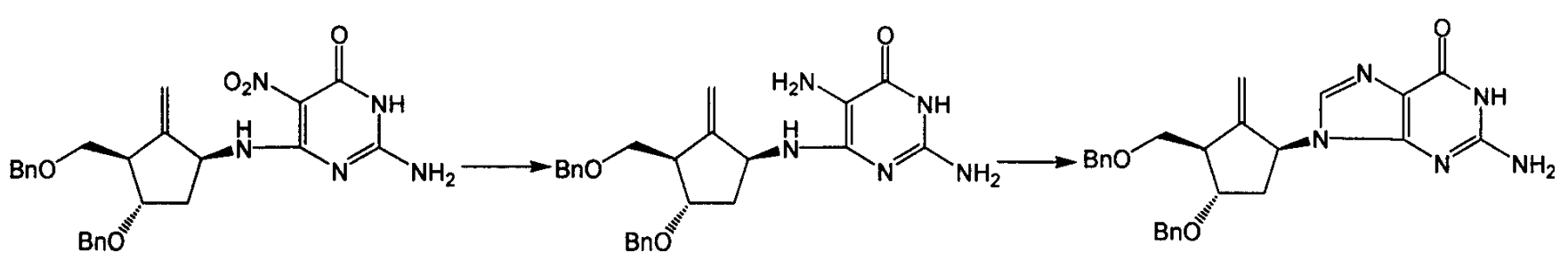
1.化合物5與2-氨基-5-硝基-3-羥基-6-氯嘧啶在極性溶劑中反應得到化合物10,優選的極性溶劑是乙醇、正丁醇和DMF,並用有機胺做縛酸劑,優選的縛酸劑是二異丙基乙胺和三乙氨,反套用氮氣保護並在回流溫度下進行,其中P為羥基保護基團;
2.化合物10中的硝基經過還原後得到二氨基嘧啶中間體化合物11,通常的還原硝基成氨基的方法都可以容易地將化合物10轉變為11,如SnCl2 /HCl,NaBH4 /CoCl2 ,Fe/HCl和連二硫酸鈉,優選連二硫酸鈉。
3.化合物11一般不需要分離提純就可以在原甲酸三烷基酯中在強酸的催化下發生關環反應生成化合物9,原甲酸三烷基酯優選原甲酸三甲酯和原甲酸三乙酯,強酸通常選用濃鹽酸,反應溫度通常在室溫和100℃之間。
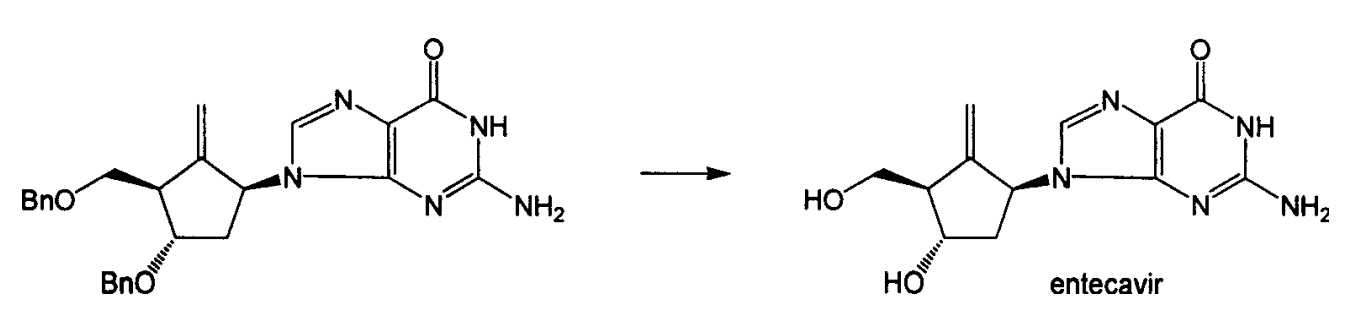
4.化合物9脫去保護基後即得到恩替卡韋。
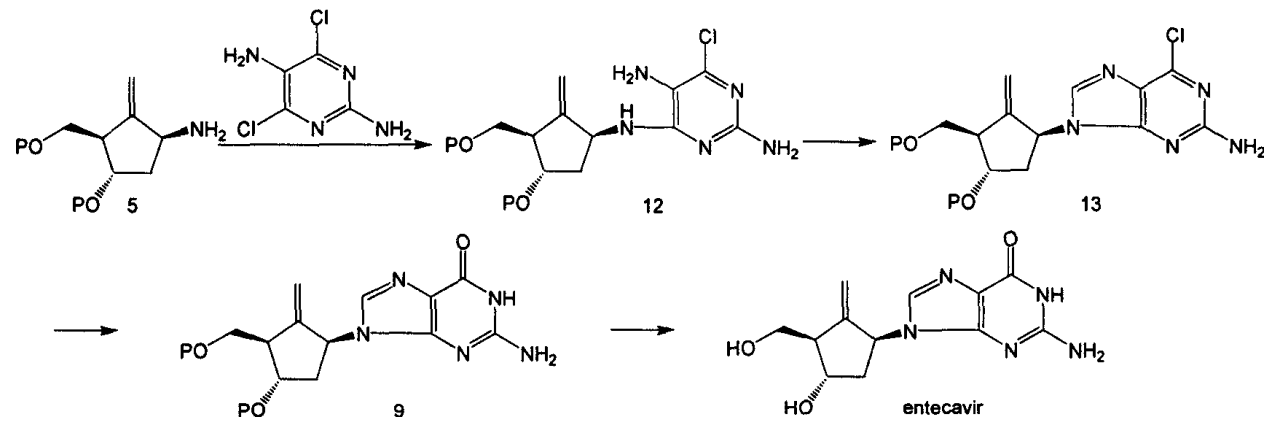
路線5:(路線3的特例)
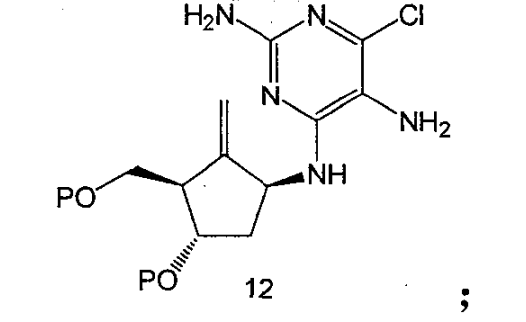
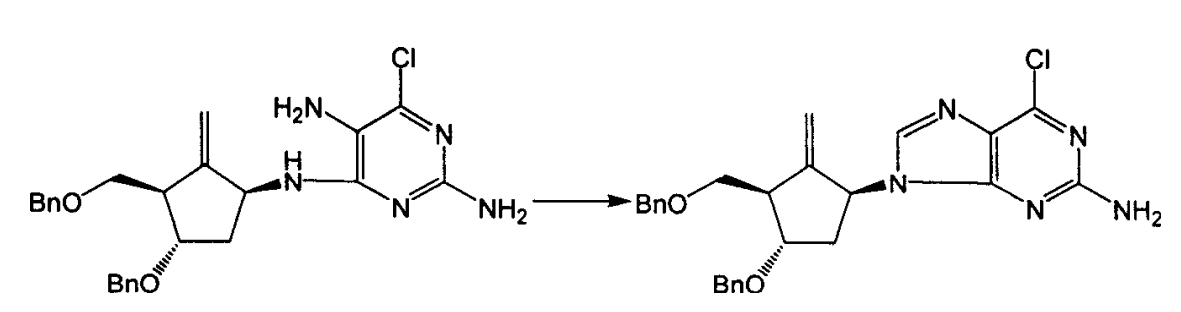
1.化合物5與2,5-二氨基-4,6-二氯嘧啶在極性溶劑中反應得到化合物12,優選的溶劑是乙醇、正丁醇和DMF,並用有機胺做縛酸劑,優選的縛酸劑是二異丙基乙胺和三乙氨,反套用氮氣保護並在溶劑的回流溫度下進行。
2.化合物12在原甲酸三烷基酯中在強酸的催化下發生關環反應生成化合物13,原甲酸三烷基酯優選原甲酸三甲酯和原甲酸三乙酯,強酸通常選用濃鹽酸,反應溫度通常在室溫和100℃之間。
3.化合物13在含有強鹼的水性溶液中進行水解,得到化合物9,水性溶液通常為水和醇類化合物的混合溶液,強鹼一般選用氫氧化鈉或氫氧化鉀,反應溫度為室溫至100℃。
4.化合物9脫去保護基後即得到恩替卡韋。
路線6:(路線3的特例)
1.化合物5與2-氨基-4,6-二氯嘧啶在極性溶劑中反應得到化合物14,優選的極性溶劑是乙醇、正丁醇和DMF,並用有機胺做縛酸劑,優選的縛酸劑是二異丙基乙胺或三乙氨,反套用氮氣保護並在回流溫度下進行,其中P為羥基保護基團;
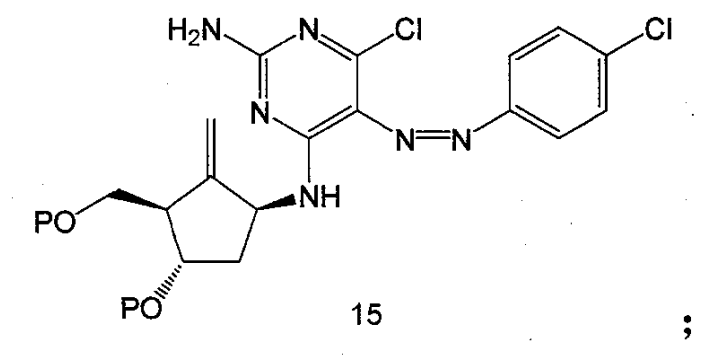
2.化合物14與對氯苯重氮鹽反應得到化合物15,反應在含水的醇類溶液中進行,反應溫度一般控制在室溫以下;
3.化合物15經過還原得到化合物12。還原劑一般選用NaBH4 /THF,Zn/HCl和Sn/HCl,反應溶劑通常用有機醇類;
4.化合物12在原甲酸三烷基酯中在強酸的催化下發生關環反應生成化合物13,原甲酸三烷基酯優選原甲酸三甲酯和原甲酸三乙酯,強酸通常選用濃鹽酸,反應溫度通常在室溫和100℃之間;
5.化合物13在含有強鹼的水性溶液中進行水解,得到化合物9,水性溶液通常為水和醇類化合物的混合溶液,強鹼一般選用氫氧化鈉或氫氧化鉀,反應溫度不超過100℃;
6.化合物9脫去保護基後即得到恩替卡韋。
改善效果 《抗病毒核苷類似物的合成方法》所提供的方法的優點:
1.由於避免了用鳥嘌呤開環,反應產率大大提高,化合物4或4’的分離提純方法簡單。
2.用鳥嘌呤直接開環時鳥嘌呤環上有9-N和7-N兩個位置可以發生親核進攻。雖然9-N的反應選擇性大於7-N,但不能完全排除7-N的反應產物,而用新的合成路線,由於原來的氨基最終只不過能轉化成9-N,所以不存在選擇性問題。
3.化合物4或4’的立體異構體可以很容易地與化合物4或4’分離,因此在最終產物中不會帶入非對映異構體。
4.由於新路線是在形成亞甲基之後再合成鳥嘌呤,所以避免了鳥嘌呤上2-氨基的保護和脫保護,簡化了合成路線。
5.反應得到的最終產物純度較高,避免了繁瑣的樹脂色譜分離。
技術領域 《抗病毒核苷類似物的合成方法》涉及核苷類似物的合成方法,具體涉及到具有抗病毒活性的化合物恩替卡韋的合成方法,本發明還涉及用於製備恩替卡韋的中間體以及製備這些中間體的方法。
權利要求 1.結構式如下的恩替卡韋的製備方法,
包括:
a.將亞甲基環戊烷化合物5
與6位帶有離去基團的嘧啶衍生物偶聯,
得到化合物6
其中P為羥基保護基團;L是任意的離去基團;R是氨基或可以轉化為氨基的基團;X是羥基或任意的可以轉化成羥基的基團,偶聯反應在極性溶劑中,並在縛酸劑存在的情況下反應,反應溫度在室溫至180℃之間;
b.除了R為氨基的情況,將化合物6的嘧啶環上的R轉化為氨基得到化合物7
c.將化合物7在原甲酸三烷基酯中用強酸催化進行關環反應得到嘌呤化合物8
d.除了X為羥基的情況,將嘌呤化合物8上的X轉化為羥基得到化合物9
e.脫去化合物9上的保護基團後得到恩替卡韋。
2.權利要求1所述的恩替卡韋的製備方法,其中P是苄基、三苯甲基、三烷基矽、苯甲醯基。
3.權利要求1所述的恩替卡韋的製備方法,其中L是氯、溴或碘。
4.權利要求1所述的恩替卡韋的製備方法,其中R是氨基,保護了的氨基,硝基,亞硝基,重氮基或氫。
5.權利要求1所述的恩替卡韋的製備方法,其中X是羥基、鹵素或保護了的羥基。
6.權利要求1所述的恩替卡韋的製備方法,包括:
a.將亞甲基環戊烷化合物5
與2-氨基-5-硝基-4-羥基-6-氯嘧啶在極性溶劑中,並在縛酸劑存在的情況下反應,得到化合物10
其中P為羥基保護基團;
b.將化合物10中的硝基還原後得到二氨基嘧啶化合物11
c.將化合物11在原甲酸三烷基酯中在強酸的催化下,發生關環反應生成化合物9
d.化合物9脫去保護基後即得到恩替卡韋。
7.權利要求6所述的恩替卡韋的製備方法,其中步驟b中所述的還原劑是SnCl2 /HCl、NaBH4 /CoCl2 、Fe/HCl或連二硫酸鈉。
8.權利要求7所述的恩替卡韋的製備方法,其中步驟b中所述的還原劑是連二硫酸鈉。
9.權利要求1所述的恩替卡韋的製備方法,包括:
a.將亞甲基環戊烷化合物5
與2,5-二氨基-4,6-二氯嘧啶在極性溶劑中,並在縛酸劑存在的情況下反應,得到化合物12
其中P為羥基保護基團;
b.化合物12在原甲酸三烷基酯中在強酸的催化下,發生關環反應生成化合物13
c.化合物13在含有強鹼的水性溶液中進行水解,得到化合物9
d.化合物9脫去保護基後即得到恩替卡韋。
10.權利要求1所述的恩替卡韋的製備方法,包括:
a.亞甲基環戊烷化合物5
與2-氨基-4,6-二氯嘧啶在極性溶劑中,在縛酸劑存在的情況下反應,得到化合物14
其中P為羥基保護基團;
b.化合物14與對氯苯重氮鹽,在含水的醇類溶液中,在室溫以下反應得到化合物15
c.用還原劑還原化合物15得到化合物12
d.化合物12在原甲酸三烷基酯中在強酸的催化下,發生關環反應生成化合物13
e.化合物13在含有強鹼的水性溶液中進行水解,得到化合物9
f.化合物9脫去保護基後即得到恩替卡韋。
11.權利要求1、6、9或10所述的恩替卡韋的製備方法,其中亞甲基環戊烷化合物5中的P為苄基。
12.權利要求6、9或10所述的恩替卡韋的製備方法,其中步驟a中所述極性溶劑是乙醇、正丁醇或DMF,縛酸劑是二異丙基乙胺或三乙胺,反套用氮氣保護並在回流溫度下進行。
13.權利要求6、9或10所述的恩替卡韋的製備方法,其中所述的原甲酸三烷基酯是原甲酸三甲酯或原甲酸三乙酯,強酸為濃鹽酸,反應在室溫至100℃之間。
14.權利要求9或10所述的恩替卡韋的製備方法,其中所述的水性溶液是水和醇類的混合溶液,強鹼是氫氧化鈉或氫氧化鉀,反應在室溫至100℃之間。
15.權利要求10所述的恩替卡韋的製備方法,其中步驟c中所述的還原劑是NaBH4 /THF,Zn/HCl或Sn/HCl,反應溶劑是有機醇類。
實施方式 實施例1
[1s-(1α,2β,3α,5β)]-5-(鄰苯二甲醯亞胺基)-3-(苯甲氧基)-2-[(苯甲氧基)甲基]環戊醇(中間體2’)的製備
在5升三口燒瓶中,加入145(0.98摩爾)鄰苯二甲醯亞胺、3.77克LiH和765毫升無水DMF,攪拌10分鐘。加熱至60℃後再攪拌15分鐘,此時渾濁液變澄清。緩慢滴加以1.87升無水DMF溶解的152克(0.49摩爾)[1s-(1α,2α,3β,5α)]-3-(苯甲氧基)-2-[(苯甲氧基)甲基]-6-氧雜二環[3.1.0]己烷(中間體1’),於60℃攪拌15分鐘。加熱至125℃,反應2小時,TLC(乙:正=1:3)顯示原料消失,以28毫升冰醋酸終止反應。攪拌10分鐘。加入2.5升飽和食鹽水,以乙酸乙酯3×1.2升萃取,有機相合併以飽和食鹽水洗滌一次,無水硫酸鈉乾燥,回收溶劑。剩餘油狀物矽膠柱分離,以8%的乙酸乙酯/石油醚和10%乙酸乙酯/石油醚洗脫,得到137.7克(0.3摩爾)無色油狀物,收率:61.5%。
測:[α]D =+34.8°(C=1.0,CHCl3 )
HNMR:δ7.71~7.82(4H,m),δ7.26~7.32(10H,m),δ4.72~4.75(1H,m),δ4.51~4.53(4H,m),δ4.43~4.46(1H,m),δ3.7~4.0(2H,m),δ3.64~3.66(1H,m),δ2.48(1H,m),δ2.35(1H,m),δ2.16(2H,m)
MS(API-ES)(M+Na)=480,
實施例2
[1s-(1α,2β,3α,5β)]-5-[鄰苯二甲醯亞胺基]-3-(苯甲氧基)-2-[(苯甲氧基)甲基]環戊酮(中間體3’)的製備
在3升三口燒瓶中,加入Dess-Martin試劑203克,加入1.4升無水CH2 Cl2 攪拌。將137.7克中間體2’以890毫升無水CH2 Cl2 溶解,滴加至上步懸濁液中,20分鐘後TLC(乙:正=1:3)顯示原料消失,停止反應。先以NaHSO3 飽和水溶液洗3次,再以NaHCO3 飽和水溶液洗3次,最後以飽和鹽水洗3次,有機層除水抽乾,得到196克黃色油狀化合物。
實施例3
1s-(1α,3α,4β)-5-鄰苯二甲醯亞胺基-2-亞甲基-4-(苯甲氧基)-3-[(苯甲氧基)甲基]環戊烷(中間體4’)的製備
在5升三口燒瓶中,加入Nysted Reagent(Wt=20%)1.46升和800毫升無水THF,攪拌,N2 保護,冷卻至-78℃。將196克中間體3’以適量CH2 Cl2 溶解,滴加至反應中。取TiCl4 /CH2 Cl2 (1:9)393毫升緩慢滴加至反應中,維持溫度在-60℃~-78℃。滴加完畢,混合物在-78℃下維持反應15分鐘。緩慢升溫至室溫,繼續攪拌1~3小時,TLC(乙:正=1:4)顯示原料消失,反應溶液呈紫黑色。將此反應溶液倒入至2.3升飽和NaHCO3 中,充分攪拌,此時會出現白色渾濁物。以乙酸乙酯萃取3次,飽和食鹽水反萃取一次,無水硫酸鈉除水,回收溶劑得到深紫色油狀物。再用油泵抽乾,得到188g淺黃色油狀化合物。
H NMR:δ7.32~7.83(4H,m),δ7.26~7.34(10H,m),δ5.43(1H,m),δ4.85(1H,s),5.11(1H,s),δ4.56~4.59(4H,m),δ4.2(1H,m),δ3.64~3.72(2H,m),δ3.12(1H,m),δ2.17~2.56(2H,m)
MS(API-ES)(M+Na)=476,(M+H)=454
實施例4
1s-(1α,3α,4β)-5-胺基-2-亞甲基-4-(苯甲氧基)-3-[(苯甲氧基)甲基]環戊烷(中間體5’)的製備
在2升三口燒瓶中,加入188克中間體4’和930毫升正丁醇,攪拌溶解。加入93毫升乙二胺,加熱至90℃回流1小時,TLC(乙:正=1:3)顯示原料消失,用377毫升水洗,減壓回收溶劑,層析分離得到78.6克(0.24摩爾)油狀物,三步總收率:80.0%。測:[α]D =+13.0°(C=1.0,CHCl3 )
H NMR:δ7.27~7.31(10H,m),δ5.06(1H,s),δ5.18(1H,s),δ4.50~4.53(4H,m),δ3.94~4.0(2H,m),δ3.39~3.57(2H,m),δ2.91(1H,m),δ2.21(4H,m)
MS(API-ES)(M+H)=324
實施例5
1s-(1α,3α,4β)-2-氨基-6-[[4-苯甲氧基-3-(苯甲氧基)甲基-2-亞甲基環戊基]氨基]-5-硝基-4(3H)-嘧啶酮的製備
在1升三口燒瓶中,加入78.6克中間體5’(0.24摩爾)和445毫升正丁醇,攪拌溶解,加入13.4毫升三乙胺,慢慢加入11.5克2-氨基-4-氯-5-硝基嘧啶酮(0.25摩爾),90℃加熱回流過夜,TLC檢測(甲醇:二氯甲烷=1:20),原料反應完畢。用1升二氯甲烷稀釋,500毫升水洗1次後用無水硫酸鈉乾燥,回收溶劑得到80克灰白色固體。
H NMR:δ10.63(1H,s),δ9.53~9.55(1H,m),δ7.26~7.36(10H,m),δ5.2~5.3(1H,m),δ5.05(1H,s),δ5.12(1H,s),δ4.47~4.50(4H,m),δ3.96~3.98(1H,m),δ3.40~3.60(2H,m),δ2.49~2.51(2H,m),δ2.17~2.56(2H,m)
實施例6
1s-(1α,3α,4β)-2-氨基-9-[4-苯甲氧基-3-(苯甲氧基)甲基-2-亞甲基環戊基]-1,9-二氫-6H-嘌呤-6-酮的製備
在3升三口燒瓶中,加入80克實施例5所得化合物和445毫升正丁醇,攪拌溶解。加入110克保險粉,加熱至60℃,緩慢加入445毫升甲酸,反應2小時後冷卻至室溫,用6N氫氧化鈉溶液中和後真空濃縮至乾。殘留物用二氯甲烷溶解後過濾除去不溶物,過濾液濃縮後加入445毫升原甲酸三乙酯,44.6毫升濃鹽酸,加熱至90℃,反應4小時後用氫氧化鈉中和至PH=7.0,經離子交換樹脂處理得到得到45克灰白色固體物(0.098摩爾),二步總收率:56%。測mp:207-210℃。
H NMR:δ10.53(1H,s),δ7.63~7.36(1H,s),δ7.28~7.63(10H,m),δ6.4(2H,s),δ5.34~5.14(2H,m),δ4.6(1H,m),δ4.52~4.60(4H,m),δ4.10(1H,m),δ3.62~3.63(2H,m),δ2.55(1H,m),δ2.45~2.49(2H,m)
實施例7
恩替卡韋的製備
在5升三口燒瓶中,加入45克實施例6所得化合物和600毫升無水二氯甲烷。-78℃和氮氣保護下,加入1M三氯化硼的二氯甲烷溶液590毫升,反應1小時後升溫至-20℃,反應半小時後再將反應混合物冷卻至-78℃,緩慢加入1.5升甲醇。真空除去溶劑後再加甲醇1.5升,真空除去甲醇,然後用700毫升蒸餾水溶解殘留物,溶液用乙酸乙酯提取後用氫氧化鈉中和至中性,將溶液濃縮至140毫升後有固體析出,過濾後得到恩替卡韋粗品20克(0.067摩爾),收率:68.4%。
H NMR:δ10.57(1H,s),δ7.69(1H,s),δ6.41(10H,s),δ5.36(1H,m),δ5.(1H,m),δ4.89(1H,s),δ4.83(1H,m),δ4.58(1H,m),δ4.22(1H,m),δ3.55(2H,m),δ2.52(1H,m),δ2.21(1H,m),δ2.04(1H,m)
實施例8
恩替卡韋的精製
在1升三口燒瓶中,加入20克恩替卡韋粗品和400毫升蒸餾水,加熱溶解。再加入0.5克活性炭,於95℃保溫攪拌30分鐘,稱熱過濾。收集濾液,冷卻至0℃析晶。得16.5克恩替卡韋,收率L82.5%。測:mp:>220℃,[α]D =+34°(C=0.30,H2 O)。(文獻:mp=234~236℃,[α]D =+33.2°)
實施例9
1s-(1α,3α,4β)-2,5-二氨基-6-[[4-苯甲氧基-3-(苯甲氧基)甲基-2-亞甲基環戊基]氨基]-4-氯-嘧啶的製備
2,5-二氨基-4,6-二氯嘧啶(1克,5.6毫摩爾),用三乙胺(3毫升,20毫摩爾)和正丁醇(20毫升,0.34摩爾)溶解,再加入化合物5’(1.1克,3.5毫摩爾),用TLC跟蹤反應(5%甲醇/二氯甲烷,Rf值=0.8),加熱回流14小時後反應結束。停止加熱,抽濾,乙醇洗滌濾餅,棄去固體,濾液抽乾,用矽膠層析柱分離,得到0.42克目標化合物。
實施例10
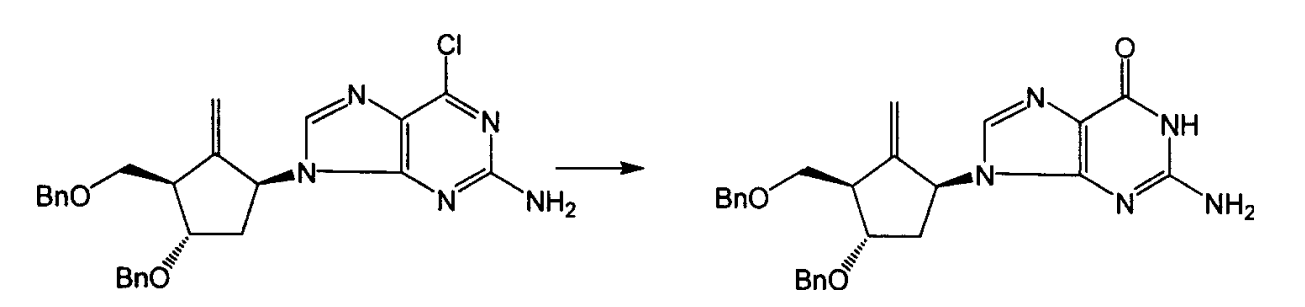
1s-(1α,3α,4β)-2-氨基-9-[4-苯甲氧基-3-(苯甲氧基)甲基-2-亞甲基環戊基]-1,9-二氫-6氯-嘌呤的製備
0.42克實施例9所得化合物,加原甲酸三甲酯(9毫升,0.82毫摩爾)溶解,再加入濃鹽酸(0.5毫升,6.25毫摩爾),TLC跟蹤反應(5%甲醇/二氯甲烷,Rf值=0.5),常溫攪拌4小時後反應結束。停止攪拌,反應液中加乙酸乙酯(50毫升),用NaHCO3 水溶液(1N)中和反應液至pH值=7。分層,有機層用無水硫酸鈉除水,抽乾,用矽膠層析柱分離,得到0.2克目標化合物。
實施例11
1s-(1α,3α,4β)-2-氨基-9-[4-苯甲氧基-3-(苯甲氧基)甲基-2-亞甲基環戊基]-1,9-二氫-6H-嘌呤-6-酮的製備
實施例10產物(0.2克,0.84毫摩爾)加入NaOH溶液(15毫升,0.5摩爾),TLC跟蹤反應(7.5%甲醇/二氯甲烷,Rf值=0.3),100℃攪拌回流6小時後反應完成。後處理:用鹽酸調節反應液pH5-6之間,用乙酸乙酯提取三次,減壓抽乾,用矽膠層析柱分離,得到80毫克目標化合物。
榮譽表彰 2017年12月11日,《抗病毒核苷類似物的合成方法》獲得第十九屆中國專利優秀獎。