基本介紹
- 中文名:Tiffeneau-Demjanov重排反應
- 外文名:Tiffeneau-Demjanov Rearrangement
- 所屬學科:有機化學
- 別名:蒂芬歐-捷姆揚諾夫重排反應、Demjanov-Tiffeneau重排反應
- 底物:1-氨甲基環烷醇
- 條件:亞硝酸
- 產物:多一個碳原子的環酮
- 反應類別:有機人名反應
發展歷史,反應內容,定義,反應特徵,反應機理,意義價值,反應舉例,
發展歷史
1903年,Demjanov, N. J.等人首次發現並報導了氨甲基取代的環烷烴在亞硝酸作用下發生擴環,生成相應的環烷基醇的反應。這類反應後來被稱為Demjanov重排反應。Demjanov, N. J.等人在合成中發現,這種反應最適合製備五元環至七元環,但是製備更小或更大的環時產率很低。
1937年,M. Tiffeneau等人改進了Demjanov重排反應,發現用亞硝酸處理1-氨甲基環烷醇(β-氨基醇)會導致碳環發生擴大,最終生成多一個碳原子的環酮。後來人們將改進後的反應命名為Tiffeneau-Demjanov重排反應。
反應內容
定義
環狀β-氨基醇(1-氨甲基環烷醇)與亞硝酸發生重氮化反應,由於脂肪族重氮鹽不穩定,很快分解放出氮氣,生成活潑的碳正離子,並進一步發生重排反應形成多一個碳原子的環酮。人們一般將這類反應稱為Tiffeneau-Demjanov重排反應。Demjanov重排反應的不同之處在於底物的β-C上沒有羥基取代基,主產物是環烷醇而不是環酮。除此之外,不含碳環的脂肪族伯胺與亞硝酸的反應也可稱為Demjanov重排反應。

Demjanov重排反應
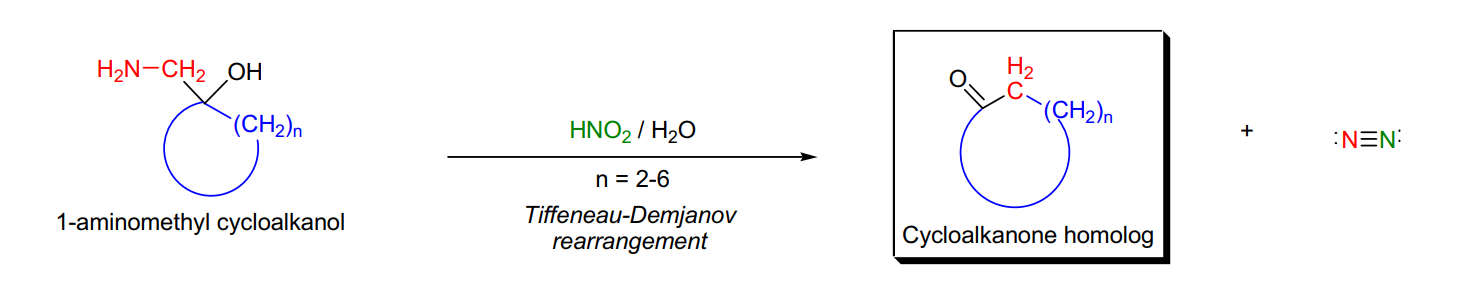
Tiffeneau-Demjanov重排反應
反應特徵
Tiffeneau-Demjanov重排反應可發生在C4~C8的環上,同時該擴環反應的產率通常高於Demjanov重排反應的產率。但是隨著環數的增加,Tiffeneau-Demjanov重排反應的產率趨於下降。如果氨甲基的碳原子被取代,Demjanov重排反應的速率將會明顯減緩,多數生成未重排的醇;相比之下,Tiffeneau-Demjanov重排反應可以正常發生,幾乎不受影響。如果底物中與氨甲基相連的環碳原子上有取代基,Demjanov重排反應則更容易進行。
反應機理
Demjanov重排反應與Tiffeneau-Demjanov重排反應的反應機理基本上是相同的。Tiffeneau-Demjanov重排反應的反應機理為:第一步是由亞硝酸形成亞硝基離子或其前驅體三氧化二氮(N2O3),這種親電試劑受到伯氨基進攻,經過一系列質子轉移形成重氮離子。重氮離子非常不穩定,很容易放出氮氣,生成一級碳正離子,然後發生[1,2]-烷基轉移,生成更加穩定的氧鎓離子,最後去質子化生成環酮。重排同時存在競爭反應,如重氮離去基團被溶劑(例如水)取代,或形成可能發生其他重排(例如氫化物轉移)的碳正離子。因為氫化物轉移的活化熵更高,所以擴環反應有利於Demjanov重排反應的進行。
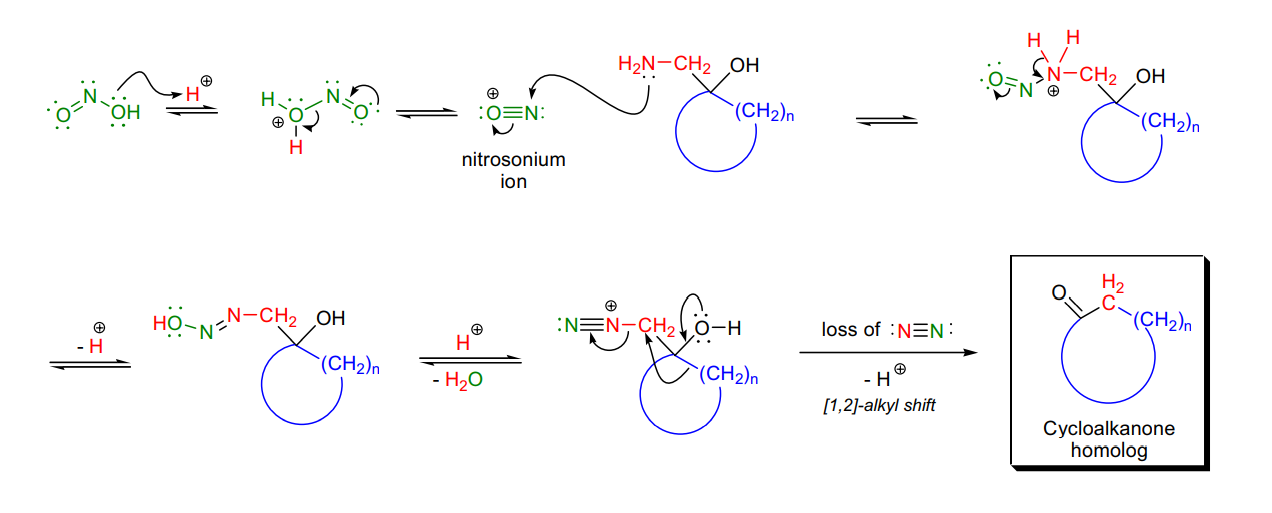
Tiffeneau-Demjanov重排反應機理
意義價值
氨甲基取代的環烷烴與亞硝酸作用生成碳正離子後,會進一步發生一系列取代、消除和重排等反應,得到的是各種產物的混合物,因此Demjanov重排反應在合成上少有實際用途。以環丁基甲胺與亞硝酸反應為例,除得到相應的醇外,還有其他包括重排的反應產物。但是該反應可以定量放出氮氣,根據氮氣的生成量可以測定—NH2的量,可用於脂肪族伯胺的定性和定量分析。
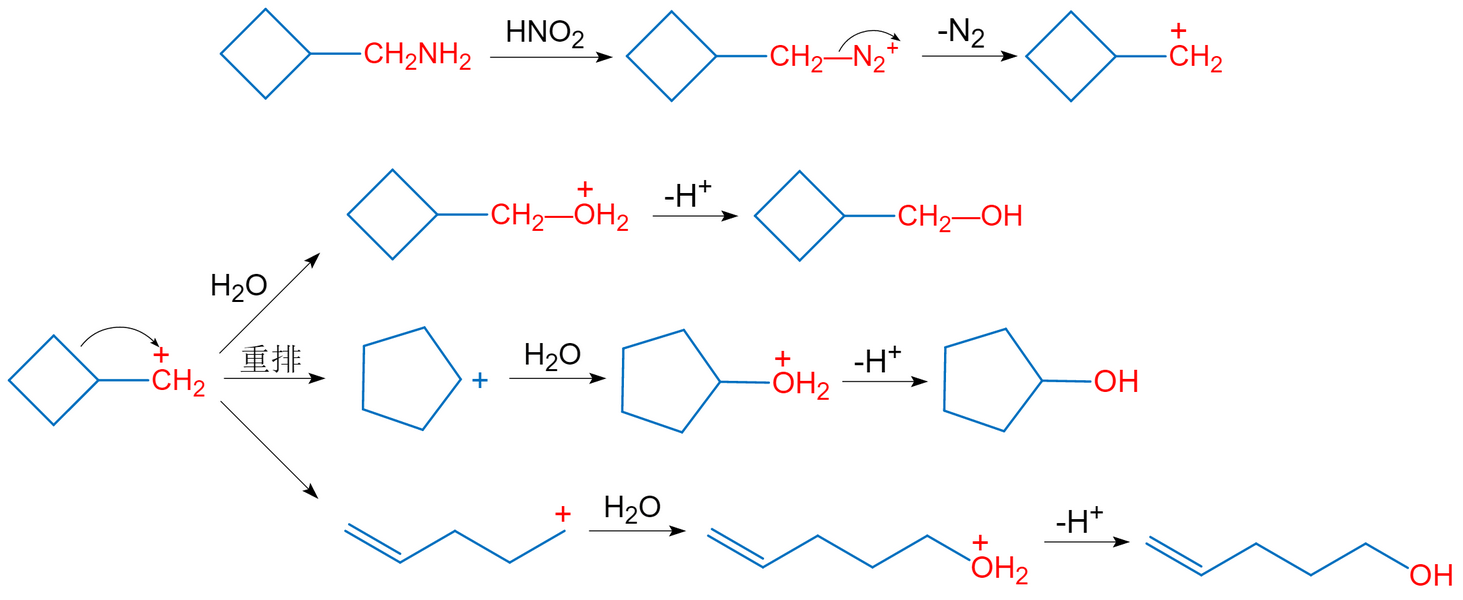
環丁基甲胺與亞硝酸的反應
Tiffeneau-Demjanov重排反應則比較具有實際製備價值,可用於製備C5~C9的脂環酮,提供了由低級環酮合成高級環酮的一種方法。以由環己酮製備環庚酮為例,合成的關鍵一步是由1-氨甲基環己醇通過Tiffeneau-Demjanov重排反應發生擴環。由於亞硝酸不穩定,實際合成中通常由亞硝酸鈉與鹽酸或硫酸混合產生。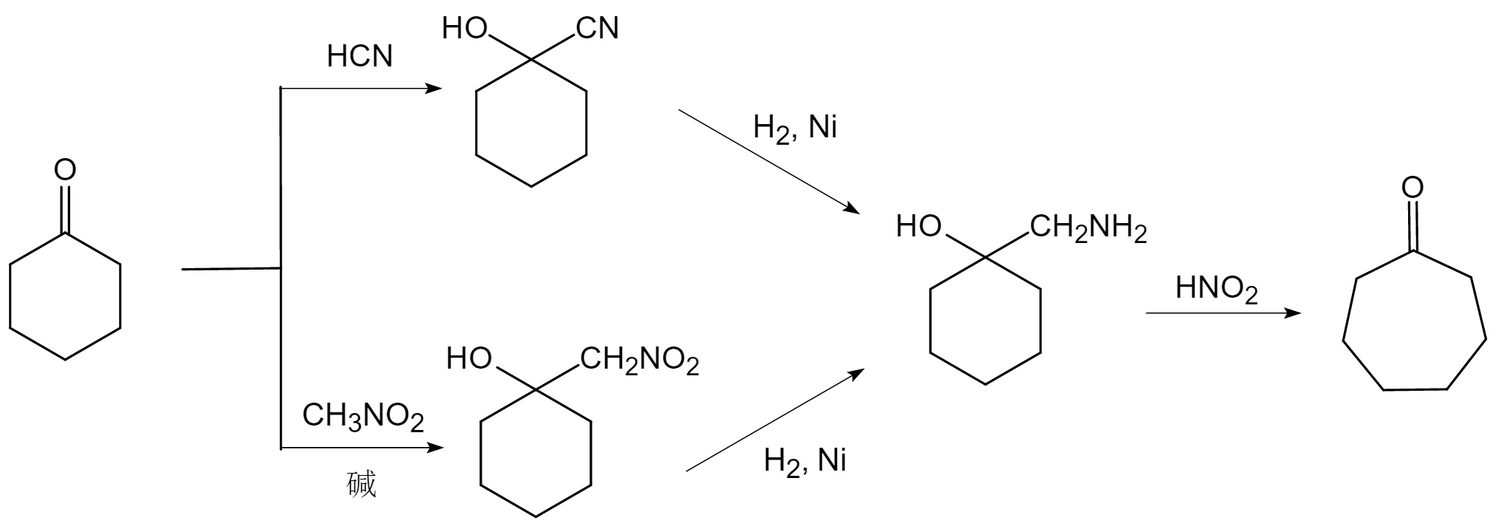

由環己酮製備環庚酮的方法
反應舉例
1988年,為研究大觀黴素類似物的生物活性,E. Fritzen等人製備了擴環且含有七元碳水化合物環的同型黴素,並對兩種差向異構的氨基醇進行了Tiffeneau-Demjanov重排反應擴環的嘗試。令人驚訝的是,只有(R)-差向異構體給出了所需的擴環酮,而(S)-差向異構體提供了相應的環氧化合物作為唯一產物。用亞硝酸處理後,(R)-差向異構體產生等量的三種產物,只有一種產物是所需的擴環酮,而另外兩種產物是(R)-環氧化合物和相應的鄰二醇。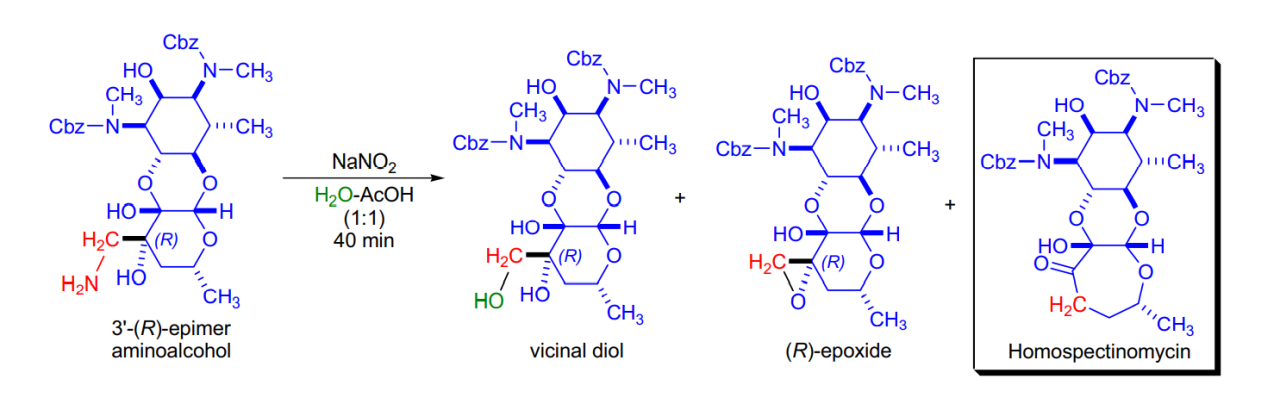

3'-(R)-差向異構體氨基醇與亞硝酸的反應
1992年,A. Nickon等人合成了brexan-2-one (tricyclo[4.3.0.0]nonane-2-one)和擴環同系物homobrexan-2-one。因為Brexane及其衍生物經常用於機理研究,所以需要一種有效且通用的方法來製備這些分子。為此,研究人員以brexane-2-one為底物,首先用三甲基氰矽烷(TMSCN)處理,然後用氫化鋁鋰(LAH)還原,得到氨基醇。再用亞硝酸處理後,繼續進行Tiffeneau-Demjanov重排反應,得到homobrexan-2-one,產率比較高。反應的關鍵一步brexane-2-one母體分子的合成是用一種內型選擇性的分子內Diels-Alder環加成的方法,而同系物的擴環是通過Tiffeneau-Demjanov重排反應實現的。

homobrexan-2-one的合成路線
1993年,P. Vogel等人研究了用亞硝酸處理後2-氨基甲基-7-氧雜雙環[2.2.1]庚烷衍生物的擴環。他們發現,環狀伯胺或氨基醇的立體化學結構顯著影響其各自的Demjanov重排反應和Tiffeneau-Demjanov重排反應的產物分布,部分研究結果如下圖所示。

2-氨基甲基-7-氧雜雙環[2.2.1]庚烷衍生物的反應

