基本信息
中文名稱:膦甲酸鈉
中文別名:膦甲酸三鈉
英文名稱:trisodium phosphonoformate
英文別名:Foscarnet sodium; Foscanet sodium; phosphonoformate sodium salt; FOSCARNET TRISODIUM SALT; SODIUM FOSCARNET;Phenytion Sodium; Foscavir; Triapten; foscarnet sodim
CAS號:63585-09-1
分子式:CNa3O5P
分子量:191.95100
精確質量:191.91800
PSA:113.13000
物化性質
外觀與性狀:白色或近乎於白色結晶粉末
熔點:62-65 °C(lit.)
沸點:270-272°C
閃點:270-272°C
安全信息
包裝等級:II
海關編碼:2942000000
危險品運輸編碼:UN 2811 6.1/PG 3
WGK Germany:3
危險類別碼:R36/37/38
安全說明:S26; S36
危險品標誌:Xi
生產方法
三氯化磷和乙醇反應得到亞磷酸三乙酯。亞磷酸三乙酯和氯甲酸乙酯反應,即可得膦甲酸三乙酯。膦甲酸三乙酯溶於氫氧化鈉的水溶液中,回流、冷卻、過濾得膦甲酸鈉的六水合物。或者將研細的氰化鈉置於四氯化碳中,滴加亞磷酸二乙酯,反應完畢,過濾、濃縮、減壓蒸餾,得氰代磷酸二己酯。將其和氫氧化鈉一起回流、過濾,用水重結晶,得膦甲酸鈉六水合物。
藥品簡介
膦甲酸鈉(別名:膦甲酸三鈉、羧基膦酸三鈉、PFA)
本品為人工合成的抗病毒藥,可抑制病毒
DNA聚合酶,抑制皰疹病毒的複製,也可抑制逆轉錄病毒、AIDS病毒等。臨床可用於敏感病毒所致的皮膚感染,黏膜感染,也可用於
HIV感染者。劑型有3%霜劑供局部外用,亦有靜脈滴注製劑。
 膦甲酸鈉
膦甲酸鈉藥物介紹
藥物名稱
| |
成份
| 膦甲酸鈉
|
化學名稱
| 膦醯甲酸三鈉六水合物。
|
性狀
| 本品為無色的澄明液體。
|
適應症
| |
用法和用量
| 靜脈滴注。劑量個體化。中心靜脈輸註:(注射液24mg/ml)可不需要稀釋直接使用。周圍靜脈輸註:必須用5%葡萄糖或生理鹽水稀釋至12mg/ml後作用。 1、 愛滋病(AIDS)患者巨細胞病毒性 視網膜炎(腎功能正常)。誘導治療:推動初始量為60mg/kg,每8小時一次,靜滴時間不得少於1小時,根據療效連用2~3周。維持治療:維持劑量為90~120mg/kg/日(按腎功能調整劑量),靜滴時間不得少於2小時。維持治療期間,若病情加重,可重複誘導治療及維持治療過程。 2、免疫功能損害患者耐 阿昔洛韋單純皰疹病毒(HSV)性 皮膚黏膜感染。推薦劑量為40mg/kg,每8或12小時一次,靜滴時間不得小於1小時,連用2~3周或直至治。 |
禁忌
| 對膦甲酸鈉過敏禁用。
|
藥理作用
膦甲酸鈉是無機
焦磷酸鹽的有機類似物,在
體外試驗中可抑制包括巨細胞病毒(
CMV)、
單純皰疹病毒1型和2型(HSV-1和HSV-2)等皰疹病毒的複製。在不影響細胞
DNA聚合酶的濃度下,膦甲酸鈉在病毒特異性DNA聚合酶的焦磷酸鹽結合位點產生選擇性抑制作用,從而表現出抗病毒活性。膦甲酸鈉不需要被
胸腺嘧啶激酶或其他激酶激活(
磷酸化),因此在體外對HSVTK
缺失突變株和CMVUL97
突變株有活性。所以,耐
阿昔洛韋的HSV株或耐
更昔洛韋的CMV株可能會對膦甲酸鈉敏感。但是,伴有DNA聚合酶改變的耐阿昔洛韋和更昔洛韋突變株可能也耐膦甲酸鈉。在體外試驗中,將膦甲酸鈉和更昔洛韋聯用可見活性增強。
毒理研究:重複給藥毒性:
大鼠連續
腹腔注射本品90天,劑量分別為200、400、800mg/kg/日,犬連續靜脈滴注本品90天,劑量分別為60、120mg/kg/日。結果顯示,大鼠和犬的無毒性反應劑量分別為200和60mg/kg/日,毒性
靶器官為腎臟,
毒性反應表現為:部分大鼠腎曲小管有伊紅色物質,部分犬出現噁心、嘔吐、厭食等消化道症狀,
尿蛋白陽性,腎灶性間質炎和
腎皮質曲管
上皮細胞輕度變性。
遺傳毒性:當膦甲酸鈉濃度大於0.5μg/ml時,在BALB/3T3體外轉化試驗中表現出
基因毒性作用。當膦甲酸鈉濃度為1000μg/ml時,在姊妹染色體互變試驗中可見
染色體畸變率增加。在小鼠體內試驗中,膦甲酸鈉高劑量(350mg/kg,以AUC計,其暴露量與臨床預期值相當)可引起
微核多染
紅細胞數增加。
 膦甲酸鈉
膦甲酸鈉 生殖毒性:膦甲酸鈉對
大鼠的生育力和一般
生殖行為未見不良影響。大鼠的
圍產期毒性試驗結果陰性。但在以上試驗中,本品的血液暴露量偏低,尚不足以推斷其臨床暴露水平下對人體生育力的潛在影響。雌性大鼠在交配前及交配期間、
妊娠期間和產後21天內皮下注射膦甲酸鈉,劑量達75mg/kg/日時,可引起仔鼠骨骼異常數目輕度增加(<5%)。在妊娠期間,家兔皮下注射膦甲酸鈉75mg/kg/日、大鼠皮下注射膦甲酸鈉150mg/kg/日(以AUC計,其暴露量分別約相當於人體每日最大暴露量的1/3和1/8),可使胎仔骨骼畸形/變異的發生率增加。上述動物研究尚不足以判斷女性患者在膦甲酸的臨床暴露量下的潛在
致畸作用。尚不清楚膦甲酸鈉是否從人乳汁中排泄,但哺乳期
大鼠給予膦甲酸鈉75mg/kg時,母鼠乳汁中排泄的膦甲酸鈉濃度是其血
藥峰濃度的3倍。
致癌性:對大鼠和小鼠進行了經口給藥500mg/kg/日和250mg/kg/日的致癌性研究。以AUC計算,其血漿藥物暴露量分別為人體最大推薦劑量時的1/3和1/5時,未見致瘤作用。未禁食齧齒動物經口給藥的
生物利用度<20%。UOG、E應47OX
動力學
據資料報導,在美國對腎功能正常患者以60mg/kg/次劑量進行間歇靜滴治療(每8小時一次)的二個臨床研究表明:首次用藥後Cmax分別為573μM和445μM,Cmin分別為28μM和88μM;使用至第14或15天的Cmax分別為579μM和517μM,Cmin分別為110μM和105μM;血漿平均
清除率分別為178±48ml/分和130±44ml/分。對接受間歇滴注者第1或第3天的研究提示平均血漿半衰期約3小時,給藥量的80~90%以原形由尿排出。本品能進入患者
腦脊液,腦脊液中藥物濃度與患者的
血腦屏障缺陷程度有關。本品可以蓄積在人的骨中,但蓄積程度尚未確定。分、量2S用7反5應。
 膦甲酸鈉
膦甲酸鈉不良反應
相互作用
3、與
利托那韋和/或沙奎那韋合用可引起腎功能損害。
4、本品可引起低鈣血症,與已知能影響
血鈣的藥物合用時應慎重。DTB4FA8SP類
藥物過量
據PDR(55)版,在一項189例的臨床
對照試驗中,10例過量且出現不良反應事件,只有1例完全恢復。1例以
癲癇大發作呼吸停止而死亡者以每天12.5g連服三天;其他9例服用劑量為推薦劑量的1.14~8倍(平均4倍)。不良反應癲癇發作(3例)、腎功能損害(3例)、
感覺異常(4例)、
電解質紊亂(5例)。本品過量無拮抗劑,
血液透析和水合作用可能有一定療效,該干預的療效尚無法確定。ZN5成不法分674
 膦甲酸鈉
膦甲酸鈉注意事項
2、使用本品期間必須密切監測腎功能,根據腎功能情況調整劑量,做到給藥個體化。
3、本品不能採用快速或彈丸式
靜脈推注方式給藥。靜脈滴注速度不得大於1mg/kg/分。
4、為減低本品的
腎毒性,使用以前及使用期間患者應水化,
靜脈輸液(5%葡萄糖或生理鹽水)量為2.5升/日,並可適當使用
噻嗪類利尿藥。
5、本品不能與其他藥物混合靜脈滴注,本品僅能使用5%葡萄糖或生理鹽水稀釋。
6、避免與皮膚、眼接觸,若不慎接觸,應立即用清水洗淨。
用藥參考
孕婦及哺乳期婦女用藥:無有關孕婦臨床套用研究資料,權衡利弊後慎用。尚不清楚本品是否從哺乳期婦女乳汁分泌哺乳期婦女套用本品時應停止哺乳。
兒童用藥:兒童用藥的安全性和有效性尚未確立。兒童用藥應仔細評價,中有在獲利在於風險時使用。
老年患者用藥:無65歲以上老年人用藥的安全和有效性資料。老年人常合併有
腎小球濾過功能減退,在用藥前以及用藥期間應評價其腎功能狀態。
實驗研究
結果:治療組肝功能改善較對照組明顯(P<0.05)。治療組4,16周
HBV-DNA陰轉率分別為36.7%和53.3%,對照組分別為16.7%和20.0%,兩組比較差異均有顯著性(P<0.05)。治療組顯著提高
輔助性T細胞(
CD4+)和CD4+/CD8+比例。
 膦甲酸鈉
膦甲酸鈉 膦甲酸鈉
膦甲酸鈉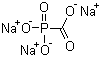 膦甲酸鈉
膦甲酸鈉 膦甲酸鈉
膦甲酸鈉 膦甲酸鈉
膦甲酸鈉