注射用膦甲酸鈉,適應症為1.愛滋病(AIDS)患者巨細胞病毒性視網膜炎;2.免疫功能損害患者耐阿昔洛韋單純皰疹病毒性皮膚黏膜感染。
基本介紹
- 藥品名稱:注射用膦甲酸鈉
- 藥品類型:處方藥、醫保工傷用藥
- 用途分類:逆轉錄酶抑制藥
性狀
適應症
2.免疫功能損害患者耐阿昔洛韋單純皰疹病毒性皮膚黏膜感染。
規格
用法用量
1.愛滋病(AIDS)患者巨細胞病毒性視網膜炎(腎功能正常)。
誘導治療:推薦初始劑量為60mg/kg,每8小時一次,靜滴時間不得少於1小時,根據療效連用2~3周。
維持治療:維持劑量為90~120mg/kg/日(按腎功能調整劑量),靜滴時間不得少於2小時。維持治療期間,若病情加重,可重複誘導治療及維持治療過程。
2. 免疫功能損害患者耐阿昔洛韋單純皰疹病毒(HSV)性皮膚黏膜感染。
推薦劑量為40mg/kg,每8或12小時一次,靜滴時間不得少於1小時,連用2~3周或直至治癒。
腎功能不全者可參照下表應進行劑量調整(表1)
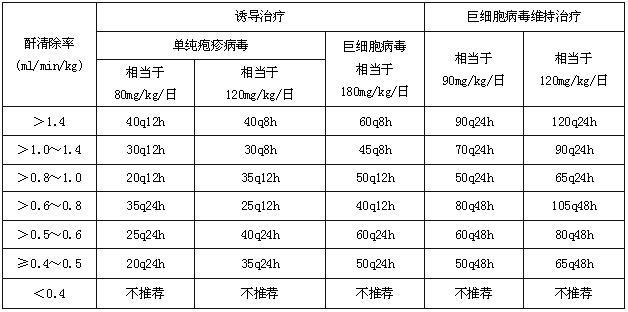
不良反應
腎功能損害:血清肌酐值升高,肌酐清除率降低,腎功能異常、急性腎功能衰竭、尿毒症、多尿、代謝性酸中毒。停止用藥1~10周內血清肌酐值能恢復至治療前水平或正常。
電介質:低鈣血症、低鎂血症、低鉀血症、低磷血症或高磷血症。本品能螯合二價金屬離子(Ca2+、Mg2+、Fe2+、Zn2+)。30%AIDS患者使用本品出現可逆性低鈣血症,呈量效關係。
驚厥(包括癲癇大發作):雖然許多患者出現驚厥可能因低鈣血症或原有疾病(隱球菌腦膜炎、占位性病變或其他中樞神經系統腫瘤),但不能除外與本品的關係。
貧血或血紅蛋白降低:一般不同時伴有白細胞及血小板計數下降。許多AIDS患者同時接受AZT治療,並在接受本品前已存在貧血。
局部刺激:注射部位靜脈炎,生殖泌尿道刺激症狀或潰瘍。
全身:疲乏、不適、寒戰、發熱、膿毒症。
胃腸系統:噁心、嘔吐、腹瀉、腹痛、消化不良、便秘,曾有胰腺炎個例報導。
代謝及營養失調:低鈉血症和下肢浮腫,乳酸脫氫酶、鹼性磷酸酶或澱粉酶升高。
中樞及周圍神經系統:Paraethesia、頭痛、眩暈、非自主性肌肉收縮、震顫、共濟失調、神經病。
精神失調:厭食、焦慮、神經質、精神混亂、抑鬱、精神病、激動、進攻性反應。
肝膽系統:ALT和AST異常。
心血管:ECG異常、高血壓或低血壓、室性心律不齊。
其他:白細胞減少、粒細胞減少、血小板減少、皮疹、肌肉無力。
禁忌
注意事項
2.使用本品期間必須密切監測腎功能,根據腎功能情況調整劑量,做到給藥個體化。
3.本品不能採用快速或彈丸式靜脈推注方式給藥。靜脈滴注速度不得大於1mg/kg/分。
4.為減低本品的腎毒性,使用以前及使用期間患者應水化;靜脈輸液(5%葡萄糖或生理鹽水)量為2.5升/日,並可適當使用噻嗪類利尿藥。
5.本品不能與其他藥物混合靜脈滴注,本品僅能使用5%葡萄糖或生理鹽水稀釋。
6.本品不能與其他腎毒性藥物如氨基糖苷類抗生素、兩性黴素B或萬古黴素等同時使用。本品不能與靜注噴他脒聯合使用,以免發生低鈣血症。
7.避免與皮膚、眼接觸,若不慎接觸,應立即用清水洗淨。
孕婦及哺乳期婦女用藥
兒童用藥
老年用藥
藥物相互作用
2.避免與氨基糖甙類、兩性黴素B腎毒性藥物合用以免加重腎損害。
3.與利托那韋和/或沙奎那韋合用可引起腎功能損害。
4.本品可引起低鈣血症,與已知能影響血鈣的藥物合用時應慎重。
null
藥物過量
本品過量無拮抗劑,血液透析和水合作用可能有一定療效,該干預的療效尚無法確定。
藥理毒理
毒理研究: 重複給藥毒性: 大鼠連續腹腔注射本品90天,劑量分別為200、400、800mg/kg/日,犬連續靜脈滴注本品90天,劑量分別為60、120 mg/kg/日。結果顯示,大鼠和犬的無毒性反應劑量分別為200和60 mg/kg/日,毒性靶器官為腎臟,毒性反應表現為:部分大鼠腎曲小管有伊紅色物質,部分犬出現噁心、嘔吐、厭食等消化道症狀,尿蛋白陽性,腎灶性間質炎和腎皮質曲管上皮細胞輕度變性。
遺傳毒性:當膦甲酸鈉濃度大於0.5μg/ml時,在BALB/3T3體外轉化試驗中表現出基因毒性作用。當膦甲酸鈉濃度為1000μg/ml時,在姊妹染色體互變試驗中可見染色體畸變率增加。在小鼠體內試驗中,膦甲酸鈉高劑量(350mg/kg,以AUC計,其暴露量與臨床預期值相當)可引起微核多染紅細胞數增加。
生殖毒性:膦甲酸鈉對大鼠的生育力和一般生殖行為未見不良影響。大鼠的圍產期毒性試驗結果陰性。但在以上試驗中,本品的血液暴露量偏低,尚不足以推斷其臨床暴露水平下對人體生育力的潛在影響。雌性大鼠在交配前及交配期間、妊娠期間和產後21天內皮下注射膦甲酸鈉,劑量達75mg/kg/日時,可引起仔鼠骨骼異常數目輕度增加([5%)。在妊娠期間,家兔皮下注射膦甲酸鈉75mg/kg/日、大鼠皮下注射膦甲酸鈉150mg/kg/日(以AUC計,其暴露量分別約相當於人體每日最大暴露量的1/3和1/8),可使胎仔骨骼畸形/變異的發生率增加。上述動物研究尚不足以判斷女性患者在膦甲酸的臨床暴露量下的潛在致畸作用。尚不清楚膦甲酸鈉是否從人乳汁中排泄,但哺乳期大鼠給予膦甲酸鈉75mg/kg時,母鼠乳汁中排泄的膦甲酸鈉濃度是其血藥峰濃度的3倍。
致癌性: 對大鼠和小鼠進行了經口給藥500 mg/kg/日和250 mg/kg/日的致癌性研究。以AUC計算,其血漿藥物暴露量分別為人體最大推薦劑量時的1/3和1/5時,未見致瘤作用。未禁食齧齒動物經口給藥的生物利用度[20%。
