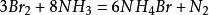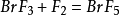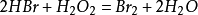發現歷史 溴元素分別被兩個科學家
安東尼·巴拉爾 (Antoine Balard) 和卡爾·羅威(Carl Löwig) 在1825年與1826年所發現。
玻封溴 1824年,法國一所藥學專科學校的22歲青年學生巴拉爾(Balard, Antoine Jerome ),在研究他家鄉
蒙彼利埃 (Montpellier)的水提取結晶鹽後的
母液 ,進行了許多實驗。當通入
氯氣 時,母液變成紅棕色。最初,巴拉爾認為這是一種氯的碘化物溶液,希望找到這些廢棄母液的組成元素。但他嘗試了種種辦法也沒法將這種物質分解,所以他斷定這是和氯以及碘相似的新元素。巴拉爾把它命名為muride,來自拉丁文muria(鹽水)。1826年8月14日
法國科學院 組成委員會審查巴拉爾的報告,肯定了他的實驗結果,把muride改稱bromine,來自希臘文brōmos(惡臭),因為溴具有刺激性臭味。實際上所有
鹵素 都具有類似臭味。溴的拉丁名bromium和元素符號Br由此而來。
事實上,在巴拉爾發現溴的前幾年,有人曾把一瓶取自德國克魯茲拉赫(Keluzilahe)鹽泉的紅棕色液體樣品交給化學家
李比希 鑑定,李比希並沒有進行細緻的研究,就斷定它是“氯化碘”,幾年後,李比希得知溴的發現之時,立刻意識到自己的錯誤,把那瓶液體放進一個柜子,並在柜子上寫上“恥辱櫃”以警示自己,此事成為化學史上的一樁趣聞。
卡爾·賈古柏·羅威在1825年從巴特克羅伊茨納赫村裡的水泉中分離出了溴。羅威用了一個有飽和氯的
礦物鹽 溶液,並用
乙醚 提取出了溴。在醚蒸發後,留下了一些棕色的液體。他用此液體作為他工作的樣本申請了一個在里歐波得·甘末林(Leopold Gmelin)的實驗室的職位。由於發現的公開被延遲了,所以巴拉爾率先發表了他的結果。
在法國科學家路易斯·尼可拉斯·瓦奎寧(Louis Nicolas Vauquelin)和路易斯·賈奎斯·瑟納德(Louis Jacques Thénard)與約瑟夫·路易·蓋-呂薩克證實了年輕藥劑師巴拉爾的實驗之後,結論出現在
法國科學院 的一場演講上,並被發表在化學紀實上。在他發表的論文中,巴拉爾說他基於安格拉達的建議把新元素的名字從muride改成bromine。其他的說法則認為法國的化學與物理學家呂薩克基於它蒸氣的獨特氣味建議了這個名稱。溴直到1860年才被大量的製造。
含量分布 溴元素在自然界中和其他鹵素一樣,基本沒有單質狀態存在。它的化合物常常和氯的化合物混雜在一起,但是數量少得多,在一些礦泉水、鹽湖水(如死海)和海水中含有溴。鹽滷和海水是提取溴的主要來源。從製鹽工業的廢鹽汁
直接電解 可得。整個大洋水體的溴儲量可達100萬億噸。地球上99%的溴元素以Br
- 的形式存在於海水中,所以人們也把溴稱為“海洋元素“。
鹽滷 元素在宇宙中的含量
0.007(ppm)
元素在海水中的含量
65(ppm)
地殼中含量
0.37(ppm)
物理性質 溴是唯一在室溫下呈現液態的
非金屬元素 ,並且是周期表上在室溫或接近室溫下為液體的六個元素之一,深紅棕色發煙揮發性液體。有刺激性氣味,其煙霧能強烈地刺激眼睛和呼吸道。在空氣中迅速揮發。
易溶 於乙醇、
乙醚 、
氯仿 、
二硫化碳 、
四氯化碳 、濃鹽酸和溴化物水溶液,可溶於水。溴的熔點是-7.2 °C,而沸點是 58.8 °C。
原子序數
35
質子數
35
中子數
45
摩爾質量
80
沸點
58.76℃
熔點
-7.2℃
密度
3.119g/cm3
原子化焓:kJ/mol@25℃
111.7
熱容J/(mol·K)
75.69
導熱係數W/(m·K)
0.122
熔化熱(千焦/摩爾)
5.286
汽化熱(千焦/摩爾)
15.438
晶體結構:晶胞為正交晶胞,晶胞參數:
a=672.65pm
α=90°
b=464.51pm
β=90°
c=870.23pm
γ=90°
化學性質
基本性質 溴在化學元素周期表中位於第4周期、第ⅦA族,第一電離能11.814eV,溴是一種強氧化劑,它會和金屬和大部分有機化合物產生激烈的反應,若有水參與則反應更加劇烈,溴是一種
鹵素 ,它的活性小於
氯 但大於碘。溴和金屬反應會產生金屬溴鹽及次溴酸鹽(有水參與時),和有機化合物則可能產生磷光或螢光化合物。溴對大多數金屬和有機物組織均有侵蝕作用,甚至包括
鉑 和
鈀 。與
鋁 、鉀等作用發生燃燒和爆炸。溴可溶於水,但對
二硫化碳 ,
有機 醇類 (像甲醇)與
有機酸 的溶解度佳。它很容易與其他原子鍵結並有強烈的
漂白 作用。
所屬周期
4
電子層排布
2-8-18-7
外層電子排布
4s2 4p5
電子層
K-L-M-N
核電荷數
35
氧化態
Br-1,Br+5,Br+1,Br+3,Br+4,Br+7
化學鍵能:(kJ /mol)
Br-H
366
Br-C
286
Br-O
234
Br-F
285
Br-Br
193
Br-B
410
Br-Si
310
Br-P
264
電離能(kJ/ mol)
M - M+
1139.9
M+ - M2+
2104
M2+ - M3+
3500
M3+ - M4+
4560
M4+ - M5+
5760
M5+ - M6+
8550
M6+ - M7+
9940
M7+ - M8+
18600
M8+ - M9+
23900
M9+ - M10+
28100
氧化還原性 溴最外層電子為4s
2 4p
5 ,有很強的得電子傾向,是
電負度 最大的元素之一,因此具有較強的氧化性。
溴單質能與大部分單質化合,部分需要加熱或其它條件。氫與溴在含鉑的石棉或矽膠催化下,加熱至200~400°C可以化合為溴化氫。溴可以把磷(0)氧化為磷(+3):
,生成的三溴化磷為液體,摻雜著部分五溴化磷。溴與一氧化碳反應,可得到碳醯溴:
。與氨反應,生成溴化銨與氮氣:
。
溴可以置換出水中的一些非金屬陰離子,例如溴與硫離子的反應:
。
溴蒸汽與氟氣混合,或者是將氟氣通入液溴中,可以得到三氟化溴:
,氟氣過量則生成五氟化溴:
。
溴在水中及鹼溶液中容易歧化,在水中反應為
,在0°C及以下的低溫鹼溶液中發生的反應的離子方程式為:
,在50°C及以上的高溫鹼溶液主要發生的反應的離子方程式為:
。
有機反應 在紫外線或250~400°C下,將溴與烷烴或者烯烴(α-H)或者甲苯混合,會發生自由基取代反應,反應將烷烴、烯烴、甲苯上的氫取代為溴。溴發生自由基取代反應時,3°碳,2°碳,1°碳之間的反應活性相差非常大,選擇性較好,得到的產物較為純淨。
在極性溶劑中,溴易發生異裂,生成溴離子,發生離子型反應,例如溴與烯烴的加成。
苯(用
溴化鐵 做催化劑)和純溴的取代反應,不用催化劑反應很慢,用鐵做催化劑時,不需加熱,即可發生反應,該反應是放熱反應。
乙醇可與溴化氫發生取代反應,C2 H5 OH+HBr=C2 H5 Br+H2 0
醛與溴在鹼的催化下或者在酸性條件下由於羰基的作用,醛的α-氫變得異常活潑而被溴取代,生成α-溴代醛和溴化氫,而且往往α-氫趨向於全部被取代,例如,CH3CHO+Br2=Br-CH2-CHO+HBr
化合物
同位素 溴有兩個穩定的
同位素 :Br-79(50.69%)及Br-81(49.31%)。其他至少有23種
放射性同位素 是已被發現可以存在的。 不少的溴同位素是核分裂的產物。有幾種來自於核分裂產物的大原子量的溴同位素會產生延遲性的中子衰變。所有的放射性溴同位素的
半衰期 相對來講是比較短的,半衰期最長的是一個
中子數 不足的同位素半衰期為2.376天。半衰期最長的豐中子同位素的半衰期為1.47天。一些溴的同位素有亞穩定的
同質異能素 。穩定的Br有一個具放射性的同質異能素,半衰期4.86秒,它最終衰變成穩定的基態。
製備方法
工業製備 使用氯氣來處理富含溴的滷水來製備溴,空氣吹出法是工業上製備溴素的主要方法。由於溴單質難保存且商業用途不大,人們不會一次性大量去製備它。
(2)用壓縮空氣吹出Br2 ,並在鹼性環境下歧化:
(3)濃縮溶液,在酸性環境下逆歧化:
實驗室製備 將氫溴酸與過氧化氫混合,溶液就會變為橙紅色(有溴生成),這時將其蒸餾就得到純度很高的液溴。
反應方程式:
,該反應放熱,要注意控制其溫度。溴可以腐蝕橡膠製品,所以在進行有關溴的實驗時要避免使用膠塞和膠管。
在實驗室里,也可以加熱溴化鉀-溴酸鉀與濃硫酸的混合物並蒸餾來制溴單質。
套用領域
工業用途 溴的化合物用途也是十分廣泛的,
溴化銀 被用作照相中的感光劑。使用老式相機時,當你“咔嚓”按下快門的時候,相片上的部分溴化銀就分解出銀,從而得到我們所說的底片。溴可用於製備有機溴化物。溴可用於製備顏料與化學中間體。溴與氯配合使用可用於水的處理與殺菌。
阻燃物
含溴阻燃劑的重要性與日俱增,當燃燒發生時,阻燃劑會生成
氫溴酸 ,它會干擾在火焰當中所進行的氧化
連鎖反應 。高活性的氫、氧與氫氧根自由基會與溴化氫反應成活性沒那么強的溴自由基。 含溴的化合物可以藉由在聚合過程中加入一些被溴化的
單體 或在聚合後加入含溴化合物的方法加入
聚合物 中。添加
四溴雙酚A 可以製造聚酯與環氧樹脂,用於印刷電路板(PCB)的環氧樹脂通常都是由阻燃劑製成的,並且在產品縮寫中以FR來表示。(如FR-4與FR-2)
溴乙烯 可以用來製造
聚乙烯 、聚氯乙烯與
聚丙烯 。
十溴二苯醚 可以添加在已完成的聚合物中。
汽油添加劑
1,2-二溴乙烷 是添加在含鉛汽油中的一種
汽油添加劑 ,它藉由產生揮發性的溴化鉛來移除引擎中的鉛,此類用法在美國占了1966年全部溴用量的77%,但這種用途在1970年代因為會污染環境而被禁止了。
殺蟲劑
溴甲烷 曾被廣泛的用做煙薰土地用的農藥,
蒙特婁公約 決定到2005年逐漸淘汰這種會破壞
臭氧層 的化合物。在1991年,估計有35000公噸的此化合物被用來對付
線蟲動物 、真菌、雜草還有一些土壤的問題。
醫療用途 醫院裡曾經使用的鎮靜劑,有一類就是用溴的化合物製成的,如溴化鉀KBr、溴化鈉NaBr、溴化銨NH
4 Br等,通常用以配成“三溴片”,可治療神精衰弱和歇斯底里症,但是三溴片已經被更好的藥品(
巴比妥 類)所取代了。又如大家熟悉的紅藥水,也是溴與汞的化合物汞溴紅。
藥物合成方面經常需要用到溴元素,比如巴比妥類,成環的時候需要用溴代烷烴,又如頭孢菌素中間體,需要先對原料青黴素V鉀鹽加入對硝基溴化苄進行酯化。
其他用途 鈣、鈉與鋅的溴化物在溴的市場中占有一席之地,這些鹽類在水裡產生稠密的化合物,可以用來做
鑽井液 ,有時也被稱做
clear brine fluids 。
溴也可以用來生產含溴植物油,含溴植物油在許多橘子口味的
軟性飲料 中當作
乳劑 。在此化合物於1940年代被發現後,它被廣泛地使用,直到在1970年代中期,英國與美國限制了它的使用並且研發出了替代用的乳劑。 但在1997年美國的軟性飲料仍然可以含有含溴植物油。
高折射率的化合物,含溴的樹脂型具有較高的折射率和較低的色散。
溴化鉀被一些攝影業者使用來防止霧(不希望出現的銀的還原)的生成。
溴蒸氣被用於敏化銀版攝影法用的銀版的第二步,該版之後會經過汞蒸氣的處理。溴的角色是加強剛被碘化的銀版的光敏。
毒理資料 單質狀態的溴是有毒且有
刺激性 的。因為溴是一種氧化劑,它不能與大部分的有機或無機化合物穩定的共存,所以輸送溴時需要謹慎,通常是使用內襯著鉛的鋼製桶子,並以堅固的金屬架支撐。
當某些特定的含溴離子化合物在酸性環境下與高錳酸鉀(KMnO4 )混合時,會產生淡棕色的溴霧,它聞起來像是漂白水,並且對黏膜有很強的刺激性。
吸入低濃度溴後可引起咳嗽、胸悶、黏膜分泌物增加,並有頭痛、頭暈、全身不適等,部分人可引起胃腸道症狀;吸入較高濃度後,鼻咽部和口腔黏膜可被染色,口中呼氣有特殊的臭味,有流淚、怕光、劇咳、嘶啞、聲門水腫甚至產生窒息,部分患者可發生過敏性皮炎,接觸高濃度溴可造成皮膚重度灼傷。長期吸入溴,可有蓄積性,除表現黏膜刺激症狀外,還伴有神經衰弱綜合徵等。溴氣的預防,主要應做好生產設備及管道密閉,加強局部通風,注意個人防護。
安全措施 泄漏:迅速撤離泄漏污染區人員至安全區,並立即進行隔離,小泄漏時隔離150m,大泄漏時隔離300m,嚴格限制出入。建議應急處理人員戴自給正壓式呼吸器,穿防酸鹼工作服。不要直接接觸泄漏物。儘可能切斷泄漏源,防止進入下水道、排洪溝等限制性空間。
小量泄漏:用蘇打或石灰中和吸收。也可以用大量水沖洗,洗水稀釋後放入廢水系統。
大量泄漏:構築圍堤或挖坑收容;用泡沫覆蓋,降低蒸氣災害。噴霧狀水冷卻和稀釋蒸氣。用泵轉移至
槽車 或專用收集器內,回收或運至廢物處理場所處置。
滅火方法
燃燒性:不燃
滅火注意事項:消防人員必須佩戴
氧氣 呼吸器、穿全身防護服。噴水保持容器冷卻,直至滅火結束。用霧狀水趕走泄漏的液體。用氨水從遠處噴射,驅趕溴蒸氣,並使之中和。但對泄漏出來的溴液不可用氨水噴射,以免引起強烈反應,放熱而產生大量劇毒的溴蒸氣。
緊急處理
吸入:迅速脫離現場至新鮮空氣處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。就醫。
食入:誤服者用水漱口,給飲牛奶或蛋清或純鹼水。就醫。
皮膚接觸:立即脫去被污染衣著,先用水沖洗,然後用1體積(25%)氨水、1體積松節油和10體積(95%)乙醇的混合液塗敷,也可先用苯、甘油等除去溴,然後再用水沖洗。就醫。
眼睛接觸:立即提起眼瞼,用大量流動清水或生理鹽水徹底沖洗至少15分鐘。就醫。
一次誤服大量溴化物者速飲高滲鹽水並探咽導吐,隨即以等滲鹽水洗胃,其後給予
硫酸鈉 導瀉。因溴離子在體內分布與
氯離子 相同,且可互相替代,二者經由腎臟排泄甚少區別,用氯化物後,氯離子排出增加,溴離子相應地增加排出,故對中毒病兒,給服適量
氯化銨 或
氯化鈉 (食鹽),對原有心臟病或心衰水腫的患兒,不宜套用大量氯化鈉,可用氯化銨代替。小兒每日用量為75mg/kg,分4次內服(開始可每小時內服1次),直至血內
溴化物 降至4.85mmol/L(50mg/dl)以下時停用同時給飲大量液,體重症病人可用生理鹽水靜脈滴注(約2500ml/m
2 )或加入適量葡萄糖溶液並可酌用
甘露醇 及利尿劑,加速
毒物 由尿排泄,因氯化物入量過多,則從組織中游離出來的溴離子來不及由腎排出,致使血清溴的濃度暫時性升高,加重病情,嚴重中毒可用
透析 療法其他為對症處理。
儲存運輸 溴單質應該存放在玻璃瓶中,加蓋玻璃塞,密閉。儲存於陰涼、通風的庫房。遠離火種、熱源。庫溫應保持在-5℃~25℃。保持容器密封。應與還原劑、鹼金屬、易燃物或可燃物、金屬粉末等分開存放,切忌混儲。儲區應備有泄漏應急處理設備和合適的收容材料。
起運時包裝要完整,裝載應穩妥。運輸過程中要確保容器不泄漏、不倒塌、不墜落、不損壞。嚴禁與還原劑、鹼金屬、易燃物或可燃物、金屬粉末、食用化學品等混裝混運。運輸時運輸車輛應配備泄漏應急處理設備。運輸途中應防曝曬、雨淋,防高溫。
 玻封溴
玻封溴 鹽滷
鹽滷