基本介紹
理化性質,概述,物理性質,化學性質,光譜圖,紅外光譜,質譜圖,作用與用途,常用用途,治療酗酒,治療癌症,生產方法,木炭硫黃法,電爐法,甲烷硫黃法,儲運方法,使用注意事項,危險性概述,急救措施,消防措施,操作處置與儲存,物質毒性,二硫化碳廢氣治理技術,二硫化碳的危害,二硫化碳治理技術,
理化性質
概述
二硫化碳是一種廣泛性的酶抑制劑,具有細胞毒作用,可破壞細胞的正常代謝,干擾脂蛋白代謝而造成血管病變、神經病變及全身主要臟器的損害。
在常溫常壓下二硫化碳為無色透明微帶芳香味的脂溶性液體,有雜質時呈黃色,少量天然存在於煤焦油與原油中,高純品有愉快的甜味及似乙醚氣味,一般試劑有腐敗臭雞蛋味,具有極強的揮發性、易燃性和爆炸性。燃燒時伴有藍色火焰並被氧化成二氧化碳與二氧化硫。主要用於生產人造粘膠纖維(人造棉、人造毛)和粘膠薄膜,還用以製造四氯化碳、四氯化碳(由二硫化碳與氯反應製得)、二硫代氨基甲酸銨(殺菌劑,由二硫化碳與氨反應製得)、黃原酸酯、浮選礦劑、溶劑和橡膠硫化劑。二硫化碳也是硫、磷、硒、溴、碘、樟腦、樹脂、蠟、橡膠和油脂等的良好溶劑,也是許多有機物進行紅外光譜測定和氫質子核磁共振光譜測定用的溶劑。能大部分從呼吸道攝入體內,也可經皮膚吸收。攝入的有1/4經呼吸排出,少量由尿排出,其餘經代謝轉化。尿中的代謝產物是硫酸鹽和存在對碘疊氮基反應具有陽性的物質,用此為二硫化碳暴露的生物指標。人吸入最低致死量為4000ppm (30分鐘)。急性中毒時,初期興奮、頭痛,繼而意識喪失、昏睡和死亡。低濃度長期暴露時,下肢出現多發性神經炎,伴有頭痛、失眠、性慾減退和記憶力下降,脫離接觸時能康復。長期暴露(例如10年)會發生視網膜症和腎疾患為特徵的血管損傷。美國、日本規定大氣最高容許濃度為10ppm (30mg/m3)。
物理性質
外觀與性狀:無色或淡黃色透明液體,純品有乙醚味,易揮發。
熔點:-111.9℃
密度:1.26g/cm3
相對蒸氣密度(空氣=1):2.64
沸點:46.2℃
穩定性:穩定
分子式:CS2
相對分子質量:76.14
飽和蒸氣壓(28℃時):53.32kPa
燃燒熱:1030.8kJ/mol
臨界溫度:279℃
臨界壓力:7.90MPa
辛醇/水分配係數的對數值:1.86,1.93,2.16
閃點:-30℃
爆炸上限(體積分數):60.0
引燃溫度:90℃
爆炸下限(體積分數):1.0
| 溫度(℃) | 二硫化碳在水中(g) | 水在二硫化碳中(g) |
|---|---|---|
0 | 0.242 | —— |
10 | 0.230 | 0.0086 |
20 | 0.210 | 0.012 |
30 | 0.185 | 0.017 |
40 | 0.111 | 0.022 |
溶解性:不溶於水,溶於乙醇、乙醚等多數有機溶劑
化學性質
| 性質 | 數值 | 單位 | 溫度(K) | 參考文獻 | 狀態 |
|---|---|---|---|---|---|
熱 容Cp | 77.8 | J/(mol·K) | 293 | l(液態,下同) | |
74.89 | J/(mol·K) | 294.81 | l | ||
76.02 | J/(mol·K) | 297.43 | l | ||
78.99 | J/(mol·K) | 298 | l | ||
76.1 | J/(mol·K) | 301.2 | l | ||
標準焓Ho298.15 | 116.94 | kJ/mol | 298.15 | g(氣態,下同) | |
117.1 | kJ/mol | 298.15 | g | ||
89.41 | kJ/mol | 298.15 | l | ||
標準熵Ho298.15 | 151 | J/(mol·K) | 298.15 | l |
log(P) = A - B/(C+t) 其中:Cp = 蒸氣壓 (bar);t= 溫度 (℃) | |||||
溫度範圍 | A | B | C | 適用範圍/℃ | 狀 態 |
276.74~353.08 | 6.85145 | 1122.500 | 236.46 | -10~160 | g |
光譜圖
紅外光譜
 紅外光譜圖
紅外光譜圖| 序號 | 峰位(cm^-1) | 透過率(%) | 半峰寬(cm^-1) | 峰差(%) |
|---|---|---|---|---|
1 | 385 | 17 | 29 | 18 |
2 | 1496 | 9 | 124 | 90 |
3 | 2134 | 47 | 43 | 51 |
質譜圖
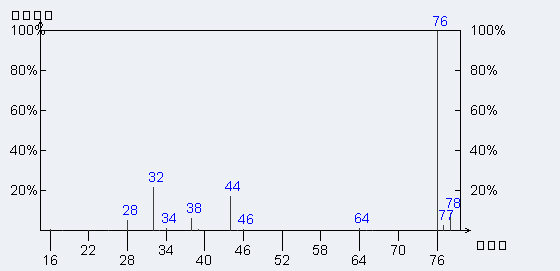 質譜圖
質譜圖作用與用途
常用用途
主要作為製造黏膠纖維、玻璃紙的原材料。用二硫化碳生產的黃原酸鹽供作冶金工業的礦石浮選劑。用於生產農用殺蟲劑。橡膠工業硫化時,可作為氯化硫的溶劑。用它製造氨處理系統中設備和管路的防腐蝕劑。也是檢驗伯胺、仲胺及α-胺基酸、測折射率、色譜分析用的溶劑。也用於從亞麻仁、橄欖果實、獸骨、皮革和羊毛中提取油脂。用作航空的潤滑劑。二硫化碳是殺菌劑稻瘟靈、克菌丹、代森錳鋅、代森鋅、代森銨、福美雙、福美鋅、福美甲胂等的中間體,也是人造纖維的原料、橡膠硫化促進劑。二硫化碳是生產人造絲、賽璐玢、四氯化碳、農藥殺菌劑、橡膠助劑的原料;在生產油脂、蠟、樹脂、橡膠和硫磺等產品時,二硫化碳是優良的溶劑;可用作羊毛去脂劑、衣服去漬劑、金屬浮選劑、油漆和清漆的脫膜劑、航空煤油添加劑等。
治療酗酒
在攝取乙醇大約五到十分鐘後,(乙醇上癮者)便會經歷長達三十分鐘甚至數小時的”宿醉反應”,症狀包括:皮膚潮紅、心臟速度加快、呼吸急促、噁心、嘔吐、劇烈頭痛、視覺障礙、精神錯亂、姿勢暈厥以及循環衰竭。在正常的代謝途徑中,乙醇在肝臟內被乙醇脫氫酶分解成乙醛,隨之再被乙醛脫氫酶分解成毒性較弱的甲酸,而阻斷此代謝途徑的方法便是透過妨礙中間階段的乙醛脫氫酶。若在沒有二硫化碳的影響下攝取乙醇,則乙醛在血液中的濃度可為原本(同樣的乙醇攝取量,不受二硫化碳影響的正常代謝途徑)的5至10倍,又乙醛為造成宿醉的主要原因之一,二硫化碳的衍生物即因此造成酒精攝取後更立即且不舒服的反應。二硫化碳不應在攝取乙醇後的十二小時內使用,此外,人們對於二硫化碳反應並不會隨著使用量、使用次數而有所減少,越長時間使用,二硫化碳的反應越強。當二硫化碳漸漸開始被消化道吸收,消失於體內時,二硫化碳所帶來的效果將會持續大約兩個星期,因此在醫學倫理中規定患者必須詳細了解二硫化碳對酒精的反應。一份發表於2006年的九年研究結果發現,處方用二硫化碳和其相關化合物碳酸胺類(calcium carbimide)的配合使用可以得到50%的戒斷率。使用二硫化碳的衍生物的戒斷治療中,存在最重要的問題為:二硫化碳的產品不能降低患者對於乙醇的渴望,而這帶來了問題:患者的低依從性。公元1986年,Fuller做了經典的研究:追蹤長期酗酒的患者一年。經過追蹤結果統計後發現,服用了的患者與只接受諮詢服務的患者,戒斷率並沒有明顯的不同。因為在研究中,僅有百分之二十服用患者,在藥物治療中有良好的依從性。而改善依從性的方法有:將二硫化碳植入真皮中讓它持續在真皮中釋放12周,再配合監控衍生物的使用(例如,藉由用藥者的配偶來達到監督效果)。 儘管到了二十世紀末,二硫化碳衍生物還是最普遍用來治療酗酒的方式,但如今已被一種由那曲酮和抗酒癮劑(一種麩胺酸的致效劑)結合而成的新藥物給取代。
治療癌症
生產方法
木炭硫黃法
根據不同的加熱方式,可分為外熱式鐵甑法和內熱式電爐法兩類。一般採用三相電爐法。
電爐法
將木炭於800℃直接焙燒除去水分和有機物後間斷加入電爐,熔融硫黃連續加入電爐內與灼紅木炭在1000℃左右進行反應,生成的二硫化碳經除硫、冷凝得到粗製品,再經精餾、冷凝,製得二硫化碳成品。
市售的二硫化碳是將木炭和硫磺加熱至850~950℃的條件下合成的。作為試劑,它可以滿足一般要求,但當要求的純度高時,則需用下述方法除去其中所含的雜質。這些雜質為硫化氫、亞硫酸、硫酸、有機硫化物、水和硫等。將100~200g的汞和適量的五氧化二磷加入到500mL市售的二硫化碳中,振盪1h左右,過濾,將濾液避光分餾,棄去高餾分和低餾分,收集中間餾分。將收集到的分餾物重新與汞和五氧化二磷混合、振盪,並分餾。如此反覆操作直到有害雜質的含量達標為止。 精製方法:所含雜質有硫、硫化物和水等。
精製方法有下列幾種:
(1) 用玻璃制的蒸餾器蒸餾3次;
(2)用氯化鈣乾燥後多次分餾;
(3)與水銀一起搖動除去硫化物,再用五氧化二磷乾燥、分餾;
(4)在1L二硫化碳中加入5g粉碎的高錳酸鉀充分搖動,至完全除去硫化氫後放置,分離後再加少量水銀搖動以除去硫,至界面處不進一步變黑為止。最後每1L二硫化碳中加入5g硫酸汞搖動,以消除臭味。分離後用氯化鈣乾燥、分餾。
甲烷硫黃法
固體硫黃加熱熔融成液狀,然後用活性白土淨化。天然氣淨化處理是利用輕柴油吸附C2以上餾分,分離出純淨的甲烷氣體。天然氣及硫黃蒸氣經加熱後,即可充分混合併加熱至650℃,然後送入反應器進行反應。採用加壓分凝法,使二硫化碳與硫化氫分離,精餾後製得二硫化碳;
以工業品二硫化碳為原料,加入無水硫酸銅 ( 每犔二硫化碳需加25~37.5g硫酸銅) ,充分攪拌至黑色粉末消失,且無難聞氣味為止,立即過濾,除去不溶性雜質,然後在濾液中加入無水硫酸銅,餾,按產品規格收集餾分,即為純品。
儲運方法
運輸注意事項:二硫化碳液面上應覆蓋不少於該容器容積 1/4的水。鐵路運輸採用小開口鋁桶、小開口厚鋼桶包裝時,須經鐵路局批准。運輸時運輸車輛應配備相應品種和數量的消防器材及泄漏應急處理設備。夏季最好早晚運輸。運輸時所用的槽(罐)車應有接地鏈,槽內可設孔隔板以減少震蕩產生靜電。嚴禁與氧化劑、胺類、鹼金屬、食用化學品等混裝混運。運輸途中應防曝曬、雨淋,防高溫。中途停留時應遠離火種、熱源、高溫區。裝運該物品的車輛排氣管必須配備阻火裝置,禁止使用易產生火花的機械設備和工具裝卸。公路運輸時要按規定路線行駛,勿在居民區和人口稠密區停留。鐵路運輸時要禁止溜放。嚴禁用木船、水泥船散裝運輸;
儲存注意事項:在室溫下易揮發,因此容器內可用水封蓋表面。儲存於陰涼、通風的庫房。遠離火種、熱源。庫溫不宜超過30℃。保持容器密封。應與氧化劑、胺類、鹼金屬、食用化學品分開存放,切忌混儲。採用防爆型照明、通風設施。禁止使用易產生火花的機械設備和工具。儲區應備有泄漏應急處理設備和合適的收容材料;
包裝注意事項:小開口鋁桶;小開口厚鋼桶;螺紋口玻璃瓶、鐵蓋壓口玻璃瓶、塑膠瓶或金屬桶(罐)外普通木箱。
使用注意事項
危險性概述
健康危害:二硫化碳是損害神經和血管的毒物。急性中毒:輕度中毒有頭暈、頭痛、眼及鼻黏膜刺激症狀;中度中毒尚有酒醉表現;重度中毒可呈短時間的興奮狀態,繼之出現譫妄、昏迷、意識喪失,伴有強直性及陣攣性抽搐。可因呼吸中樞麻痹而死亡。嚴重中毒後可遺留神衰綜合徵,中樞和周圍神經永久性損害。慢性中毒:表現有神經衰弱綜合徵,植物神經功能紊亂,多發性周圍神經病,中毒性腦病。眼底檢查:視網膜微動脈瘤,動脈硬化,視神經萎縮。
燃爆危險:該品極度易燃,具刺激性。
急救措施
皮膚接觸:立即脫去污染的衣著,用大量流動清水沖洗至少15分鐘。就醫。
眼睛接觸:提起眼瞼,用流動清水或生理鹽水沖洗。就醫。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如出現呼吸困難應立即就醫處治。
食入:飲足量溫水,催吐。就醫。
消防措施
危險特性:極易燃,其蒸氣能與空氣形成範圍廣闊的爆炸性混合物。接觸熱、火星、火焰或氧化劑易燃燒爆炸。受熱分解產生有毒的硫化物煙氣。與鋁、鋅、鉀、氟、氯、疊氮化物等反應劇烈,有燃燒爆炸危險。高速衝擊、流動、激盪後可因產生靜電火花放電引起燃燒爆炸。其蒸氣比空氣重,能在較低處擴散到相當遠的地方,遇火源會著火回燃。
有害燃燒產物:一氧化碳、二氧化碳、二氧化硫。
滅火方法:噴水冷卻容器,可能的話將容器從火場移至空曠處。處在火場中的容器若已變色或從安全泄壓裝置中產生聲音,必須馬上撤離。滅火劑:霧狀水、泡沫、乾粉、二氧化碳、砂土。泄漏應急處理
應急處理:迅速撤離泄漏污染區人員至安全區,並進行隔離,嚴格限制出入。切斷火源。應急處理人員應佩戴安全防護設備。不要直接接觸泄漏物。儘可能切斷泄漏源。防止流入下水道、排洪溝等限制性空間。
小量泄漏:用砂土、蛭石或其它惰性材料吸收。
大量泄漏:構築圍堤或挖坑收容。噴霧狀水或泡沫冷卻和稀釋蒸汽、保護現場人員。用防爆泵轉移至槽車或專用收集器內,回收或運至廢物處理場所進行無害化處理,污染現場,應急處置工具,清洗廢水更應隨之進行無害化處理至達到環保要求。
操作處置與儲存
操作注意事項:密閉操作,局部排風。操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴自吸過濾式防毒面具(半面罩),戴化學安全防護眼鏡,穿防靜電工作服,戴橡膠耐油手套。遠離火種、熱源,工作場所嚴禁吸菸。使用防爆型的通風系統和設備。防止蒸氣泄漏到工作場所空氣中。避免與氧化劑、胺類、鹼金屬接觸。灌裝時應控制流速,且有接地裝置,防止靜電積聚。配備相應品種和數量的消防器材及泄漏應急處理設備。倒空的容器可能殘留有害物。
儲存注意事項:在室溫下易揮發,因此容器內可用水封蓋表面。儲存於陰涼、通風的庫房。遠離火種、熱源。庫溫不宜超過30℃。保持容器密封。應與氧化劑、胺類、鹼金屬、食用化學品分開存放,切忌混儲。採用防爆型照明、通風設施。禁止使用易產生火花的機械設備和工具。儲區應備有泄漏應急處理設備和合適的收容材料。
物質毒性
高濃度時具有麻醉作用。可通過呼吸道及皮膚侵害人體機能,對生物有劇毒。對人體中毒機理,主要使中樞神經中毒引起神經系統疾病。中毒者的處理,是應儘快脫離現場,移至通風良好處,呼吸衰弱者需立即進行人工呼吸。
| 編號 | 毒性類型 | 測試方法 | 測試對象 | 使用劑量 | 毒性作用 |
|---|---|---|---|---|---|
1 | 急性毒性 | 吸入 | 人類 | 4000 ppm/30M | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
2 | 急性毒性 | 吸入 | 人類 | 2000 ppm/5M | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
3 | 急性毒性 | 未知 | 男性 | 186 mg/kg | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
4 | 急性毒性 | 口服 | 齧齒動物- 大鼠 | 1200 mg/kg | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
5 | 急性毒性 | 吸入 | 齧齒動物- 大鼠 | 25 gm/m3/2H | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
6 | 急性毒性 | 口服 | 齧齒動物- 鼠 | 2780 mg/kg | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
7 | 急性毒性 | 吸入 | 齧齒動物- 鼠 | 10 gm/m3/2H | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
8 | 急性毒性 | 口服 | 齧齒動物- 兔 | 2550 mg/kg | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
9 | 急性毒性 | 口服 | 齧齒動物- 豚鼠 | 2125 mg/kg | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
10 | 急性毒性 | 腹腔注射 | 齧齒動物- 豚鼠 | 400 mg/kg | 1.肝毒性——肝臟變性 |
11 | 急性毒性 | 吸入 | 哺乳動物- 未指定 | 2000 ppm/5M | 詳細的毒副作用沒有報告以外的其他致死劑量值 |
12 | 多次劑量 | 口服 | 齧齒動物- 大鼠 | 5055 mg/kg/4W-I | 1.心臟毒性——心律失常(包括在傳導的變化) 2.心臟毒性——脈衝 3.營養和代謝系統毒性——體重減輕或體重增加下降 |
13 | 多次劑量 | 吸入 | 齧齒動物- 大鼠 | 10 mg/m3/5H/13W-I | 1.大腦毒性——其他退化 2.內分泌毒性——其他變化 3.生化毒性——神經遞質多巴胺傳遞異常 |
14 | 多次劑量 | 吸入 | 齧齒動物- 大鼠 | 2000 ppm/4H/2W-I | 1.行為毒性——心理、生理變化 2.慢性病相關毒性——死亡 |
15 | 多次劑量 | 吸入 | 齧齒動物- 大鼠 | 114 mg/m3/8H/20W-I | 1.腎、輸尿管和膀胱毒性——包括急性毒性腎功能衰竭,急性毒性腎小管壞死 2.血液毒性——脾變化 3.慢性病相關毒性——死亡 |
16 | 多次劑量 | 吸入 | 齧齒動物- 大鼠 | 800 ppm/6H/12W-I | 1.營養和代謝系統毒性——體重減輕或體重增加下降 2.生化毒性——抑制轉氨酶活性 3.生化毒性——抑制其他酶活性 |
17 | 多次劑量 | 吸入 | 齧齒動物- 大鼠 | 1500 mg/m3/5H/26W-I | 1.生化毒性——抑制磷酸酶 2.生化毒性——抑制其他酶活性 3.生化毒性——新陳代謝、血液運輸異常 |
18 | 多次劑量 | 吸入 | 齧齒動物- 大鼠 | 800 mg/m3/5H/1Y-I | 1.生化毒性——抑制磷酸酶 2.生化毒性——抑制其他酶活性 |
19 | 多次劑量 | 吸入 | 齧齒動物- 大鼠 | 100 mg/m3/17W-I | 1.心臟毒性——冠狀心臟變化 2.血管毒性——血管結構變化 |
20 | 多次劑量 | 吸入 | 齧齒動物- 大鼠 | 500 ppm/24H/25W-C | 1.周圍神經毒性——傳入神經異常 2.周圍神經毒性——傳出神經異常 3.營養和代謝系統毒性——體重減輕或體重增加下降 |
21 | 多次劑量 | 吸入 | 齧齒動物- 大鼠 | 800 ppm/6H/15W-I | 1.大腦毒性——中樞神經系統異常 2.營養和代謝系統毒性——體重減輕或體重增加下降 |
22 | 多次劑量 | 腹腔注射 | 齧齒動物- 大鼠 | 3 mg/kg/3D-I | 1.脊髓神經毒性——其他脊髓退行性改變 |
23 | 多次劑量 | 腹腔注射 | 齧齒動物- 大鼠 | 6475 mg/kg/4W-I | 1.大腦毒性——其他退行性改變 2.行為毒性——嗜睡 3.行為毒性——激動 |
24 | 多次劑量 | 腹腔注射 | 齧齒動物- 大鼠 | 5600 mg/kg/35D-I | 1.心臟毒性——其他變化 2.血管毒性——血管結構變化 3.血液毒性——血清中成分的變化(如TP,膽紅素,膽固醇) |
25 | 多次劑量 | 口服 | 齧齒動物- 鼠 | 5512 mg/kg/5D-I | 1.內分泌毒性——胸腺重量的變化 2.營養和代謝系統毒性——體重減輕或體重增加下降 3.慢性病相關毒性——死亡 |
26 | 多次劑量 | 吸入 | 齧齒動物- 鼠 | 114 mg/m3/8H/20W-I | 1.胃腸道毒性——其他變化 2.營養和代謝系統毒性——體重減輕或體重增加下降 3.慢性病相關毒性——死亡 |
27 | 多次劑量 | 吸入 | 哺乳動物- 狗 | 1250 mg/m3/8H/11W- | 1.大腦毒性——無明顯變化 2.眼毒性——無明顯變化 3.心臟毒性——心電圖改變 |
28 | 多次劑量 | 吸入 | 靈長目動物- 猴 | 1200 mg/m3/6H/20W-I | 1.內分泌毒性——高血糖 2.血液毒性——血清中成分的改變(例如TP,膽紅素,膽固醇) |
29 | 多次劑量 | 吸入 | 靈長目動物- 猴 | 160 ppm/6H/36D | 1.眼毒性——無明顯變化 |
30 | 多次劑量 | 口服 | 齧齒動物- 兔 | 25298 mg/kg/26W-I | 1.心臟毒性——心臟重量的變化 2.內分泌毒性——高血糖 3.免疫系統毒性——免疫細胞和免疫活性物質減少 |
31 | 突變毒性 | 細菌- 鼠傷寒沙門氏菌 | 100 uL/plate | ||
32 | 突變毒性 | 人類淋巴 | 8 mg/L | ||
33 | 突變毒性 | 人類淋巴 | 10200 ug/L | ||
34 | 生殖毒性 | 吸入 | 男人 | 40 mg/m3,male 91 week(s) pre-mating | 1.生殖毒性生殖毒性——生精功能(包括遺傳物質,精子形態,精子活力和計數)下降 |
35 | 生殖毒性 | 口服 | 齧齒動物- 大鼠 | 2 mg/kg,female 6-15 day(s) after conception | 1.生殖毒性生殖毒性——胎兒毒性(除了死亡,例如,胎兒發育不良) |
36 | 生殖毒性 | 吸入 | 齧齒動物- 大鼠 | 200 mg/m3/24H,female 1-21 day(s) after conception | 1.生殖毒性生殖毒性——胚胎植入前的死亡率增加 |
37 | 生殖毒性 | 吸入 | 齧齒動物- 大鼠 | 10 mg/m3/8H,female 1-22 day(s) after conception | 1.生殖毒性生殖毒性——眼鏡/耳朵發育異常 2.生殖毒性生殖毒性——新生兒活力異常 |
38 | 生殖毒性 | 吸入 | 齧齒動物- 大鼠 | 100 mg/m3/8H,female 1-22 day(s) after conception | 1.生殖毒性生殖毒性——新生兒體重增加緩慢 |
39 | 生殖毒性 | 吸入 | 齧齒動物- 大鼠 | 100 mg/m3/8H,female 1-21 day(s) after conception | 1.生殖毒性生殖毒性——胎兒死亡 2.生殖毒性生殖毒性——顱面發育異常(包括鼻,舌) 3.生殖毒性生殖毒性——發育異常 |
40 | 生殖毒性 | 吸入 | 齧齒動物- 大鼠 | 30 ug/m3/8H,female 1-22 day(s) after conception | 1.生殖毒性生殖毒性——新生兒行為異常 |
41 | 生殖毒性 | 吸入 | 齧齒動物- 大鼠 | 600 ppm/6H,male 50 day(s) pre-mating | 1.生殖毒性生殖毒性- ——生精功能(包括遺傳物質,精子形態,精子活力和計數)下降 2.生殖毒性生殖毒性——前列腺,睪丸,考伯氏腺,其他性腺功能異常 |
42 | 生殖毒性 | 吸入 | 齧齒動物- 鼠 | 2000 mg/m3/2H,female 1-21 day(s) after conception | 1.生殖毒性生殖毒性——胚胎植入前的死亡率增加 2.生殖毒性生殖毒性——產仔數下降 |
43 | 生殖毒性 | 吸入 | 齧齒動物- 鼠 | 10 mg/m3/2H,female 3 week(s) pre-mating | 1.生殖毒性生殖毒性——生育能力下降 |
44 | 生殖毒性 | 口服 | 齧齒動物- 兔 | 350 mg/kg,female 6-19 day(s) after conception | 1.生殖毒性生殖毒性——植入後死亡率增加 |
45 | 生殖毒性 | 口服 | 齧齒動物- 兔 | 2100 mg/kg,female 6-19 day(s) after conception | 1.生殖毒性生殖毒性——其他發育異常 |
二硫化碳廢氣治理技術
二硫化碳是一種常見的 有機溶劑和化工原料 ,工業上廣泛用於生產粘膠纖維、玻璃紙、四氯化碳 、農藥和橡膠的硫化等。在生 產和使用過程中產生的大氣量 、低濃度的 CS2 廢氣 高毒、易燃、易爆 ,對環境和人體健康危害極大 。 為了保護環境和人體健康 ,控制CS2的排放是非常 必要的 。
二硫化碳的危害
二硫化碳對環境的危害
CS2 的化學反應活性較低, 但在平流層中通過光化學反應 , 易被氧化成 SO2, 導致酸雨的形成。因此 CS2對大氣環境所造成的危害是不容忽視的。
二硫化碳對工業生產的危害
CS2 對工業生產也有很大危害。 CS2 緩慢水解生成硫化氫 ,腐蝕生產設備, 造成經濟損失 ;同時毒害下游工業的催化劑, 如合成甲醇、烷基化過程及合成氨等的催化劑 。
二硫化碳對人體的危害
CS2 是一種多系統親和毒物 ,對神經 、心血管、生殖 、胃腸道、泌尿等系統均有毒害作用 。 CS2 主要經呼吸道進入人體 ,高濃度時皮膚亦可吸收。吸入人體後的 CS2廣泛分布於肝、腎、腦、肺、脂肪、肌肉、脾 、心 、腎上腺等器官中 ,其中在肝、腎組織中含量最高,腦組織中含量最低 ,但駐留時間最長 ,中毒主要表現為中樞和 外 周 神 經 損 害。CS2 不僅能引起神經、心血管等系統的 病變, 導致高血壓、冠心病、記憶力減退和失眠等, 而且對生殖系統也有毒害 。有文獻報導, CS2 具有 胚胎毒性和生殖毒性 , 對接觸女工月經也有 影響 。 CS2 可導致胚胎髮育障礙和子代先天缺 陷 ,而且這種致畸作用可隔代遺傳。
二硫化碳治理技術
CS2 廢氣的治理技術歷經多年的發展, 已經形 成一些卓有成效的方法 。
冷凝法
CS2 的沸點為 46.3 ℃,液化溫度低, 所以採用 冷凝法回收 CS2 是一種既經濟又方便的方法。廢 氣中 CS2 含量越高 ,冷卻溫度越低 ,則回收效果越 好 。
目前有些廠家採用常溫水(自來水 )冷卻回收 CS2 ,然後將廢氣直接從排毒塔排出, 這種方法的回 收率較低。比較合理的方法是採用多級列管加填 料 (例如瓷環 )冷卻回收 CS2。此方法冷卻面積大, 冷卻效率高 , 費用較低。其基本流程是 :先將 CS2 廢氣經常溫水 (自來水 )冷卻 (一級), 再經冷凍水 冷卻(二 、三級), CS2 及水蒸氣等可凝性氣體被冷 凝下來 ,再進行提純回收 , 經這種方法處理後 CS2 的回收率大約能提高 20%左右。
吸附法
採用吸附法處理 CS2 廢氣需要吸附性能良好 且成本低廉的吸附劑, 最常用的吸附劑是活性炭。 活性炭吸附 CS2 屬於以物理吸附為主的放熱吸附, 低溫有利於吸附 ,溫度對活性炭的平衡吸附量有負 效應, 而且影響相當嚴重。活性炭吸附 CS2 主要在 微孔中進行 ,吸附量與吸附劑比表面積和微孔體積 有關。
水分對活性炭吸附 CS2 的能力有影響, 因為 活性炭對 CS2 與水蒸氣的吸附具有明顯的選擇 性 ,當水分超過 6% ~ 8%(w)時, CS2 的吸附量 急劇下降。
活性炭吸附 CS2 的一般流程為CS2 廢氣 通過活性炭床層時 CS2 被吸附 ,當活性炭吸附達到 飽和時 ,利用 CS2 沸點低(46.3 ℃)的特性 ,加熱使 其解析出來 ,再冷凝回收。也可用蒸汽直接解析, 解析後的活性炭經乾燥、冷卻後可重新使用。
截止到目前 ,對活性炭吸附 CS2 的研究較多而 對活性炭纖維 (ACF)吸附 CS2 的報導較少。 ACF 具有比表面積大 、微孔數量多 、孔徑分布窄、吸附速 度快 、再生能力強等特點在最近倍受關注。ACF對 CS2 的吸附性能比活性炭優越, 且 使用方便, 吸附量大 。
完全氧化法
完全氧化法包括催化氧化法和熱力燃燒法,後 者需用大量外加燃料燃燒來供熱, 使廢氣溫度提高 到 CS2 的完全氧化溫度 。 催化氧化法在一定條件下 要優於熱力燃燒法。
熱力燃燒法是 CS2 廢氣在熱交換器中預熱後 , 進入熱力燃燒室進行燃燒的方法。該方法的主要 原理是使廢氣中的 CS2 和 O2 反應生成 SO2 進而轉 化成 SO3 , 經吸附或冷凝成為 H2 SO4 。
催化氧化法是將 CS2 廢氣加熱後,在催化劑床 層作用下, CS2 在較低溫度和較短時間內被氧化為 SO2 ,再冷凝為濃硫酸的方法。常用的催化劑有 Al -Mn、Pt、Ti等 。該方法既能便於硫的除去和回 收,又不會產生二次污染 。目前世界上較具代表性 的是丹麥托普索 (Topsoe)公司的 WSA法和瑞士毛雷爾公司的 KVT-SUIFOX法。兩者的反應機理相似
濕式氧化法
螯合鐵氧化法
螯合鐵氧化法是近年來的 一項重要研究課題, 工業上已廣泛用於脫除 H2 S, 如果加以改進, 則可用來脫除 CS2 。將丙二醇、 異丙醇等醇類作為增溶劑加入到 EDTA螯合鐵溶 液中, 可促進難溶於水的 CS2 的溶解。實驗表明, 在 EDTA-Fe濃度為 0.2 mol/L,醇含量(按體積計 算 )約為 30%的條件下 , CS2 的脫除率可達 96%, 但此反應需在較高壓力下進行。
溴水吸收 —電解法
有實驗在洗滌塔中採用溴水吸收化纖加工過程中產生的 CS2 廢氣,得到 HBr和 H2SO4 , 然後電解 HBr,再生循環, 吸收液經濃縮後可得到濃 H2 SO4 。此法回收利用率高,可得到 H2 、H2SO4 等副產 品 ,且 Br2 可循環使用 ,但運轉費用較高 ,對設備防 腐要求較高 。
化學吸收轉化法
此法是通過化學反應將 CS2 轉化吸收從而達 到脫除的一種方法 。例如湖北省化學研究院開發 研製的 MZX高溫有機硫轉化吸收型精脫硫劑 , 採用多種金屬氧化物複合 ,添加一定比例的粘合劑 擠壓成型後 , 再浸漬活性組分後乾燥焙燒而成。
MZX精脫硫劑可以有效地將 CS2 轉化並脫除, 反 應溫度為 350 ~ 450 ℃, MZX精脫硫劑脫硫操作簡 單 ,費用較低 ,在工業上可取代傳統的鈷鉬加氫串 聯氧化鋅的工藝 ,具有良好的工業套用前景。 同時湖北省化學研究院開發研製的 EZ-2寬溫氧化鋅精脫硫劑將 CS2 轉化吸收, 並且可在常溫至 400 ℃的寬 溫區下使用 。其脫硫精度高,能有效保護下游生產 中對硫敏感的催化劑 ,解決了設備硫腐蝕和催化劑 中毒問題,經濟效益顯著。
KDS-I型吸收劑是能在常溫常壓下脫除 CS2 的轉化吸收型脫硫劑 ,此脫硫劑是由胺負載到矽酸 鈣載體上製備的, 在 45 ℃時 KDS-I型吸收劑對 CS2 的脫除率可達 70%以上。
催化加氫或催化水解法
催化加氫脫硫劑是採用具有加氫功能的物質作為活性組分浸漬到 A12O3 或者 A12O3 /SiO2 載 體上構成加氫催化劑 。其活性組分主要有 WNi、 MoNi、MoCo、MoCoNi、WmoNi、WmoNiCo等 , 有時摻 入少量 P、B、F等助劑 。催化加氫法脫除 CS2 是 在 300 ~ 400 ℃使用 CO-MO/Al2O3 催化劑通過加 氫生成 H2S 。
反應生成的硫化氫經串聯固定床反應器脫除 。 催化水解 CS2 在反應溫度 200 ~ 300 ℃進行 , 能耗相對較低, 副反應較少。 CS2 在催化劑上水解 轉化為硫化氫, 然後硫化氫被氧化鐵或活性炭脫硫 劑吸附脫除。水解催化劑通常採用活性氧化鋁 。
研 究了氧化鋁基上 CS2 的水解反應 性 ,有認為 CS2 催化水解反應為鹼催化反應, 鹼性 有利於 CS2 的水解。有學者指出弱的表面鹼性中心是 CS2 水解活性中心, 同時次弱的鹼性 中心也參與 CS2 水解 。
低溫催化水解可以進一步節能降耗和減少副 反應的發生 。 有學者對低溫下催化水解 -氧化 耦合一步法脫除 CS2 的可行性進行了研究 。即在 降低 CS2 水解溫度的同時 ,也能將生成的硫化氫脫 除。催化水解 -氧化耦合是在一個反應器內 ,使用 雙功能催化劑或兩種不同功能的催化劑 ,將原料氣 經催化合成中間產物 , 再進一步催化合成最終產物。在 CS2 的脫除中, 套用了具有水解和氧化 雙功能的催化劑, 實現了一步法脫除 CS2 。
首先 CS2 在催化劑的水解中心水解生成中間產物硫化 氫,然後硫化氫在氧化中心被氧化生成單質硫和硫 酸鹽而沉積於催化劑上 。通過研究 , 得出此方法在低溫 (100 ~ 130 ℃)下脫除 CS2 是可行的 。
電漿法
目前電漿法處理 CS2 廢氣主要處於實驗 室研究階段 , 其基本原理是 :通過陡前沿、窄脈寬 (納秒級)的高壓脈衝電暈放電或通過電場加速作用 ,在常溫常壓下產生非平衡電漿 , 即高能電 子 、O· 、OH·等活性粒子, 對 CS2 分子進行氧化、 降解反應,使其最終轉化為 CO2 、SO2。
光分解法
光分解 CS2 有兩種形式:一種是用特定波長的 光直接照射使 CS2 分解 ;另一種是在催化劑存在 下 ,光照使 CS2 分解。 直接光降解法中 CS2 可直接吸收特定波長的 光輻射而被分解 ,同時廢氣中的氧氣和水蒸汽也能 吸收輻射產生具有較強氧化能力的羥基和高能氧 原子, 這些自由基可以引起 CS2 的氧化反應。
光催化降解 CS2 的基本原理是在一定波長的 光照射下, 光催化劑 (如常用的 TiO2 )被激活 , 使 H2 O生成羥基自由基,然後羥基自由基將 CS2 氧化 降解。
生物法
生物法利用微生物的生命活動處理 CS2 廢氣, 具有投資省 、運行費用低 、較少產生二次污染等優 點 。生物法的關鍵在於填料的選擇和脫硫微生物 的選擇與培養 。因為降解 CS2 的菌株不易培養馴 化 ,目前對生物法處理 CS2 的研究文獻不是很多。
曾報導過降解 CS2 的菌株研究結 果 ,但只報導了一種可用於 CS2 降解的菌株。 生物法處理 CS2 廢氣主要是套用噬硫桿菌群 的生化作用 , 套用最為廣泛的菌種是排硫桿菌 (ThiobacillusYhioparus)、氧化硫桿菌 (T:ThioXidans)等。微生物通過一系列生化反應將廢氣 中的 CS2 轉化為無害的 CO2 氣體 、單質硫或硫酸 鹽 ,同時在氧化過程中獲得能量, 並以 CS2 為碳源 合成細胞成分。
在國內 ,生物法處理 CS2 廢氣還處於研究階 段 ,目前還未開發出生物法處理的工藝和裝備 。在 國外, 義大利斯尼亞 (SNIA)公司和奧地利蘭精 (LENZING)公司都擁有套用微生物工程治理粘膠 纖維工業廢氣中 H2S和 CS2 的技術 。兩家公司的 工藝流程很相似 :首先將廢氣泵入生化塔 ,在生化 塔中利用噬硫桿菌群將廢氣中的 H2 S、CS2 吸收轉 化為硫或硫酸鹽 ,進而稀釋成硫酸回收 , 淨化後的 氣體直接排放,廢氣中其他雜質通過生化塔後的過 濾器濾除,清液經補水和調溫後回用 。