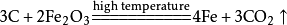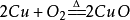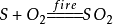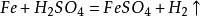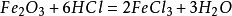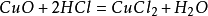要點,書寫步驟,反應條件,箭頭與等號,氣體符號與沉澱符號,物質狀態,要領技巧,書寫的技巧,計算,配平方法,最低公倍數法,觀察法,奇偶配平法,得氧失氧法,指姆大法,待定係數法,國中化學,氧氣,自然界中的水,質量守恆定律,碳和碳氧化物,燃料及其利用,還原方程歸總,金屬,酸鹼鹽,高中化學,非金屬單質,非金屬氧化物,金屬氧化物,含氧酸,鹼,鹽,氧化還原,離子反應,記憶方法,
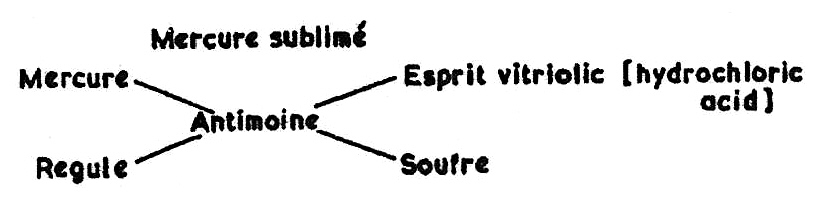 史上第一條化學方程式 Jean Beguin 1615年
史上第一條化學方程式 Jean Beguin 1615年要點
書寫步驟
第一步:寫出反應物和生成物的化學式。
第三步:註明反應條件和物態等。
第四步:檢查化學方程式是否正確。
反應條件
1.
熱化學方程式寫反應條件。一般的在等號上方標記Δ。配平係數大多不可以是可以是分數(相互之間可以約分除外)。
2.常溫常壓下可以進行的反應,不必寫條件;但是題目中的實驗若有特定的條件,一律標註該特定條件(如加熱)。
3.反應單一條件時,條件一律寫上面;有兩個或更多條件的,上面寫不下的寫在下面;既有催化劑又有其它反應條件時,一律把催化劑寫在上面。
箭頭與等號
在專業領域的文獻中,不論無機、
有機反應方程式中均使用
箭頭號“→ ”來連線反應物和生成物。國外化學教科書、上海市中學化學二期課改教材(上海科學技術出版社2006年7月,姚子鵬主編)、2011-2012蘇教版化學書、上海高考的化學卷、理綜卷中也採用了箭頭號。但在多數省市的中學教學中,仍建議按照教材在書寫無機化學反應方程式時使用等號,以更好地表示反應中的“生成”與“
質量守恆”含義。
2013年中學階段
無機反應方程式一律用等號連線反應物和生成物,
有機反應一律用箭頭來連線反應物和生成物,是
可逆反應的一律用可逆符號表示。
氣體符號與沉澱符號
1. 氣體符號“↑”和沉澱符號“↓”是化學反應中生成物的狀態符號。只有生成物才能使用“↑”或“↓”符號,使用時寫在相應化學式的右邊。
2. 當生成物在反應條件是氣態的,才用“↑”號,如:
但還必須同時注意兩點:
(1)若反應物中有一種或幾種氣態物質,則生成的氣態物質不再用“↑”號,如:
(2)不論反應物狀態如何,只要產物只有一種物質,且是氣體時也不用“↑”。
3. 在溶液中進行的化學反應,有難溶物質或不溶物質生成時,用“↓”號表示。如:
4. 若反應不是在溶液中進行的,就不存在沉澱析出現象,不能用“↓”號。如:
5. 對於金屬與鹽溶液之間的置換反應,生成的金屬單質,由於覆蓋在金屬的表面,沒有沉澱析出,不應使用“↓”號,如:
6. 在複分解反應中,若生成物是微溶物時,應把它視為“沉澱”,標上“↓”。如:
7. 必須以客觀事實為依據,即使是同一個化學反應,也必須要看具體情況。如硫化氫與二氧化硫氣體混合反應生成硫,不用沉澱符號,即:
當把二氧化硫通入到氫硫酸時,溶液中出現了黃色的渾濁現象,生成的單質硫應標上“↓”,即
又如向氯化銀懸濁液中滴加硫化鈉溶液,白色沉澱變成黑色,發生了沉澱的轉化,生成的硫化銀應標上“↓”,即:
物質狀態
熱化學方程式
加熱化學方程式需要標出每一個反應物、生成物的狀態,可分g (氣體)、l (液體)、s (固體)、aq (溶液)四大類。字母外需要打括弧,例如H2O (l)、Na2CO3(aq)、CaCO3(s)。
普通方程式則不用g、l、s、aq的標記。生成物方面,當反應物中不含氣體時,氣體生成物要用“↑”標記;只有在溶液中,反應物中不含固體時,難溶或固體生成物一律用“↓”標記。如電解池反應的化學方程式:
水蒸氣
反應物狀態的不同
反應物若以特殊狀態參加反應,例如濃硫酸、熔融
氧化鋁,過量,少量,一律在相應的反應物後打括弧註明狀態
<1>反應物的濃度不同,產物不同
如:銅與濃硝酸反應的化學方程式:
銅與稀硝酸反應的化學方程式:
如:鎂與過量二氧化碳反應的化學方程式:
鎂與少量二氧化碳反應的化學方程式:
如:電解氯化鈉溶液的化學方程式:
電解熔融氯化鈉的化學方程式:
有機反應 合成酚酞
合成酚酞 有機反應化學方程式中,有機物一般採用結構簡式(這並不是絕對的,如燃燒反應、使用分子式就能體現反應原理的化學反應)
燃燒反應無需考慮有機物結構,因此可以採用分子式:
有機物根據其簡化程度不同,可以有多種結構簡式,如乙醇的結構簡式可寫為CH3CH2OH或C2H5OH。根據其反應原理不同,選取的結構簡式一般不同。
如乙醇與HBr的取代反應或脫水成醚的反應等,此類反應的原理為乙醇中-OH發生的反應,故烴基部分可以不體現出來,乙醇一般寫作C2H5OH(也可採用CH3CH2OH)。
但是,乙醇的催化氧化反應、消去反應的原理是烴基部分發生了反應,則烴基需表現出來,乙醇則應寫為CH3CH2OH。
很多物質也是同理,例如苯酚的酸性反應,是苯酚中-OH發生了反應,所以苯酚的結構簡式一般寫為C6H5OH(也可以將苯環體現出來)。
如果是苯酚的取代反應(如與Br2的反應),是苯酚中的苯環發生了反應,這時在書寫苯酚的結構簡式的時候,苯環則需體現出來。
根據這個原則,有些物質甚至可以採用分子式,如溴乙烷的水解反應。
但如果是溴乙烷的消去反應,則是烴基部分發生了反應,溴乙烷則需使用結構簡式,即CH3CH2Br。
以上原則僅適用於有機化合物,對於無機物在有機反應的書寫方法,可根據自身習慣選擇使用分子式(化學式)或結構簡式。(硝酸的結構簡式為HO-NO2,水的結構簡式為H-OH,溴的結構簡式為Br-Br)。
要領技巧
化學式在化學用語系列中,處於承上啟下的地位,前有元素符號和化合價知識,這是書寫化學式的基礎;後有化學方程式和
電離方程式等,這又是以化學式為基礎的,其中如有一個化學式錯誤,則全式毫無意義,若再以這樣的錯誤化學方程式作依據進行化學計算,則錯得更遠,真可謂是“失之毫釐,差之千里”。可見,掌握書寫化學式的要領,直接影響著其他化學用語、其他化學知識和技能的學習。
國中化學中,出現的不同物質的化學式有一百多個。記憶和書寫物質的化學式,絕不能靠死記硬背,而應掌握其書寫要領,只要常寫常練,便能較快地達到熟練的程度。
要正確書寫物質的化學式,一是要熟練記憶元素符號,二是書寫化合物的化學式時,要熟練記憶常見元素和原子團的化合價,三是書寫化合物的化學式要符合各元素正負化合價的代數和為零的原則,四是掌握書寫化學式的一般方法。總起來說,這就是書寫化學式的要領。
化學式的一般寫法是:
(1)單質的化學式
除H2、O2、N2、F2、Cl2、Br2和I2七種單質為雙原子分子,O3為三原子分子,P4為四原子分子外,其餘單質(稀有氣體、金屬單質和非金屬固態單質等)都是以元素符號表示其化學式。
(2)化合物的化學式
書寫時一般規律是先讀後寫,後讀先寫;排好順序,寫好角號。一般將顯正價的元素或
原子團寫在左邊,顯負價的元素或原子團寫在右邊。其書寫步驟是:定位、標價、交叉約簡和檢驗四步。
例如:寫出氧化鋁、磷酸、
氫氧化銅和硫酸鐵的化學式。
①定位:確定元素或原子團的順序。
Al O、H P O4、Cu O H、Fe S O4
②標價:正確地在各元素或原子團的上方標出化合價。
③交叉約簡:將化合價的絕對值交叉寫在對方元素或原子團的右下方,能約簡的要約為最簡約數。原子或
原子團的個數為1時,通常1省去不寫。原子團在2個或2個以上時,應加上括弧。
④檢驗:當正價總數與負價總數之和為零時,化學式正確。
Al2O3、H3PO4、Cu(OH)2、Fe2(SO4)3
上述步驟是對初學者而言,寫得多了,熟練了,便可得心應手一次寫出。要注意的是,化學式表示某物質的組成,因此,只有某種物質是確實存在的,表示這種物質的化學式才有意義。不是任意兩種或兩種以上的元素都能化合成化合物,所以,我們不能隨意寫出一種客觀上不存在的物質的化學式。
書寫的技巧
1.書寫化學方程式的步驟
以書寫碳在高溫時跟氧化鐵反應的化學方程式為例,歸納步驟如下:
①根據反應的事實(該反應生成鐵和二氧化碳氣體),在式子的左邊寫出反應物的化學式,在式子的右邊寫出生成物的化學式。反應物或生成物不止一種,就分別用
加號把它們連線起來(反應物之間的“+”號表示“……跟……反應”,生成物之間的“+”號表示“……跟……”),並在式子左、右之間劃一條短線段。在這一步里,一定要注意把各種物質的化學式寫正確,否則,寫出的式子無意義!
②根據質量守恆定律,用配係數的方法,使左、右兩邊同一元素原子的個數相等(即配平),然後將短線段改為等號(等號表示“生成了……”)。應當注意,配平時只能選擇適當的係數,不能改變化學式。
③在等號或箭號上、下方註明反應條件,如點燃、電解、高溫、加熱(用“△”號表示)、催化劑等,同時,標明生成物中的氣體或沉澱產物的狀態。生成物是氣體的在其化學式的右邊加上“↑”號(反應物中如有氣體,則氣態生成物不再標“↑”符號);產物是沉澱的加“↓”號。
概而言之,在書寫化學方程式時,必須要符合化學反應的客觀規律,不能憑空臆造。書寫程式一般是:寫好化學式—係數要配平—中間聯等號—條件要注清—生成氣體或沉澱,要用箭號來標明。
要寫好化學方程式,還要熟練掌握和運用酸、鹼、鹽的溶解性表,金屬活動性順序和常見元素、原子團的化合價,以及書寫物質化學式的技能。
2.化學方程式書寫中常見錯誤簡析
化學方程式的書寫,是元素符號和化學式書寫能力的綜合運用,因而也是化學用語學習中顯得尤為重要和難度較大的部分。
這裡,跟同學們談一談書寫化學方程式中應注意避免的幾種錯誤,概括起來,主要有“四亂”。
一是亂套“公式”。一些同學書寫化學方程式時,雖然注意了不能憑空臆造化學式,但又沒有掌握典型記憶與類型推導相結合的方法,加之缺乏化學基礎知識,因而把記住的某個熟悉的化學方程式當作為一般公式去套用,犯了亂套“公式”的錯誤。
當然,某些化學性質相似的物質,可以發生一些相似的化學反應,這在典型記憶與類型推導相結合的方法中已敘述過。
由此可見,書寫化學方程式不一定象數學、物理上那樣,有固定的公式可套,而是要根據反應物的性質和反應的條件,運用化學基礎知識和理論來推測反應能否發生,從而寫出正確的化學方程式來。
二是亂寫逆反應。產生此類錯誤的原因是,國中學生把化學方程式與
數理方程式混為一談,隨意把化學方程式倒過來寫。我們知道,數理方程式可以
移項,或將
等號左右兩端反過來寫;而化學方程式與數理方程式是絕然不同的兩種概念。雖然有些化學反應是可逆的,但多數化學反應並非如此。至於有些反應,在相同或不相同的條件下,能夠向相反方向進行,也不一定是可逆反應,而是意義完全相反的
反應類型。
上述情況,雖在獨立場合都正確,但絕不能相互代替。
此外,對於複分解反應中,除注意生成物中要有沉澱析出、放出氣體或生成水的條件才能使反應發生外,還應注意在鹽與鹼、鹽與鹽的反應中,鹽和鹼都必須是可溶性的
電解質。否則反應照樣不能發生。
三是亂標生成物的狀態和反應條件。
四是亂寫化學式。例如:
這類錯誤較為嚴重。這是對物質的化學式的書寫規則不懂或沒有入門造成的。克服的辦法是:在書寫每一個化學式時,都要運用化合價規則去檢驗校正,在所有化學式都正確的基礎上再進行配平。
計算
一. 重點和難點
重點:根據化學方程式計算的方法、格式和步驟。
難點:不純物的計算。
二. 具體步驟
1. 根據化學方程式的計算
化學方程式不僅表示什麼物質參加反應和反應後生成什麼物質,而且還表示反應物和生成物各物質間的質量比。根據化學方程式的計算就是依據反應物和生成物之間的質量比進行的。因此,已知反應物的質量可以算出生成物的質量;已知生成物的質量可以算出反應物的質量;已知一種參加反應的反應物的質量可以算出另一種參加反應的反應物的質量;已知一種生成物的質量可以算出另一種生成物的質量。
化學計算題是從“量”的方面來反映物質及其變化規律的。
化學計算包括化學和數學兩個因素,其中化學知識是數學計算的基礎,數學又是化學計算的工具。根據化學方程式的計算,必須對有關的化學知識有清晰的理解,熟練掌握有關反應的化學方程式。如果化學方程式中的化學式寫錯了,或者沒有配平,化學計算必然會得出錯誤結果。
2. 根據化學方程式計算的步驟
(1)根據題意設未知量。
(2)根據題意寫出正確的化學方程式。
(3)寫出有關物質的相對分子質量或相對分子質量和以及已知量和未知量。寫在化學方程式的相對應的化學式的下面。
(4)列比例式,求解。
(5)簡明的答題。
3. 根據化學方程式計算的注意事項
(1)解題格式必須規範。
(2)根據化學方程式計算是以
純淨物的質量進行計算,對於不純的反應物或不純的生成物必須折算成純淨物的質量,再進行計算。
(3)必須正確使用單位。
4. 根據化學方程式計算時,常見的錯誤:
(1)不認真審題,答非所問。
(2)元素符號或化學式寫錯。
(3)化學方程式沒有配平。
(4)相對分子質量計算錯誤。
(5)單位使用錯誤。
(6)把不純物質當成純淨物進行計算。
配平方法
最低公倍數法
A、找出原子個數較多,且在反應式兩邊各出現一次的
原子,求它的最低公倍數。
B、推出各分子的係數。
例如:
第一步:CuSO4+NaOH-----Cu(OH)2+Na2SO4
第二步:CuSO
4+2NaOH----Cu(OH)
2+Na
2SO
4(
配平)
第三步:CuSO4+2NaOH===Cu(OH)2↓+Na2SO4(註明生成物物態)
觀察法
從化學式較複雜的一種生成物推算有關各反應物化學式的化學計量數和該生成物的化學計量數;根據求得的化學式的化學計量數,再找出其他化學式的化學計量數,直至配平。
例如: 第一步 H2O(g)+Fe---Fe3O4+H2
第二步 4H2O(g)+3Fe---Fe3O4+H2
第三步 4H2O(g)+3Fe====Fe3O4+4H2(反應條件:加熱)
奇偶配平法
看哪種元素在反應化學方程式左右兩邊出現次數最多;從該元素個數為奇數的化學式入手,將其配成偶數(即化學計量數為2);由它求得的化學計量數配平其他化學式的化學計量數,使兩邊原子個數相等。
例:配平
H2O(g)+Fe---Fe3O4+H2
4H2O(g)+Fe---Fe3O4+H2
4H2O(g)+3Fe---Fe3O4+4H2
第三步:配平後的化學方程式:
4H2O(g)+3Fe====Fe3O4+4H2(反應條件:加熱)
4、待定化學計量數法
以不同的未知數代表化學方程式中各化學式的化學計量數;根據
質量守恆定律,反應前後各原子的種類不變、各原子的數目相等,列出數學方程組;解方程組,並令其中任一未知數為1,求出其他未知數的值;最後將未知數的數值代入原化學方程式。
例如:NH3+Cl2----NH4Cl+N2
設各物質的化學計量數依次為a、b、c、d。
aNH3+bCl2----cNH4Cl+dN2
列方程組 a=c+2d (滿足氮原子數相等)
3a=4c (滿足氫原子數相等)
2b=c (滿足氯原子數相等)
令b=1,解得:a=8/3,c=2,d=1/3
8NH3+3Cl2====6NH4Cl+N2(由於係數不能為小數,所以a,b,c,d均擴大3倍得出)
5 、化合價升降法
一、配平原則由於在氧化
還原反應里存在著電子的轉移,因此元素的化合價必然有升有降,我們把化合價能升高的元素或含該元素的物質稱還原劑;反之稱為氧化劑。由氧化還原反應的知識我們不難得出配平原則:還原劑失電子總數=氧化劑得電子總數,即
還原劑(元素)化合價升高的價數=氧化劑(元素)化合價降低的價數。
二、氧化還原反應方程式配平的一般方法與步驟
1、一般方法:從左向右配。
2、步驟:標變價、找變化、求總數、配係數。
即:⑴ 標出變化元素化合價的始態和終態;
⑵ 始態 終態 變化的總價數 = 變化 × 係數
註:假設以上變化均以正價表示,其中(b-a)×(d-c) 為最低公倍數。
⑶ 將 上的係數,分別填在還原劑和氧化劑化學式的前面作為係數;
⑷ 用觀察法配平其它元素;
⑸ 檢查配平後的方程式是否符合質量守恆定律(離子方程式還要看是否符合電荷守恆)
得氧失氧法
對於
氧化還原反應,先觀察得出氧化劑失氧的數目,再觀察得出還原劑得氧的數目,然後配平
比如:3CO+Fe2O3====2Fe+3CO2
氧化劑
氧化鐵反應前後失掉三個氧,
還原劑一氧化碳反應前後得到一個氧,所以需要三個一氧化碳才能奪去氧化鐵中的氧,一氧化碳、二氧化碳配3,鐵配2
指姆大法
普通的完全氧化還原反應,可用兩對反應物與生成物元素化合價升或降價的差約分交叉成為係數,然後配平。例如:C+H2SO4——CO2+SO2+H2O,C的化合價為0,CO2中C的化合價為+4,兩者價相差4。H2SO4中S的化合價為+6,SO2的化合價為+4,兩者價相差2。兩元素的價差比(C:S)為4:2=2:1,交換為1:2,即反應中1個C對應2個H2SO4,即1C+2H2SO4——CO2+SO2+H2O,然後配平為C+2H2SO4=CO2+2SO2+2H2O
普通部分氧化還原反應在後邊變價的位置放手指,歧化反應必須在後邊放,歸中反應一般在前面放。有關於有機物參加反應的配平,有機物中的氫永遠為+1價,O永遠為-2價,碳的化合價設X解(可能為分數)。
待定係數法
你可假設這個化學方程式每一物質前面的係數為x,y,z,m,n.......字母隨你寫,然後根據反應前後元素種類與原子個數相等,算出每一 元素的比值即x,y,z,m,n.......的比值再根據 最低公倍數法去配平。
例如:NH4NO3--N2+O2+H2O
我們把它寫為xNH4NO3--yN2+zO2+mH2O
則反應前N的個數為2x,H為4x,O為3x
反應後N的個數為2y,H為2m,O為2z+m
根據反應前後元素種類與原子個數相等有2x=2y,4x=2m,3x=2z+m
得x=y=m/2=2z即2x=2y=m=4z
則這個化學方程式2zNH4NO3--2zN2+zO2+4zH2O
即為2NH4NO3--2N2+O2+4H2O
金屬活動性順序:
K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb>(H)>Cu>Hg>Ag>Pt>Au.
金屬活動性順序中排在越前面的金屬,活潑性越強,金屬就越容易失去最外層電子,從而金屬的金屬性(還原性)就越強。
國中化學
氧氣
(2)氧氣與化合物的反應:
(3)氧氣的來源:
15.加熱
氯酸鉀和二氧化錳混合物:
(實驗室制氧氣原理2)
植物的光合作用:6CO2+6H2O ==光/葉綠素== 6O2+C6H12O6
自然界中的水
17.水在直流電的作用下分解(研究水的組成實驗):
質量守恆定律
碳和碳氧化物
(2)煤爐中發生的三個反應:(幾個化合反應)
(3)二氧化碳的製法與性質:
30.大理石與稀鹽酸反應(實驗室制二氧化碳):
34.1.石灰水與二氧化硫反應(所以反應中有硫元素的參與,澄清石灰水就不能鑑別二氧化碳)
(4)一氧化碳的性質:
其它反應:
37.
碳酸鈉與稀鹽酸反應(化學反應式滅火器的原理):
燃料及其利用
還原方程歸總
金屬
(1)金屬與氧氣反應:
(2)金屬單質 + 酸 →鹽 + 氫氣 (
置換反應)
(3)金屬單質 + 鹽(溶液) →新金屬 + 新鹽
(4)鐵的冶煉原理:
酸鹼鹽
1、酸的化學性質
(1)酸 +金屬→ 鹽 + 氫氣(見上文)
(3)酸 + 鹼 → 鹽 + 水(中和反應)
63. 鹽酸和
氫氧化鈣反應:2HCl + Ca(OH)
2== CaCl
2+ 2H
2O
64.
氫氧化鋁藥物治療胃酸過多:3HCl + Al(OH)
3== AlCl
3+ 3H
2O
65. 硫酸和燒鹼反應:H2SO4+ 2NaOH == Na2SO4+ 2H2O
(4)酸 + 鹽 → 另一種酸 + 另一種鹽
66.大理石與稀鹽酸反應:CaCO3+ 2HCl == CaCl2+ H2O + CO2↑
67.碳酸鈉與稀鹽酸反應: Na2CO3+ 2HCl == 2NaCl + H2O + CO2↑
68.
碳酸氫鈉與稀鹽酸反應:NaHCO
3+ HCl== NaCl + H
2O + CO
2↑
69. 硫酸和
氯化鋇溶液反應:H
2SO
4+ BaCl
2== BaSO
4↓+ 2HCl
2、鹼的化學性質
70.氫氧化鈉暴露在空氣中變質:2NaOH + CO2== Na2CO3+ H2O
71.氫氧化鈉吸收二氧化硫氣體:2NaOH + SO2== Na2SO3+ H2O
72.氫氧化鈉吸收
三氧化硫氣體:2NaOH + SO
3== Na
2SO
4+ H
2O
73.氫氧化鈣放在空氣中變質:Ca(OH)2+ CO2== CaCO3↓+ H2O
74. 氫氧化鈣吸收二氧化硫:Ca(OH)2+ SO2== CaSO3↓+ H2O
(2)鹼 + 酸 → 鹽 + 水(中和反應,方程式見上)
(3)鹼 + 鹽 → 另一種鹼 + 另一種鹽
75. 氫氧化鈣與碳酸鈉:Ca(OH)2+ Na2CO3== CaCO3↓+ 2NaOH
3、鹽的化學性質
(1)鹽(溶液) + 金屬單質 → 另一種金屬 + 另一種鹽
76. 鐵和硫酸銅溶液反應:Fe + CuSO4== FeSO4+ Cu
(2)鹽 + 酸 → 另一種酸 + 另一種鹽
77.碳酸鈉與稀鹽酸反應: Na2CO3+ 2HCl == 2NaCl + H2O + CO2↑(這裡生成的碳酸直接分解了)
碳酸氫鈉與稀鹽酸反應:NaHCO3+ HCl== NaCl + H2O + CO2↑
(3)鹽 + 鹼 → 另一種鹼 + 另一種鹽
78. 氫氧化鈣與碳酸鈉:Ca(OH)2+ Na2CO3== CaCO3↓+ 2NaOH
(4)鹽 + 鹽 → 兩種新鹽
79.氯化鈉溶液和硝酸銀溶液:NaCl + AgNO3== AgCl↓ + NaNO3
80.
硫酸鈉和氯化鋇:Na
2SO
4+ BaCl
2== BaSO
4↓ + 2NaCl
高中化學
非金屬單質
| 化學方程式 | 基本反應類型 | 反應現象 | 用途 |
|---|
Cl2+H2=光照或點燃=2HCl | 化合反應 | 氫氣在氯氣中燃燒,發出蒼白色火焰,產生大量熱,有白霧生成 | 氯化氫的合成,製備鹽酸。 |
3Cl2+2P=2PCl3 | 化合反應 | 有白色煙霧生成 | — |
Cl2+PCl3=PCl5 | 化合反應 | 有白色煙霧生成 | — |
Cl2+2Na=2NaCl | 化合反應 | 有黃色火焰,放出大量熱,產生白煙。 | — |
3Cl2+2Fe=2FeCl3 | 化合反應 | 劇烈燃燒,生成棕褐色的煙。 | — |
Cl2+2FeCl2=2FeCl3 | 化合反應 | 劇烈燃燒,生成棕褐色的煙。 | — |
Cl2+Cu=CuCl2 | 化合反應 | 劇烈燃燒,生成棕黃色的煙。 | — |
Cl2+2NaBr=2NaCl+Br2 | 化合反應 | — | — |
Cl2+2NaI =2NaCl+I2 | 化合反應 | — | — |
Cl2+Na2S=2NaCl+S | 化合反應 | — | — |
Cl2+H2S=2HCl+S | 置換反應 | 剛開始有乳白色沉澱生成,隨後沉澱變成淡黃色 | — |
Cl2+SO2+2H2O=H2SO4+2HCl | 氧化還原反應 | 試管內氣體褪色,試管口有刺激性氣味氣體逸出 | — |
Cl2+H2O2=2HCl+O2 | 置換反應 | — | — |
2O2+3Fe=點燃=Fe3O4 | 化合反應 | 鐵在純氧中劇烈燃燒,火星四射,放出大量熱,生成黑色固體。 | — |
O2+K=點燃=KO2 | 化合反應 | 鉀在純氧中燃燒,有淺紫色火焰,產生黃色固體。 | |
2K+O2=K2O2 | 化合反應 | — | — |
S+H2=H2S | 化合反應 | — | — |
S+2Cu=Cu2S | 化合反應 | 加熱熔融後反應,固體變黑。 | — |
S+Zn=ZnS | 化合反應 | 加熱後劇烈反應,放出白光,產生大量熱。 | — |
N2+3H2=高壓高溫催化劑=2NH3 | 化合反應 | 有刺激性氣味氣體逸出 | 工業合成氨 |
N2+3Mg=點燃=Mg3N2 | 化合反應 | 鎂在氮氣中燃燒,發出耀眼白光,放出大量熱,產生淡黃色固體。 | — |
H2+Br2=點燃=2HBr | 化合反應 | 氫氣在溴蒸汽中點燃,放出熱量,紅棕色逐漸褪去,產生白霧。 | — |
一、非金屬單質的化學性質(F2>Cl2 >O2>S>N2>P>C>Si>H)
1、氧化性:
2F2+2H2O===4HF+O2(水是還原劑)
Cl2+H2===2HCl (將H2在Cl2點燃;混合點燃、加熱、光照發生爆炸)
Cl2+2NaBr===2NaCl+Br2Cl2+2Br=2Cl+Br2
Cl2+H2S=2HCl+S↓ (水溶液中:Cl2+H2S=2H++2Cl–+S↓
Cl2+H2O2=2HCl+O2Cl2+H2O2=2H++Cl–+O2
2O2+3Fe=Fe3O4
O2+K=KO2
S+H2=H2S
2S+C=CS2
S+Zn=ZnS
S+Fe=FeS (既能由單質製取,又能由離子製取)
S+O2==SO2
S+H2SO4(濃) ===3SO2↑+2H2O
S+6HNO3(濃)===H2SO4+6NO2↑+2H2O
3S+4HNO3(稀)===3SO2+4NO↑+2H2O
3S+4H++4NO3-==SO2+4NO↑+2H2O
C+O2(足量)===CO2
2C+O2(少量)===2CO
C+CO2=高溫==2CO
C+H2O=高溫==CO+H2(生成水煤氣)
2C+SiO2=高溫==Si+2CO(製得粗矽)
Si(粗)+2Cl2=△==SiCl4
SiCl4+2H2=高溫==Si(純)+4HCl
Si+2NaOH+H2O==Na2SiO3+2H2↑
Si+2OH-+H2O=+2H2↑
3、歧化反應
Cl2+H2O==HCl+HClO(加鹼或光照促進歧化: (Cl2+H2O=H++Cl–+HClO)
Cl2+2NaOH==NaCl+NaClO+H2O (Cl2+2OH–=Cl–+ClO–+H2O)
Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O (Cl2+2OH–=Cl–+ClO–+H2O)
3Cl2+6KOH(濃)=5KCl+KClO3+3H2O (3Cl2+6OH–=5Cl–+ClO3–+3H2O)
3S+6NaOH=2Na2S+Na2SO3+3H2O (3S+6OH–=2S2–+SO32–+3H2O)
4P+3KOH(濃)+3H2O==PH3↑+3KH2PO2(4P+3OH–+3H2O==PH3↑+3H2PO2–)
還原性:
4HCl(濃)+MnO2=MnCl2+Cl2↑+2H2O
4HCl(g)+O2=2Cl2+2H2O
16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O
14HCl+K2Cr2O7=2KCl+2CrCl3+3Cl2+7H2O
2H2O+2F2=4HF+O2
2H2S+3O2(足量)=2SO2+2H2O
2H2S+O2(少量)=2S+2H2O
2H2S+SO2=3S+2H2O
H2S+H2SO4(濃)=S↓+SO2+2H2O
3H2S+2HNO3(稀)=3S↓+2NO+4H2O
5H2S+2KMnO4+3H2SO4=2MnSO4+K2SO4+5S↓+8H2O
3H2S+K2Cr2O7+4H2SO4=Cr2(SO4)3+K2SO4+3S↓+7H2O
2 高中化學方程式小結(僅供參考)
H2S+4Na2O2+2H2O=Na2SO4+6NaOH
2NH3+3CuO=3Cu+N2+3H2O
2NH3+3Cl2=N2+6HCl
8NH3+3Cl2=N2+6NH4Cl
4NH3+3O2(純氧)=2N2+6H2O
4NH3+5O2=4NO+6H2O
4NH3+6NO=5N2+6H2O(用氨清除NO)
NaH+H2O=NaOH+H2
4NaH+TiCl=Ti+4NaCl+2H2
CaH2+2H2O=Ca(OH)2+2H2
酸性:
4HF+SiO2=SiF4 ↑+2H2O
(此反應廣泛套用於測定礦樣或鋼樣中SiO2的含量)
2HF+CaCl2=CaF2 ↓+2HCl
H2S+Fe=FeS+H2
H2S+CuCl2=CuS↓+2HCl
H2S+2AgNO3=Ag2S+2HNO3
H2S+HgCl2=HgS↓+2HCl
H2S+Pb(NO3)2=PbS↓+2HNO3
鹼性:
NH3+HCl=NH4Cl(通常檢驗NH3)
NH3+HNO3=NH4NO3
2NH3+H2SO4=(NH4)2SO4
NH3+NaCl+H2O+CO2=NaHCO3↓+NH4Cl
(此反套用於工業製備小蘇打,蘇打)
不穩定性:
2HF—X—>H2+F2(氟化氫很穩定,既不會被高錳酸鉀或二氧化錳所氧化,也不會在高溫分解)
2HCl==H2+Cl2
2H2O==2H2+O2(水在高溫可以分解)
2H2O2=2H2O+O2 ↑(制氧氣,加入催化劑即可有氧氣生成)
H2S=加熱=H2+S
2NH3=高溫,可逆=N2+3H2
非金屬氧化物
低價態的還原性:
2SO2+O2=催化劑;加熱;可逆=2SO3
2SO2+O2+2H2O=2H2SO4
(這是SO2在大氣中緩慢發生的環境化學反應)
SO2+Cl2+2H2O=H2SO4+2HCl
SO2+Br2+2H2O=H2SO4+2HBr
SO2+I2+2H2O=H2SO4+2HI
SO2+NO2=SO3+NO
2NO+O2=2NO2
NO+NO2+2NaOH=2NaNO2+H2O
(用於制硝酸工業中吸收尾氣中的NO和NO2)
2CO+O2=2CO2
CO+CuO=Cu+CO2
3CO+Fe2O3=2Fe+3CO2
CO+H2O=CO2+H2
氧化性:
SO2+2H2S=3S+2H2O
SO3+2KI=K2SO3+I2
NO2+2KI+H2O=NO+I2+2KOH
(不能用澱粉KI溶液鑑別溴蒸氣和NO2)
4NO2+H2S=4NO+SO3+H2O
2NO2+Cu=4CuO+N2
CO2+2Mg=2MgO+C
(CO2不能用於撲滅由Mg,Ca,Ba,Na,K等燃燒的火災)
SiO2+2H2=Si+2H2O
SiO2+2Mg=2MgO+Si
與水的作用:
SO2+H2O=可逆=H2SO3
SO3+H2O=H2SO4
3NO2+H2O=2HNO3+NO ↑
N2O5+H2O=2HNO3
P2O5+H2O=2HPO3
P2O5+3H2O=2H3PO4 (P2O5極易吸水,可作氣體乾燥劑)
P2O5+3H2SO4(濃)=Δ=2H3PO4+3SO3↑ (SO3是白色固體,但加熱會變成氣體)
CO2+H2O<===>H2CO3(可逆)
與鹼性物質的作用:
SO2+2NH3+H2O=(NH4)2SO3
SO2+(NH4)2SO3+H2O=2NH4HSO3
(這是硫酸廠回收SO
2的反應.先用
氨水吸收SO
2,
再用H2SO4處理: 2NH4HSO3+H2SO4=(NH4)2SO4+2H2O+2SO2
SO2+Ca(OH)2=CaSO3↓+H2O
(不能用澄清石灰水鑑別SO2和CO2.可用品紅鑑別)
SO3+MgO=MgSO4
SO3+Ca(OH)2=CaSO4+H2O
CO2+2NaOH(過量)=Na2CO3+H2O
CO2(過量)+NaOH=NaHCO3
CO2+Ca(OH)2(過量)=CaCO3↓+H2O
2CO2(過量)+Ca(OH)2=Ca(HCO3)2
CO2+2NaAlO2+3H2O=2Al(OH)3↓+Na2CO3
CO2+C6H5ONa+H2O=C6H5OH+NaHCO3
SiO2+CaO=高溫=CaSiO3
SiO2+2NaOH=Na2SiO3+H2O
SiO2+Na2CO3=高溫=Na2SiO3+CO2↑ (與制玻璃相關)
SiO2+CaCO3=高溫=CaSiO3+CO2↑(煉鐵爐渣的形成)
金屬氧化物
低價態的還原性:
6FeO+O2=△=2Fe3O4
FeO+4HNO3(濃)=Fe(NO3)3+NO2↑+2H2O
氧化性:
Na2O2+2Na=2Na2O (此反套用於製備Na2O)
MgO,Al2O3幾乎沒有氧化性,很難被還原為Mg,Al.
一般通過電解制Mg和Al.
Fe2O3+3H2=△=2Fe+3H2O (制還原鐵粉)
與水的作用:
Na2O+H2O=2NaOH
2Na2O2+2H2O=4NaOH+O2↑
(此反應分兩步:Na2O2+2H2O=2NaOH+H2O2;
2H2O2=2H2O+O2↑. H2O2的製備可利用類似的反應:
BaO2+H2SO4(冷,稀)=BaSO4+H2O2)
MgO+H2O(沸水)=Mg(OH)2(緩慢反應)
與酸性物質的作用:
Na2O+SO3=Na2SO4
Na2O+CO2=Na2CO3
Na2O+2HCl=2NaCl+H2O
2Na2O2+2CO2=2Na2CO3+O2
Na2O2+H2SO4(冷,稀)=Na2SO4+H2O2
MgO+SO3=MgSO4
MgO+H2SO4=MgSO4+H2O
Al2O3+3H2SO4=Al2(SO4)3+3H2O
(Al
2O
3是
兩性氧化物:Al
2O
3+2NaOH=2NaAlO
2+H
2O)
FeO+2HCl=FeCl2+3H2O
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2S(g)=Fe2S3+3H2O
Fe3O4+8HCl=FeCl2+2FeCl3+4H2O
含氧酸
氧化性:(與金屬反應時:酸性+氧化性;與非金屬時:氧化性)
4HClO3+3H2S=3H2SO4+4HCl
HClO3+HI=HIO3+HCl
3HClO+HI=HIO3+3HCl
HClO+H2SO3=H2SO4+HCl
HClO+H2O2=HCl+H2O+O2↑(氧化性:HClO>HClO2>HClO3>HClO4,但濃,熱的HClO4氧化性很強)
2H2SO4(濃)+C=△=CO2↑+2SO2↑+2H2O
2H2SO4(濃)+S=△=3SO2↑+2H2O
6H2SO4(濃)+2Fe=△=Fe2(SO4)3+3SO2↑+6H2O
6H2SO4(濃)+2Al=△=Al2(SO4)3+3SO2↑+6H2O (濃H2SO4中Fe、Al室溫下鈍化)
2H2SO4(濃)+Cu=△=CuSO4+SO2↑+2H2O
H2SO4(濃)+2HBr=△=SO2↑+Br2+2H2O
H2SO4(濃)+2HI=△=SO2↑+I2+2H2O (HX(X=Br,I)製備用濃磷酸,難揮發酸制易揮發酸)
H2SO4(稀)+Fe=FeSO4+H2↑
H2SO3+2H2S=3S↓+3H2O
4HNO3(濃)+C=△=CO2+4NO2↑+2H2O
6HNO3(濃)+S=△=H2SO4+6NO2↑+2H2O
5HNO3(濃)+P=△=H3PO4+5NO2↑+H2O
6HNO3(濃)+Al=△=Al(NO3)3+3NO2↑+3H2O
6HNO3(濃)+Fe=△=Fe(NO3)3+3NO2↑+3H2O (Al、Fe與濃硝酸常溫鈍化)
4HNO3(稀)+Fe=Fe(NO3)3+NO↑+2H2O (Fe少量)
8HNO3(稀)+3Fe=3Fe(NO3)2+2NO↑+4H2O(Fe過量)
30HNO3+8Zn=8Zn(NO3)3+3N2O↑+15H2O
30HNO3+8Zn=8Zn(NO3)3+3NH4NO3+9H2O
36HNO3+10Zn=10Zn(NO3)3+3N2↑+18H2O
還原性:
H2SO3+X2+H2O=H2SO4+2HX (X表示Cl2,Br2,I2)
2H2SO3+O2=2H2SO4
H2SO3+H2O2=H2SO4+H2O
5H2SO3+2KMnO4=2MnSO4+K2SO4+2H2SO4+3H2O
H2SO3+2FeCl3+H2O=H2SO4+2FeCl2+2HCl
酸性:
H2SO4(濃) +CaF2=△=CaSO4+2HF ↑
H2SO4(濃)+NaCl=△=NaHSO4+HCl ↑
H2SO4(濃)+NaNO3=NaHSO4+HNO3
3H2SO4(濃)+Ca3(PO4)2=CaSO4+2H3PO4
2H2SO4(濃)+Ca3(PO4)2=2CaSO4+Ca(H2PO4)2
3HNO3+Ag3PO4=H3PO4+3AgNO3
2HNO3+CaCO3=Ca(NO3)2+H2O+CO2↑
(用HNO3和濃H2SO4不能製備H2S,HI,HBr,(SO2)等還原性氣體)
4H3PO4+Ca3(PO4)2=3Ca(H2PO4)2(重鈣)
H3PO4(濃)+NaBr=△=NaH2PO4+HBr↑
H3PO4(濃)+NaI=△=NaH2PO4+HI↑
不穩定性:
2HClO=光照=2HCl+O2↑ (氯水現配現用)
4HNO3=光照或△=4NO2↑+O2↑+2H2O (濃硝酸呈黃色原因,保存在棕色瓶中)
H2SO3=H2O+SO2↑
H2CO3=H2O+CO2↑
H4SiO4=H2SiO3↓+H2O
鹼
低價態的還原性:
4Fe(OH)2+O2+2H2O=4Fe(OH)3
與酸性物質的作用:
2NaOH+SO2(足量)=Na2SO3+H2O
NaOH+SO2(少量)=NaHSO3
NaOH+H2S(少量)=NaHS+H2O
2NaOH+H2S(足量)=Na2S+2H2O
2NaOH+SiO2=Na2SiO3+H2O (NaOH不用磨口玻璃瓶,鹼式滴定管用橡膠管)
2NaOH+Cl2=NaCl+NaClO+H2O (制漂白液[84消毒液])
NaOH+HCl=NaCl+H2O
2NaOH+Al2O3=2NaAlO2+H2O
3NaOH+AlCl3=Al(OH)3↓+3NaCl
NaOH+Al(OH)3=NaAlO2+2H2O(酸性:AlCl3>Al(OH)3)
4NaOH+AlCl3=NaAlO2+3NaCl
NaOH+NH4Cl=NaCl+NH3*H2O
NaOH+NH4Cl=△=NaCl+NH3↑+H2O
Mg(OH)2+2NH4Cl=MgCl2+2NH3.H2O
Ca(OH)2(s)+2NH4Cl=△=CaCl2+2NH3↑+2H2O (實驗室制NH3)
不穩定性:
Mg(OH)2=△=MgO+H2O
2Al(OH)3=△=Al2O3+3H2O
2Fe(OH)3=△=Fe2O3+3H2O
Cu(OH)2=△=CuO+H2O
通式:2MOH=△=M2O+H2O(M指不活潑金屬)
鹽
氧化性:
2FeCl3+Fe=3FeCl2
2FeCl3+Cu=2FeCl2+CuCl2(用於雕刻銅線路版)
2FeCl3+Zn=2FeCl2+ZnCl2
FeCl3+Ag=FeCl2+AgCl
Fe2(SO4)3+2Ag=2FeSO4+Ag2SO4(反應很慢)
Fe(NO3)3與Ag不反應。氧化性銀離子略>鐵離子,氯離子、硫酸根離子與銀形成難溶物,增強了銀的還原性
2FeCl3+H2S=2FeCl2+2HCl+S ↓
2FeCl3+2KI=2FeCl2+2KCl+I2
FeCl2+Mg=Fe+MgCl2
還原性:
2FeCl2+Cl2=2FeCl3
SnCl2+Cl2=SnCl4(SnCl2有強還原性)
3Na2S+8HNO3(稀)=6NaNO3+2NO↑+3S↓ +4H2O
3Na2SO3+2HNO3(稀)=3Na2SO4+2NO↑+H2O
2Na2SO3+O2=2Na2SO4
與鹼性物質的作用:
MgCl2+2NH3.H2O=Mg(OH)2↓ +NH4Cl
AlCl3+3NH3.H2O=Al(OH)3↓ +3NH4Cl
FeCl3+3NH3.H2O=Fe(OH)3↓ +3NH4Cl
與酸性物質的作用:
Na3PO4+HCl=Na2HPO4+NaCl
Na2HPO4+HCl=NaH2PO4+NaCl
NaH2PO4+HCl=H3PO4+NaCl
Na2CO3+HCl=NaHCO3+NaCl
NaHCO3+HCl=NaCl+H2O+CO2↑
3Na2CO3+2AlCl3+3H2O=2Al(OH)3↓ +3CO2↑+6NaCl
3Na2CO3+2FeCl3+3H2O=2Fe(OH)3↓ +3CO2↑+6NaCl
3NaHCO3+AlCl3=Al(OH)3↓ +3CO2↑
3NaHCO3+FeCl3=Fe(OH)3↓ +3CO2↑
3Na2S+Al2(SO4)3+6H2O=2Al(OH)3↓ +3H2S ↑
3NaAlO2+AlCl3+6H2O=4Al(OH)3↓ +3NaCl
不穩定性:
Na2S2O3+2H+=2Na++S+SO2↑+H2O
NH4HCO3=NH3↑+H2O↑+CO2↑
2KNO3=△=2KNO2+O2↑
2Cu(NO3)2=△=2CuO+4NO2↑+O2↑
2KMnO4=△=K2MnO4+MnO2+O2↑ (用於實驗室製備氧氣)
2KClO3=MnO2 △=2KCl+3O2↑
2NaHCO3=△=Na2CO3+H2O+CO2↑
Ca(HCO3)2=CaCO3↓+H2O+CO2↑
CaCO3=高溫=CaO+CO2↑
MgCO3=△=MgO+CO2↑
H2SO3=H2O+SO2↑
2ClO2=加熱或震盪=Cl2+2O2 (二氧化氯不穩定,會爆炸性分解)
2BaO2=△=2BaO+O2↑ (過氧化鋇能在700℃分解)
氧化還原
1、木炭還原氧化銅: 2CuO + C= 高溫= 2Cu + CO2↑
2、鈉在空氣中燃燒:2Na + O2 =△=Na2O2 鈉與氧氣反應:4Na + O2= 2Na2O
3、過氧化鈉與二氧化碳:2Na2O2+ 2CO2= 2Na2CO3+ O2
離子反應
1、硫酸根的檢驗: BaCl2+ Na2SO4 = BaSO4↓+ 2NaCl
2、碳酸根的檢驗: CaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
3、碳酸鈉與鹽酸: Na2CO3+ 2HCl = 2NaCl + H2O + CO2↑
5、鐵片與硫酸銅溶液: Fe + CuSO4= FeSO4+ Cu
6、
氯化鈣與碳酸鈉溶液:CaCl
2+ Na
2CO
3= CaCO
3↓+ 2NaCl
8、
過氧化鈉與水:2Na
2O
2+ 2H
2O = 4NaOH + O
2↑
10、鈉與水:2Na + 2H2O = 2NaOH + H2↑
11、鐵與水蒸氣:3Fe + 4H2O(g) = Fe3O4 + 4H2↑
12、鋁與氫氧化鈉溶液:2Al + 2NaOH + 2H2O = 2NaAlO2+ 3H2↑
13、氧化鈣與水:CaO + H2O = Ca(OH)2
14、氧化鐵與鹽酸:Fe2O3+ 6HCl = 2FeCl3+ 3H2O
15、氧化鋁與鹽酸:Al2O3+ 6HCl = 2AlCl3+ 3H2O
16、氧化鋁與氫氧化鈉溶液:Al2O3+ 2NaOH = 2NaAlO2+ H2O
17、
氯化鐵與氫氧化鈉溶液:FeCl
3+ 3NaOH = Fe(OH)
3↓+ 3NaCl
18、硫酸亞鐵與氫氧化鈉溶液:FeSO4+ 2NaOH = Fe(OH)2↓+ Na2SO4
19、氫氧化亞鐵氧化成
氫氧化鐵:4Fe(OH)
2+ 2H
2O + O
2= 4Fe(OH)
320、氫氧化鐵分解:2Fe(OH)3=△=Fe2O3+ 3H2O↑
21、實驗室製取氫氧化鋁:Al2(SO4)3+ 6NH3.H2O = 2Al(OH)3↓ + 3(NH4)2SO4
22、
氫氧化鋁與鹽酸:Al(OH)
3+ 3HCl = AlCl
3+ 3H
2O
23、氫氧化鋁與過量氫氧化鈉溶液:Al(OH)3+ NaOH = NaAlO2+ 2H2O
24、氫氧化鋁分解:2Al(OH)3=△= Al2O3+ 3H2O
25、三氯化鐵溶液與鐵粉:2FeCl3+ Fe = 3FeCl2
26、氯化亞鐵中通入
氯氣:2FeCl
2+ Cl
2= 2FeCl
327、
二氧化矽與氫氟酸:SiO
2+ 4HF = SiF
4+ 2H
2O 矽單質與氫氟酸反應:Si + 4HF = SiF
4+ 2H
2↑
28、二氧化矽與氧化鈣高溫:SiO2 + CaO =高溫= CaSiO3
29、二氧化矽與氫氧化鈉溶液:SiO2+ 2NaOH = Na2SiO3+ H2O
30、
矽酸鈉溶液中通入少量二氧化碳:Na
2SiO
3+ CO
2+ H
2O = Na
2CO
3+ H
2SiO
3↓
31、矽酸鈉與鹽酸:Na2SiO3+ 2HCl = 2NaCl + H2SiO3↓
32、氯氣與鐵:2Fe + 3Cl2=點燃=2FeCl3
33、氯氣與銅:Cu + Cl2=點燃= CuCl2
34、氯氣與鈉:2Na + Cl2=點燃=2NaCl
35、氯氣與水:Cl2+ H2O⇌HCl + HClO
36、
次氯酸光照分解:2HClO =光照= 2HCl + O
2↑
37、氯氣與氫氧化鈉溶液:Cl2+ 2NaOH = NaCl + NaClO + H2O
38、氯氣與氫氧化鈣:2Cl2+ 2Ca(OH)2= CaCl2+ Ca(ClO)2+ 2H2O
39、鹽酸與硝酸銀溶液:HCl + AgNO3= AgCl↓ + HNO3
41、二氧化硫與水:SO2+ H2O⇌H2SO3
42、
氮氣與氧氣在放電下:N
2+ O
2=放電= 2NO
43、
一氧化氮與氧氣:2NO + O
2= 2NO
244、
二氧化氮與水:3NO
2+ H
2O = 2HNO
3+ NO
45、二氧化硫與氧氣在催化劑的作用下:2SO2+ O2=催化劑=2SO3
46、三氧化硫與水:SO3+ H2O = H2SO4
47、
濃硫酸與銅:Cu + 2H
2SO
4(濃) =△=CuSO
4+ 2H
2O + SO
2↑
48、濃硫酸與木炭:C + 2H2SO4(濃) =△=CO2↑+ 2SO2↑ + 2H2O
49、濃硝酸與銅:Cu + 4HNO3(濃) = Cu(NO3)2 + 2H2O + 2NO2↑
50、稀硝酸與銅:3Cu + 8HNO3(稀) = 3Cu(NO3)2+ 4H2O + 2NO↑
51、氨水分解:NH3.H2O =△= NH3↑ + H2O
52、
氨氣與
氯化氫:NH
3+ HCl = NH
4Cl
53、
氯化銨分解:NH
4Cl =△= NH
3↑ + HCl↑
54、碳酸氫氨分解:NH4HCO3=△= NH3↑ + H2O↑ + CO2↑
55、
硝酸銨與氫氧化鈉:NH
4NO
3+ NaOH =△= NH
3↑ + NaNO
3+ H
2O
56、氨氣的實驗室製取:2NH4Cl + Ca(OH)2=△= CaCl2+ 2H2O + 2NH3↑
57、氯氣與氫氣:Cl2+ H2=點燃= 2HCl
58、硫酸銨與氫氧化鈉:(NH4)2SO4+ 2NaOH =△=2NH3↑ + Na2SO4+ 2H2O
59、二氧化硫與氧化鈣:SO2+ CaO = CaSO3
記憶方法
掌握化學方程式的書寫要領
左寫反應物,右邊寫生成,寫對化學式,係數來配平,中間連等號,條件要注清,生成沉澱氣,箭頭來標明。
歸類記憶
根據知識系列或反應類型或物質類別記憶,使零散的知識通過歸納成為有規律可循、以重點物質為中心的知識網路。
聯繫實驗現象記憶
化學方程式枯燥難記,如何使化學用語的學習有聲有色、興趣盎然,可聯繫實驗現象記憶。如硫在氧氣中燃燒,記憶聯想:燃硫入氧,燃燒變旺,火焰藍紫,美麗漂亮,產生氣體,可真夠“嗆”。磷在氧氣中燃燒,記憶聯想:紅磷燃燒,可真熱鬧,濃煙滾滾,亮似“燈泡”。
 史上第一條化學方程式 Jean Beguin 1615年
史上第一條化學方程式 Jean Beguin 1615年







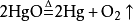





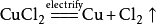






 合成酚酞
合成酚酞