二氧化氮(nitrogen dioxide),化學式NO2。高溫下棕紅色有毒氣體。在常溫下(0~21.5℃)二氧化氮與四氧化二氮混合而共存。有毒。有刺激性。溶於濃硝酸中而生成發煙硝酸。能疊合成四氧化二氮。與水作用生成硝酸和一氧化氮。與鹼作用生成硝酸鹽。能與許多有機化合物起激烈反應。二氧化氮在臭氧的形成過程中起著重要作用。人為產生的二氧化氮主要來自高溫燃燒過程的釋放,比如機動車尾氣、鍋爐廢氣的排放等。 二氧化氮還是酸雨的成因之一,所帶來的環境效應多種多樣,包括:對濕地和陸生植物物種之間競爭與組成變化的影響,大氣能見度的降低,地表水的酸化、富營養化(由於水中富含氮、磷等營養物藻類大量繁殖而導致缺氧)以及增加水體中有害於魚類和其它水生生物的毒素含量。
基本介紹
- 中文名:二氧化氮
- 英文名:nitrogen dioxide
- 別稱:過氧化氮
- 化學式:NO2
- 分子量:46.01
- CAS登錄號:10102-44-0
- EINECS登錄號:233-272-6
- 熔點:−11 ℃(lit.)
- 沸點:21 ℃(lit.)
- 水溶性:易溶於水
- 密度:2.05 g/L 在 25 ℃(lit.)
- 外觀:室溫下為 有刺激性氣味的紅棕色氣體
- 閃點:無意義
- 套用:製備硝酸;用作氧化劑
- 安全性描述:是一種重要的大氣污染物
- 危險性符號:R:R26-R34
- 危險性描述:二氧化氮吸入後對肺組織具有強烈的刺激性和腐蝕性,出現肺水腫。
- 危險品運輸編號:23012
- 安全術語:S1/2-S9-S26-S28-S36/37/39-S45
- 發現者:約瑟夫·普雷斯特利
- 聯合國編號:1067
- 安全包裝方法:鋼質氣瓶
- 主要用途:用於制硝酸、硝化劑、氧化劑等。
分子結構,物理性質,性質與穩定性,化學性質,自身的化合,和水的反應,氧化性,主要用途,危險性,健康危害,毒理學資料及環境行為,應急處理方法,急救措施,防護措施,泄漏處理,消防措施,處置儲存,接觸防護,毒理學,生態學,廢棄處置,運輸信息,法規信息,來源,實驗製法,製取方法,收集方式,尾氣處理,常見謠言,
分子結構
判斷NO2分子的結構
在NO2分子中,N周圍的價電子數為5,根據價層電子對互斥理論(VSEPR理論),氧原子不提供電子,因此,中心氮原子的價電子總數為5,相當於三對電子對.。其中有兩對是成鍵電子對,一個成單電子當作一對孤電子對。氮原子價層電子對排布應為平面三角形。所以NO2分子的結構為V字形,O-N-O鍵角約為120度。
物理性質
外觀與性狀:黃褐色液體或棕紅色氣體,其固體呈無色,有刺激性氣味。
相對密度(水=1):1.45
相對蒸氣密度(空氣=1):3.2
飽和蒸氣壓(kPa):101.32(22℃)
臨界溫度(℃):158
臨界壓力(MPa):10.13
性質與穩定性
當溫度高於150℃時開始分解,到650℃時完全分解為一氧化氮和氧氣。與水反應生成硝酸和一氧化氮;與濃硫酸反應生成亞硝基硫酸,與鹼反應生成等摩爾硝酸鹽和亞硝酸鹽。二氧化氮在氣相狀態下有疊合作用,生成四氧化二氮,它總是與四氧化二氮在一起呈平衡狀態存在。
化學性質
二氧化氮 (NO2)在21.1℃溫度時為棕紅色刺鼻氣體。常溫下化學性質較穩定。
自身的化合
二氧化氮加壓時很容易聚合。通常情況下與其二聚體形式——四氧化二氮(無色抗磁性氣體)混合存在,構成一種平衡態混合物:二氧化氮轉化成四氧化二氮放熱。升高溫度,平衡向二氧化氮生成的方向移動;降低溫度,平衡向四氧化二氮生成的方向移動。 二氧化氮和四氧化二氮
二氧化氮和四氧化二氮
 二氧化氮和四氧化二氮
二氧化氮和四氧化二氮
和水的反應
二氧化氮溶於水並與水反應生成硝酸或硝酸和一氧化氮。但二氧化氮溶於水後並不會完全反應所以會有少量二氧化氮分子存在,為黃色。由於硝酸同時會分解,所以可以看作可逆反應。因二氧化氮溶於水後還生成一氧化氮,所以不是硝酸的酸酐。


二氧化氮可以直接被過氧化鈉吸收,生成硝酸鈉:
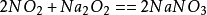
其他複分解反應
也可以被氫氧化鈉吸收(發生的是歧化反應):



氧化性
二氧化氮中氮元素化合價為+4,有氧化性。
二氧化氮可以和氧氣一樣支持某些金屬和非金屬的燃燒:(現象:固體在紅棕色氣體中繼續燃燒,發出耀眼的光芒,氣體的紅棕色逐漸褪去)


例如與氨氣反應:

主要用途
危險性
健康危害
侵入途徑:吸入。
健康危害:氮氧化物主要損害呼吸道。吸入初期僅有輕微的眼及上呼吸道刺激症狀,如咽部不適、乾咳等。常數小時至十幾小時或更長時間潛伏期後發生遲發性肺水腫、成人呼吸窘迫綜合徵,出現胸悶、呼吸窘迫、咳嗽、咯泡沫痰、紫紺等。可並發氣胸及縱隔氣腫。肺水腫消退後兩周左右可出現遲發性阻塞性細支氣管炎。
慢性影響:主要表現為神經衰弱綜合徵及慢性呼吸道炎證。個別病例出現肺纖維化。可引起牙齒酸蝕症。
健康危害:氮氧化物主要損害呼吸道。吸入初期僅有輕微的眼及上呼吸道刺激症狀,如咽部不適、乾咳等。常數小時至十幾小時或更長時間潛伏期後發生遲發性肺水腫、成人呼吸窘迫綜合徵,出現胸悶、呼吸窘迫、咳嗽、咯泡沫痰、紫紺等。可並發氣胸及縱隔氣腫。肺水腫消退後兩周左右可出現遲發性阻塞性細支氣管炎。
慢性影響:主要表現為神經衰弱綜合徵及慢性呼吸道炎證。個別病例出現肺纖維化。可引起牙齒酸蝕症。
毒理學資料及環境行為
 各類含氧氮化合物的構型
各類含氧氮化合物的構型急性毒性:LC50126mg/m3,4小時(大鼠吸入)
致突變性:微生物致突變:鼠傷寒沙門氏菌6ppm。哺乳動物體細胞突變:大鼠吸入15ppm(3小時),連續。
生殖毒性:大鼠吸入最低中毒濃度(TCL0):8.5µg/m3,24小時(孕1-22天),引起胚胎毒性和死胎。
致突變性:微生物致突變:鼠傷寒沙門氏菌6ppm。哺乳動物體細胞突變:大鼠吸入15ppm(3小時),連續。
生殖毒性:大鼠吸入最低中毒濃度(TCL0):8.5µg/m3,24小時(孕1-22天),引起胚胎毒性和死胎。
危險特性:本品不燃燒,但可助燃。具有強氧化性,遇衣物、鋸末、棉花或其它可燃物能立即燃燒。與一般燃料或火箭燃料以及氯代烴等猛烈反應引起爆炸。遇水有腐蝕性,腐蝕作用隨水分含量增加而加劇。
燃燒(分解)產物:氮氧化物。
燃燒(分解)產物:氮氧化物。
應急處理方法
急救措施
皮膚接觸:脫去污染的衣著,用流動清水沖洗。
眼睛接觸:立即提起眼瞼,用流動清水沖洗。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。就醫。
食入:飲足量溫水,催吐,就醫。
眼睛接觸:立即提起眼瞼,用流動清水沖洗。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。就醫。
食入:飲足量溫水,催吐,就醫。
防護措施
呼吸系統防護:空氣中濃度超標時,佩戴自吸過濾式防毒面具(全面罩)。緊急事態搶救或撤離時,建議佩戴空氣呼吸器。
眼睛防護:呼吸系統防護中已作防護。
身體防護:穿膠布防毒衣。
手防護:戴橡膠手套。
其它:工作現場禁止吸菸、進食和飲水。保持良好的衛生習慣。進入罐、限制性空間或其它高濃度區作業,須有人監護。
眼睛防護:呼吸系統防護中已作防護。
身體防護:穿膠布防毒衣。
手防護:戴橡膠手套。
其它:工作現場禁止吸菸、進食和飲水。保持良好的衛生習慣。進入罐、限制性空間或其它高濃度區作業,須有人監護。
泄漏處理
迅速撤離泄漏污染區人員至上風處,並進行隔離,嚴格限制出入。建議應急處理人員戴自給正壓式呼吸器,穿防毒服。儘可能切斷泄漏源。若是氣體,合理通風,加速擴散。噴霧狀水稀釋、溶解。構築圍堤或挖坑收容產生的大量廢水。漏氣容器要妥善處理,修復、檢驗後再用。若是液體,用大量水沖洗,洗水稀釋後放入廢水系統。若大量泄漏,構築圍堤或挖坑收容;噴霧狀水冷卻和稀釋蒸氣。用防爆泵轉移至槽車或專用收集器內,回收或運至廢物處理場所處置。
消防措施
滅火方法:本品不燃。消防人員必須佩戴過濾式防毒面具(全面罩)或隔離式呼吸器、穿全身防火防毒服。在上風處滅火。切斷氣源。噴水冷卻容器,可能的話將容器從火場移至空曠處。滅火劑:乾粉、二氧化碳、禁止用水、鹵代烴滅火劑滅火。
處置儲存
操作注意事項:嚴加密閉,提供充分的局部排風和全面通風。操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴自吸過濾式防毒面具(全面罩),穿膠布防毒衣,戴橡膠手套。遠離火種、熱源,工作場所嚴禁吸菸。遠離易燃、可燃物。防止氣體或蒸氣泄漏到工作場所空氣中。避免與還原劑接觸。搬運時輕裝輕卸,防止鋼瓶及附屬檔案破損。配備相應品種和數量的消防器材及泄漏應急處理設備。
儲存注意事項:儲存於陰涼、通風的庫房。遠離火種、熱源。庫溫不宜超過15℃。應與易(可)燃物、還原劑、食用化學品分開存放,切忌混儲。儲區應備有泄漏應急處理設備。
接觸防護
職業接觸限值
中國MAC(mg/m3):5[NO2]
前蘇聯MAC(mg/m3):2
TLVTN:ACGIH 3ppm,5.6mg/m3
TLVWN:ACGIH 5ppm,9.4mg/m3
監測方法:鹽酸萘乙二胺比色法
工程控制:嚴加密閉,提供充分的局部排風和全面通風。提供安全淋浴和洗眼設備。
呼吸系統防護:空氣中濃度超標時,佩戴自吸過濾式防毒面具(全面罩)。緊急事態搶救或撤離時,建議佩戴空氣呼吸器。
眼睛防護:呼吸系統防護中已作防護。
身體防護:穿膠布防毒衣。
手防護:戴橡膠手套。
其他防護:工作現場禁止吸菸、進食和飲水。保持良好的衛生習慣。進入罐、限制性空間或其它高濃度區作業,須有人監護。
毒理學
吸入- 大鼠 LC50: 88 PPM/4h; 吸入- 小鼠 LC50: 1000 PPM/10min
生態學
其它有害作用:該物質對環境有危害,應特別注意對地表水、土壤、大氣和飲用水的污染。
廢棄處置
廢棄處置方法:根據國家和地方有關法規的要求處置。或與廠商或製造商聯繫,確定處置方法。
運輸信息
危險貨物編號:23012
UN編號:1067
包裝類別:O52
包裝方法:鋼質氣瓶。
運輸注意事項:採用鋼瓶運輸時必須戴好鋼瓶上的安全帽。鋼瓶一般平放,並應將瓶口朝同一方向,不可交叉;高度不得超過車輛的防護欄板,並用三角木墊卡牢,防止滾動。嚴禁與易燃物或可燃物、還原劑、食用化學品等混裝混運。夏季應早晚運輸,防止日光曝曬。公路運輸時要按規定路線行駛,禁止在居民區和人口稠密區停留。鐵路運輸時要禁止溜放。
法規信息
法規信息 化學危險物品安全管理條例(1987年2月17日國務院發布),化學危險物品安全管理條例實施細則 (化勞發[1992] 677號),工作場所安全使用化學品規定 ([1996]勞部發423號)等法規,針對化學危險品的安全使用、生產、儲存、運輸、裝卸等方面均作了相應規定;常用危險化學品的分類及標誌 (GB 13690-92)將該物質劃為第2.3 類有毒氣體;劇毒物品分級、分類與品名編號(GA 57-93)中,該物質的液化或壓縮品被劃為第一類 A級無機劇毒品。
危險化學品重大危險源辨識(GB18218-2009)中,該物質的臨界量為1噸,滿1噸即成為重大危險源。
來源
另外閃電也可以產生NO2,在閃電時由於空氣中電場極強,空氣中的一些物質的分子被撕裂而導電,雷電電流通過時產生大量的熱,使已經呈游離狀態的空氣成分N2、O2結合。
N2+O2==放電或高溫==2NO,NO進一步與空氣中O2反應,生成NO2 2NO+O2===2NO2,NO2與雲結合成HNO3,3NO2+H2O=2HNO3+NO,與雨水一起落下,進入土壤中,溶解一些岩石中的礦物質成為硝酸鹽,變成天然氮肥。
實驗製法
製取方法
實驗室通常用不活潑金屬與濃硝酸反應:

收集方式
向上排空氣法(由於二氧化氮易溶於水,故不可用排水法進行收集。)
尾氣處理
通入氫氧化鈉溶液即可快速吸收。
常見謠言
謠言:把少量NO2氣體通入過量小蘇打溶液中,再使溢出的氣體通過裝有足量的過氧化鈉顆粒的乾燥管,最後收集到的氣體是A.氧氣B.二氧化氮C.二氧化氮和氧氣D.二氧化氮和一氧化氮
駁斥:這種所謂習題存在根本性的科學錯誤,NO、NO2均能與Na2O2直接反應而不會有殘留,因此不可能出現通過過氧化鈉充分吸收後殘留一氧化氮或二氧化氮的情況,只可能殘留氧氣O2,然而又因為存在如下反應
2NO+O2=2NO2(注意這與過氧化鈉直接吸收NO的反應互相競爭,總反應可以看成2NO+O2+Na2O2=2NaNO3),形成的二氧化氮又可以被過氧化鈉繼續吸收。所以實際上的情況是氣體全部被吸收或者只剩餘氧氣,並且由於兩個反應競爭性的進行,無法進行定量分析與討論。

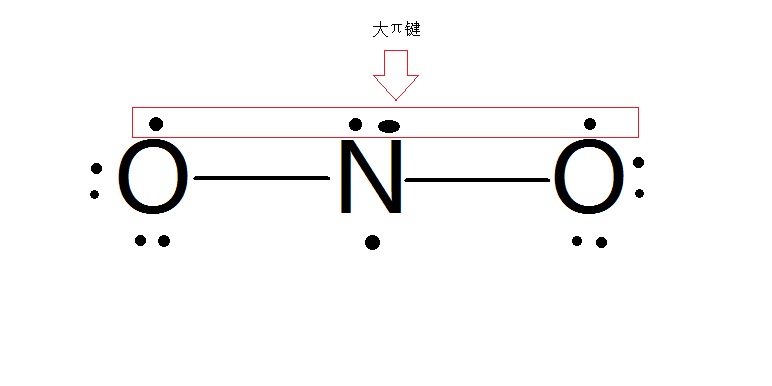 二氧化氮分子結構
二氧化氮分子結構