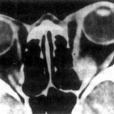
病因病理
發病機理尚未完全闡明,和自身免疫因素有關。近年的研究進展有以下幾方面:
(一)體液免疫突眼症 一般認為系自身免疫性疾病,眼部可能與甲狀腺存有共同的
抗原決定簇,TSH受體抗原、甲狀腺球蛋白-抗甲狀腺球蛋白抗體免疫複合物、抗某些細菌及病毒等外來抗原的抗體等可能參與發病。最近有資料支持眼窩組織記憶體有臟器特異性抗原,屬獨立的臟器特異性自身免疫性疾病。內分泌浸潤性突眼症的血清中已檢出眼外肌的64kDa蛋白及其特異性抗體,推測該種蛋白與突眼症發病有關。
(二)細胞免疫 對患者的眼外肌內浸潤的T細胞的研究表明,該種T細胞有認別眼外肌抗原的功能,能刺激T
細胞增殖和產生移動抑制因子。約有半數患者存有抗體依賴性細胞介導細胞毒作用(ADCC)。突眼症患者NK活性多低下,故自身抗體生成亢進。
(三)球後成纖維細胞的作用 IGF-I和成纖維細胞生成因子(FGF)有刺激成纖維細胞作用。免疫組化染色證明眼外肌、
脂肪細胞、炎症浸潤細胞中存有IGF-I,考慮與發病有關。成纖維細胞活性增強與突眼有密切關係,使粘多糖、膠元、糖蛋白分泌增多,特別是粘多糖有較強的吸水性,進而使脂肪組織、眼外肌間質水腫。
綜上所述,突眼的發病是細胞免疫和體液免疫聯合作用的結果。
臨床表現
浸潤性突眼起病可急可緩,可伴有或不伴有高代謝症群,症狀出現可先於高代謝症群,也可在其之後,病情多為中度或重度,呈進行性雙側或單側突眼,與良性突眼不同,突眼度多在19~20mm以上伴下列多種症狀:眶內、眶周組織充血、眼瞼水腫,伴有眼球脹痛、畏光、流淚、視力減退、眼肌麻痹、眼球轉動受限,伴斜視、復視,嚴重時球結膜膨出、紅腫而易感染;由於眼瞼收縮、
眼球突出,眼瞼不能閉合,角膜常多暴露,引起角膜乾燥,發生炎症,繼之潰瘍,並可繼發感染,甚至角膜穿孔而失明。角膜受累可輕可重,輕者僅有角膜炎狀改變,中度者發生角膜炎與潰瘍,嚴重者角膜混濁、壞死、穿孔,少數病人由於眶內壓力增高,影響了視神經的血流供應,而引起一側或雙側視神經乳頭水腫、視神經炎或球後神經炎,甚至視神經萎縮,視力喪失;部分患者可伴有局限性
粘液性水腫皮損,以脛前發病較多;伴有或不伴有高代謝症群及甲狀腺瀰漫性腫大;突眼程度與甲亢輕重不平行。少數病例突眼不著而以單側或雙側眼肌麻痹表現出現或伴有杵狀指(趾)及
骨關節病。
促使突眼加重的因素有:
①甲亢控制過快,抗甲狀腺藥物用量過大,又未合用
甲狀腺片。
②甲亢控制已過頭,發生了甲減。因此,為了避免突眼加重,抗甲狀腺藥物不宜用量過大,應及時加用適量乾甲狀腺片,並防止甲減發生。
③手術治療或同位素治療後,可能和甲狀腺受損、抗原釋放增多有關,如果發生甲減也可加重突眼。因此對明顯的突眼患者,手術或同位素治療宜慎重。
內分泌突眼由起病到病情穩定、緩解,一般病程1~2年,也有延長至5年者。病情緩解後,眼部充血、腫脹現象逐漸減輕或消失,症狀改善,病人的眼部不適感減輕,但眼睛很少能恢復正常,一般仍留下某種程度的眼瞼收縮、肥厚、眼球突出,眼外肌纖維化。
單側突眼,尤其無明顯甲亢者診斷時應注意除外眶內或
顱內腫瘤,以及某些局部病變引起之突眼如球後出血、海綿竇或眼靜脈血栓形成等。
T3抑制試驗在後者示正常抑制,而在本病則不受抑制。
TRH興奮試驗在眶內或顱內腫瘤者示正常興奮曲線,而在本病示低平曲線,故T3抑制試驗及TRH試驗在本病中具有診斷意義。此外,眼底檢查、頭顱、眶內X線攝片、CT,MR檢查及甲狀腺抗體如TSI,TBII測定也有助於鑑別。
治療
突眼嚴重者不宜行甲狀腺手術治療,採用放射性131碘治療也須慎重。伴有高代謝症群者,用小劑量抗甲狀腺藥物緩慢地控制甲亢輔以其他治突眼的方法是比較安全可取的措施,但有時也可導致突眼惡化,故在療程中必須隨時觀察,防止其發展。
(一)局部治療 注意眼睛休息、戴黑色或茶色眼鏡避免強光及各種外來刺激,睡眠時用抗菌眼膏並戴眼罩,以免角膜暴露部分受刺激而發生炎症。用單側眼罩減輕復視,高枕臥位,控制食鹽攝入,抗菌眼藥水(膏)及可的松眼藥水交替使用。0.5%~1%
甲基纖維素或0.5%氫化可的松溶液對減輕眼睛刺激症狀效果較好。球後
透明質酸酶注射療效較差。眶內肌肉圓錐注射甲基強的松龍可能有效。有嚴重突眼甚至結膜水泡樣膨出如金魚眼者宜迅速行眼瞼側面縫合術,對保護角膜是較為有效的方法,待突眼好轉後再行拆除縫線,但瞼緣合處可
繼發感染,遺留疤痕形成鋸齒樣瞼緣。突眼嚴重及視力受到威脅經局部和全身治療無效時可採用各種眶內減壓術,但國內少用。
(二)全身治療
乾甲狀腺製劑 用於甲亢治程中及伴有明顯突眼者,每日口服30~60mg,直至見效,劑量遞減,維持1~3年。
免疫抑制劑 如
糖皮質激素、
環磷醯胺、CB1348等的套用。突眼初期三個月套用療效較好。嚴重病例
醋酸潑尼松的最大劑量可達每日120~140mg,症狀改善後,醋酸潑尼松劑量應遞減至能保持症狀改善的最低水平。對症狀較輕的病例可用醋酸潑尼松30~60mg/d持續到有效,如視力繼續惡化或無效可短期內用60mg以上至120mg/d,療程4~12周,以後劑量逐漸遞減,維持量5~20mg/d,視病情許可停藥,可加用利尿劑以減輕球後水腫,但應避免
電解質紊亂等副作用。環磷醯胺每日或隔日200mg靜脈注射或CB13486mg/d和醋酸潑尼松每日或隔日30~60mg口服隔周交替使用療效較好,且可減少藥物用量及副作用。療程3~4周,見效後醋酸潑尼松遞減至抽除,環磷醯胺改每日口服50~100mg(CB13482~4mg/d)維持較長時期,用藥期間應隨訪血象。
局部糖皮質激素注射 由於大劑量或較長期的服用糖皮質激素可產生一系列副作用,故有學者主張間歇性眼球後或球結合膜下局部注射庫存糖皮質激素製劑(depotpreparations)。此種療法對浸潤性症狀(如復視)可能獲得良好療效。近年有報告套用
環胞黴素A治療,有一定效果,與皮質激素合用,可能更為有效。
球後或垂體放射治療 球後照射應在大劑量糖皮質類固醇治療無效或因有禁忌證不能用皮質激素時考慮套用。放射線對敏感的
淋巴細胞起抑制作用,在上述療法未能良好奏效時,輔以球後放射治療對眼部浸潤及充血症狀可獲得較好療效,但對
眼球突出療效甚微。垂體照射療效不肯定,尚有發生
垂體功能減退之虞,故少有採用。
血漿置換法 可迅速去除血漿中抗眼外肌抗體等抗球後組織自身抗體,特別對病程較短、眼球突出急劇、有軟組織、角膜病變及
視力障礙者尤為有效。但此法的療效為一過性,一般應繼以
類固醇激素治療。血漿置換量每次2升,計3~4次。由於內科治療單獨套用療效多不持續,為獲得長期持續性療效,有必要合併套用。較為有效的治療法為:血漿置換、類固醇激素和放療三者並用。首先,用血漿置換將血漿中自身抗體迅速清除,再以類固醇激素抑制抗體生成,最後以放療達到抑制眼窩內自身免疫反應。
外科手術 嚴重突眼且視力受明顯威脅者,應和外科或眼科醫生共同研討手術方案。眼眶後壁及頂部移除術,篩竇後壁和上頜竇頂部切除術常被套用。