歷史沿革 1934年,
恩里科·費米 和
羅馬大學 的研究團隊發布訊息表示他們發現了元素94。1783年胡塞·德盧亞爾和浮士圖·德盧亞爾兄弟發現從黑鎢礦可以獲得同樣的酸。費米將元素取名 “
hesperium ”,並曾在他1938年的
諾貝爾獎 演說中提及。然而,他們的研究成果其實是鋇、
氪 等許多其他元素的混合物。但由於當時
核分裂 尚未發現,這個誤會便一直延續。
格倫·西奧多·西博格 1941年,經找到周期表中最後一個可能存在的元素,而考慮過“ultimium”或“extremium”等名稱。
元素簡介 鈽有六種同位素和四種
氧化態 ,易和碳、
鹵素 、氮、
矽 起化學反應。鈽暴露在潮濕的空氣中時會產生氧化物和
氫化物 ,其體積最大可膨脹70%,屑狀的鈽能
自燃 。它也是一种放射性毒物,會於骨髓中富集。因此,操作、處理鈽元素具有一定的危險性。
物理性質 鈽和多數金屬一樣具銀灰色外表,又與
鎳 特別相似,但它在氧化後會迅速轉為暗灰色(有時呈黃色或橄欖綠)。鈽在室溫下以α型存在,是元素最普遍的結構型態(
同素異形體 ),質地如
鑄鐵 般堅而質脆,但與其他金屬製成合金後又變得柔軟而富延展性。鈽和多數金屬不同,它不是熱和
電 的良好導體。它的熔點很低(640 °C),而沸點異常的高(3235°C)。
鈽在室溫時的
電阻率 比一般金屬高很多,而且鈽和多數金屬相反,其電阻率隨溫度降低而提高。但研究指出,當溫度降至100K以下時,鈽的電阻率會急劇降低。電阻率由於輻射損傷,會在20K之後逐漸提高,速率因同位素結構而異。
鈽具有自發輻射性質,使得晶體結構產生疲勞,即原有秩序的原子排列因為輻射而隨時間產生紊亂。然而,當溫度上升超過100K時,自發輻射也能導致退火,削弱疲勞現象。
鈽和多數金屬不同:它的密度在熔化時變大(約2.5%),但液態金屬的密度又隨溫度呈線性下降。另外,接近熔點時,鈽的液態金屬具有很高的
黏性 和
表面張力 (相較於其他金屬)。
鈽最普遍釋放的游離輻射類型是α粒子發射(即釋放出高能的
氦 原子核)。最典型的一種
核武器 核心即是以5公斤(約12.5×10^24個)鈽原子構成。由於鈽的半衰期為24100年,故其每秒約有11.5×10^12個鈽原子產生衰變,發射出5.157MeV的α粒子,相當於9.68瓦特能量。α粒子的減速會釋放出熱能,使觸摸時感覺溫暖。
化學性質 鈽金屬 鈽及其
同位素 因為其放射性而有一定危險性。鈽產生的
α射線 並不會穿透人體的皮膚而進入人體,但鈽可能被人體吸入或消化而進入人體從而對內臟造成不利影響。α射線會造成細胞的損傷、染色體的損傷,理論上可能導致癌症發病率的上升。但是這種影響並不會比其它能放出α射線的放射性物質危害更大。相比之下,鈽的半衰期很長,使得單位時間裡的輻射量相對要小,危害也就更小。在自然界廣泛存在的氡的放射危害就要比鈽大的多。鈽容易在人體的肝臟和骨骼中聚集,但該過程非常緩慢。
在20世紀四十年代,美國就有26名工作人員因核武器研究,受到了鈽的污染。但是在他們身上並沒有出現嚴重的健康影響,更沒有人因此而死亡。
在一般情況下,鈽有六種
同素異形體 ,並在高溫、限定壓力範圍下有第七種(zeta, ζ)存在。這些同素異形體的內能相近,但擁有截然不同的密度和
晶體結構 。因此鈽對溫度、壓力以及化學性質的變化十分敏感,各同素異形體的體積並隨
相變 而具有極大差異性。密度因同素異形體而異,範圍自16.00 g/cm^3到19.86 g/cm^3不等。
諸多同素異形體的存在,造成鈽的狀態易變,使鈽元素的製造變得非常困難。例如,α型存在於室溫的純鈽中。它和
鑄鐵 有許多相似加工後性質,但只要稍微提高溫度,便會轉成具有可塑性和可鍛造性的β型。造成鈽複雜相圖的背後因素迄今仍未被完整解惑。α型屬於低對稱性的
單斜 結構,因此促成它的易碎性、強度、壓縮性及低傳導性。
鈽是一種具放射性的
錒系 金屬。它的5f電子是離域和定域之間的過渡界線。鈽因此常被認為是最複雜的元素之一。它的
同位素 鈽-239 是三個最重要的易裂變同位素之一(另外二者為鈾-233和鈾-235);鈽-241也具有高度易裂變性。所謂的具“易裂變性”(fissile),是指同位素的
原子核 受到
慢中子 撞擊後,能夠產生
核分裂 ,並另釋放出足以支持
核連鎖反應 、進一步促使原子核分裂的中子。
電解法精煉的武器級鈽元素環狀物 環狀金屬鈽重5.3公斤,直徑約11厘米,足夠製作一枚
核彈 。它的形狀有助於維繫
臨界安全 。
鈽有二十種
放射性同位素 。在自然界中只找到兩種鈽同位素,一種是從
氟碳鈰鑭礦 中找到的微量鈽-244,已知鈽的同位素中壽命最長的是鈽-244,半衰期是8.26×10^7年,它具有足夠長的半衰期,可能是地球上原始存在的。另一種是從含鈾礦物中找到的
鈽-239 ,是鈾238吸收自然界裡的中子而形成的。其他鈽同位素都是通過人工核反應合成的。
其中壽命最長的有鈽-244(半衰期為8080萬年)、鈽-242(半衰期為373300年)及鈽-239(半衰期為24110年)。其餘的放射性同位素半衰期都低於7000年。鈽也有八種
亞穩態 ,但狀態並不穩定、半衰期都不超過一秒。
鈽的同位素的
質量數 範圍從228到247不等。其中質量數低於鈽-244(最穩定的同位素)的同位素,主要的衰變方式是
自發裂變 和
α衰變 ,衰變產物通常生成
鈾 (92個
質子 )和
鎿 (93個質子)的同位素(忽略裂變過程產生之二子核的大範圍)。質量數大於鈽-244的同位素則以
β衰變 為主要衰變方式,衰變產物多為鎇(95個質子)。鈽-241是鎿衰變系的母同位素,透過β粒子或電子放射衰變成鎇-241。
衰變能量MeV
衰變產物
Pu-238
人造
87.74年
自發分裂
204.66
-
α衰變
5.5
U-234
Pu-239
微量
24100年
自發分裂
207.06
-
α衰變
5.157
U-235
Pu-240
人造
6500年
自發分裂
205.66
-
α衰變
5.256
U-236
Pu-241
人造
14年
自發分裂
210.83
-
β衰變
0.02078
Am-241
Pu-242
人造
373000年
自發分裂
209.47
Kr-92,Ba-141,2箇中子
α衰變
4.984
U-238
Pu-244
微量
8.08×10^7年
α衰變
4.666
U-240
鈽-238和鈽-239是最普遍的人造同位素。鈽-239是使用鈾(U)和中子(n),並以
鎿 (Np-239)作為中間體,產生β衰變(β)。透過反應1合成。
反應1 鈾-235裂變中的中子被鈾-238原子核
俘獲 、形成鈾-239;
β衰變 將一個中子轉變成質子,形成鎿-239(半衰期為2.36日),另一次β衰變則形成鈽-239。
合金管 計畫的學者曾在1940年推導出此反應式。
反應2 鈽-238是以
氘核 (D,重
氫 的原子核)撞擊鈾-238。透過反應2合成。
在此反應過程中,一個氘核撞擊鈾-238,生成兩個中子和鎿-238;鎿-238再發射負β粒子、產生自發衰變,形成鈽-238。
鈽同位素會發生放射性衰變,釋放出
衰變熱 。不同的同位素,單位質量所釋出的熱量也有所差異。衰變熱的單位通常以“瓦特/公斤”或“毫瓦特/公克”計。所有同位素在衰變時都會釋放出微弱的伽馬射線。
它最穩定的
同位素 是鈽-244,
半衰期 約為八千萬年,足夠使鈽以微量存在於自然環境中。
鈽-240
自發裂變 的比率很高,容易造成
中子通量 激增,因而影響了鈽作為核武及反應器燃料的適用性。
分離鈽同位素的過程成本極高又耗時費力,因此鈽的特定同位素時幾乎都是以特殊反應合成。
1940年,
格倫·西奧多·西博格 和
埃德溫·麥克米倫 首度在柏克萊加州大學實驗室,以
氘 撞擊鈾-238而合成鈽元素。麥克米倫將這個新元素取名Pluto(意為
冥王星 ),西博格便開玩笑提議定其元素符號為Pu(音類似英語中表嫌惡時的口語“pew”)。科學家隨後在自然界中發現了微量的鈽。二次大戰時
曼哈頓計畫 則首度將製造微量鈽元素列為主要任務之一,曼哈頓計畫後來成功研製出第一個核子彈。1945年7月的第一次
核試驗 “三一核子彈”,以及第二次、投於
長崎市 的“
胖子核子彈 ”,都使用了鈽製作核心部分。關於鈽元素的人體輻射實驗研究並在未經受試者同意之下進行,二次大戰期間及戰後都有數次核試驗相關意外,其中有的甚至造成傷亡。
核能發電廠 核廢料 的清除,以及
冷戰 期間所打造的核武建設在核武裁減後的廢用,都延伸出日後核武擴散以及環境等問題。非陸上核試驗也會釋出殘餘的原子塵,現已依《部分禁止核試驗條約》明令禁止。
名稱
鈽(Pu)
系列
周期,元素分區
3,7,f
類型
金屬
外表
銀白色
[244]
159
187±1 pm
氧化態
+4(+3、+5、+6、+7)
[
氡 ]5f6 7s2(2-8-18-32-24-8-2)
584.7 KJ/mol
單斜晶系。單斜晶型(鈽α和鈽β)、斜方晶型(鈽γ)、面心立方晶型(鈽δ)、體心四方晶型(鈽δ')、體心立方晶型(鈽ε)。
a=618.3 pm
b=482.2 pm
c=1096.3 pm
α=90°
β=101.790°
γ=90°
鈽同位素的衰變熱:
同位素
衰變方式
鈽-238
87.74
560
2600
α衰變成為鈾-235
24100
1.9
0.022
鈽-240
α衰變成為鈾-236
6560
6.8
910
鈽-241
14.4
4.2
0.049
鈽-242
α衰變成為鈾-238
376000
0.1
1700
室溫時,純鈽金屬是銀灰色、但因氧化而鏽蝕。鈽在
水溶液 中形成四種離子
氧化態 :
鈽在溶液中的各種氧化態 Pu(III)—Pu^3+(藍紫色)
Pu(IV)—Pu^4+(黃棕色)
Pu(V)—PuO^2+(粉紅色)
Pu(VI)—PuO2^2+(粉桔色)
Pu(VII)—PuO5^3?(綠色)–七價離子較稀有鈽溶液所呈現的顏色決定於氧化態和酸
陰離子 的性質。鈽的酸陰離子種類影響了
錯合 (原子與中心原子結合)的程度。
三氟化鈽 為藍紫色固體,熔點為1425±3℃;在沒有
鋁 或
鋯 離子存在時,很難溶於酸中。三氟化鈽可由鈽(IV)的
硝酸鹽 、氧化物、
氫氧化物 等化合物與
無水氟化氫 在550~600℃反應製得,也可在含鈽(III)的水溶液中加入氟離子沉澱而製得。三氟化鈽是還原法制金屬鈽的原料。
四氟化鈽 為淡棕色(PuF4·2.5H2O為粉紅色),熔點為1037℃,沸點約1277℃;微溶於水,只能溶於含有
硼酸 、鋁(III)或鐵(III)的溶液中。四氟化鈽可由鈽(IV)的氧化物、硝酸鹽、
草酸鹽 等化合物在有
氧氣 存在的條件下與無水氟化氫進行高溫反應而製得。四氟化鈽也是還原法制金屬鈽的原料。
六氟化鈽在-180℃時是白色固體,液態和
氣態 呈棕色到紅棕色,熔點為51.59℃,沸點為62.16℃;六氟化鈽在
熱力學 上是不穩定的,它是一個很強的氧化劑;能與
四氟化鈾 、二氧化硫、一氧化碳、二氧化碳等反應生成四氟化鈽,與潮濕空氣或水發生非常激烈的反應;六氟化鈽由於α輻解而不斷生成四氟化鈽。六氟化鈽可由二氧化鈽或四氟化鈽在500~700℃高溫下與氟氣反應製得。鈽(VI)的其他氟化物有PuO2F2、M2PuO2F4·H2O和MPuO2F3·H2O(M為NH4、Na、K等)。
三氯化鈽 是藍至綠色的固體,熔點為750℃,沸點為1767℃;易吸潮,易溶於酸和水。三氯化鈽可由多種方法製備,通常由
二氧化鈽 與光氣在高溫下反應而製得。在製備中,大多數其他元素生成揮發性的
氯化物 ,而三氯化鈽不揮發,因而鈽的純度較高。三氯化鈽也是製備金屬鈽的一種化合物。
四氯化鈽是不穩定化合物,容易分解,不易製得。鈽(IV)的其他氯化物有 M2PuCl6(M為Cs、Rb、K、Na等)。
其他已經製得的化合物還有:三溴化鈽,熔點約為681℃;
三碘化鈽 ,熔點約777℃。
二氧化鈽是綠棕色到黃棕色的固體,在氦氣中的熔點為2280±30℃,蒸氣壓很低;它的化學惰性很大,在鹽酸和
硝酸 中溶解極慢且不完全,在沸騰的氫溴酸中溶解較快,用
硫酸氫鈉 等熔劑在
熔融 條件下可溶解二氧化鈽;高溫下二氧化鈽可與氟化氫反應生成三氟化物,有氧氣存在時生成四氟化物;高溫下與氟作用生成六氟化鈽,與鋅鎂合金反應還原生成金屬鈽。由於二氧化鈽具有高熔點、輻照穩定、同金屬互容以及容易製備等特性,是核燃料的一種適用的組成形式。二氧化鈽可由金屬鈽或其化合物(磷酸鹽除外)在空氣中灼燒製得,也可由含氧化合物在真空或惰性氣氛中加熱到1000℃而製得。β-三氧化二鈽的熔點為2085±25℃;可由二氧化鈽與碳在氦中加熱到1625℃製得。α-三氧化二鈽可由在真空中加熱二氧化鈽到1650~1800℃ 而製得。α-三氧化二鈽由二氧化鈽熔化時損失氧而製得,其熔點為2360±20℃。
鈽化合物的結晶體 碳化物:已知有二碳化三鈽、
碳化鈽 、三碳化二鈽和二碳化鈽。室溫下碳化鈽在空氣中穩定,但在400℃時則劇烈燃燒;不與冷水作用,但與熱水反應生成三價氫氧化物、氫和甲烷的混合物,以及少量的其他
碳氫化合物 ;碳化鈽與冷硝酸作用很慢。三碳化二鈽的化學性質與碳化鈽略有不同,三碳化二鈽在高溫下的氧化作用及在酸和沸水中的水解作用都比碳化鈽弱。鈽的碳化物可由金屬鈽、二氧化鈽或氫化鈽在高溫下與石墨反應而製得。反應條件不同,可以製得不同組分的鈽的碳化物。鈽的碳化物由於具有較高的導熱性、低的蒸氣壓和較大的鈽密度,可以做核反應堆的燃料。
氮化物:已知鈽的唯一氮化物為
氮化鈽 。氮化鈽在
氬氣 氛中熔點為2450±50℃;遇冷水緩慢水解並生成二氧化鈽,氮化鈽易溶於
無機酸 中;與
氮化鈾 能形成一系列固溶體。氮化鈽具備核燃料的
某些特性,如熔點高、鈽密度高和好的導熱性,但它的主要缺點是在高溫下揮發性較高和易分解。氮化鈽可由氫化鈽與氮在高於 230℃時反應而製得。
草酸鹽:鈽(III)的草酸鹽Pu2(C2O4)3·10H2O和鈽(IV)的Pu(C2O4)2·6H2O都是難溶性化合物,隨著加熱,它們逐漸失去其結晶水,隨後分解,最終產物為二氧化鈽。鈽的草酸鹽可由鈽的相應氧化態的鹽的稀酸溶液與草酸或草酸鈉沉澱而製得。
能源與熱源:同位素鈽-238的半衰期為87.74年。它會放出大量熱能,伴隨著低能的伽馬和
自發裂變 射線/粒子。它是
α輻射體 ,同時具有高輻射能及低穿透性,故僅需低度防護措施。單一紙張就可以抵擋鈽-238所放射出的α粒子;同時,每公斤的鈽-238可產生約570瓦特熱能。
套用領域 同位素鈽-239是
核武器 中最重要的裂變成份。將鈽核置入
反射體 (質量數大的物質的反射層)中,能使逃逸的中子再反射回彈心,減少中子的損失,進而降低鈽達到
臨界質量 的標準量:從原需16公斤的鈽,可減少至10公斤,即一個直徑約10厘米的球體的量。它的臨界質量約僅有鈾-235的三分之一。
曼哈頓計畫 期間製造的“
胖子核子彈 ”型鈽彈,為了達到極高的密度而選擇使用易爆炸、壓縮的鈽,再結合中心中子源,以刺激反應進行、提高反應效率。因此,鈽彈只需6.2公斤鈽便可達到
爆炸當量 ,相當於兩萬噸的
三硝基甲苯 (TNT)。在理想假設中,僅僅4公斤的鈽原料(甚至更少),只要搭配複雜的裝配設計,就可製造出一個
核子彈 。
核廢料:一般輕水反應爐所產生的核廢料中含有鈽,但為鈽-242、鈽-239和鈽-238的混合物。它的濃度不足以製作成核武器,不過可以改用作一次性的混氧燃料(MOX fuel)。在反應爐中以慢速熱中子放射線照射鈽時,會偶然發生中子俘獲,而增加鈽-242和鈽-240的量。因此反應進行到第二輪之後,鈽只能和快中子反應堆反應、消耗。在反應器中沒有快中子時(普遍情況下),剩餘的鈽通常會被遺棄,形成壽命長、處理棘手的核廢料。
毒性分析 對鈽毒性的誤解由來已久,關於它是
劇毒 的物質、“一丁點就能致人死亡”的說法在西方世界也同樣流傳廣泛。推測,鈽可能是受到了劇毒的釙的牽連。兩者的衰變類型相同,化學符號接近(Po、Pu),連中文寫法、讀音都那么那么的相近,也難怪不明真相的民眾們把他們的各類性質掰到一起去。
鈽因周圍壓力變化而有六種同素異形體
流言 據
BBC 報導,前英國政府輻射事務顧問巴斯比博士表示,日本核電站的問題極為嚴重,尤其令人擔心的是福島核電站三號反應堆。他稱,該反應堆遇到麻煩,因為它使用的是一種不同的燃料:它不是
鈾 ,而是一種鈾鈽混合燃料,而鈽是極為危險的,因此一旦這種物質泄漏出來,將使
海嘯 災難雪上加霜。鈽是世界上毒性第二大的物質(世界上毒性第一大的物質為釙)。一片藥片大小的鈽,足以毒死2億人,5克的鈽足以毒死所有人類。鈽的毒性比砒霜大4.86億倍。
真相 2011年3月14日凌晨03:11的BBC新聞,報導了前英國政府輻射事務顧問巴斯比博士(Dr Christopher Busby)對福島核電站3號機組的擔憂。這條新聞的背景是日本內閣官房長官枝野幸男2011年3月13日警告說,福島第一核電站3號機組反應堆面臨遭遇外部氫氣爆炸風險。但是關於鈽的毒性問題,卻不似流言所描述的那么可怕。“一片藥片大小的鈽足以毒死2億人,5克的鈽足以毒死所有人類”的說法更是沒有任何的科學依據。
香港無線電視 的新聞節目曾引用此謠傳,結果被當地監管機構警告,指報導令觀眾驚恐,未有提供足夠證據確保報導準確。
結論 鈽的毒性並沒有謠言描述的那么可怕,“5克的鈽足以毒死所有人類”純屬無稽之談。使用鈾鈽混合燃料的反應堆如果發生爆炸泄露,並不會比使用鈾燃料的傳統反應堆要來的更危險。對於鈽危害的擔憂,更多的是來自於鈽的電離輻射能力。
鈽衰變時會產生α射線。α射線的穿透能力非常弱,在空氣中前進幾厘米就將能量耗盡。對於環境中的鈽並不用太擔心。一旦鈽進入到人體內,形成的內照射會對人體有一定的影響。
根據報導,中國核科學家
鄧稼先 曾在1979年一次核航彈空投試驗失敗後接觸過用於製造其核裝置的鈽,最終仍活到1986年(死因為長期放射傷害導致的癌症),可見鈽並沒有如謠言中所描述的劇烈急毒性。
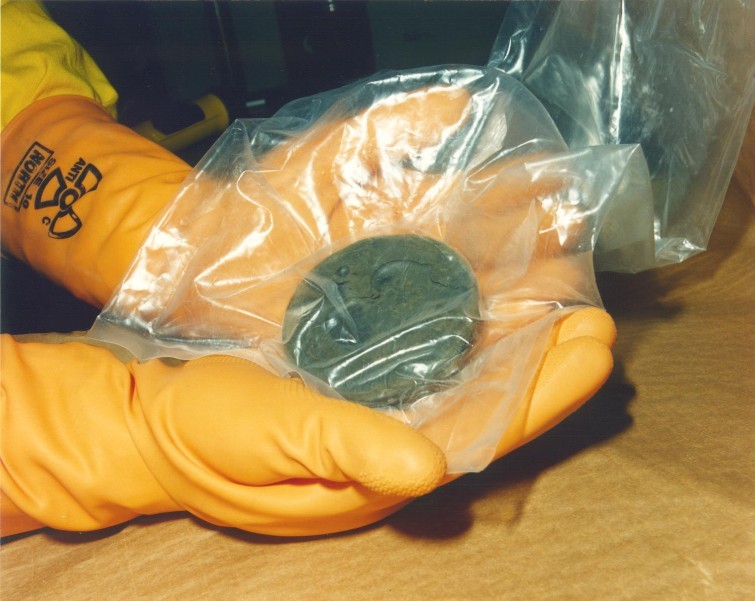
而英國女王
伊莉莎白 二世訪問哈維爾核子實驗室時,就曾受邀觸摸了一塊以塑膠包裹的鈽環,以親自體會其溫暖的觸感。基於鈽本身的化學毒性並不那么大,電離輻射能力也不比其它放射性元素要來的特殊,加上鈾鈽混合燃料里鈽也只有7%,3號反應堆如果發生爆炸泄露,並不會比其它使用鈾燃料的反應堆要來的更危險。
相關事件
福島事故 2011年3月28日晚,日本東京電力公司宣布,福島第一核電站廠區採集的土壤樣本首次檢測出放射性元素鈽。東電副社長說,這種核裂變產生的強輻射物可能來自受損燃料棒。
發出光、熱的鈽元素球狀礦 東電稱,現階段檢測到鈽的濃度屬於正常水平,不會影響人體健康。
東電當天深夜在首都東京召開新聞發布會說,工作人員在2011年3月21日和22日從福島第一核電站區域內5處地點採集土壤樣本,公司委託外部機構檢測,證實這些樣本中存在微量的鈽—238、鈽—239和鈽—240。
東電副社長武藤榮說,“讓人們感到憂慮,我表示道歉”,但這些鈽的濃度屬於正常環境下土壤中放射物濃度水平,不會構成威脅,出事機組搶修工作也沒有停止。
武藤說,現有鈽的濃度與冷戰時期美國、蘇聯等國大氣核試驗後飄落至日本的放射性物質濃度水平相當,“不到危害人體健康的程度”。
土壤樣本中鈽的濃度為每公斤0.54貝克勒爾至每公斤0.18貝克勒爾不等。
東電宣布將加強對核電站區域內和周邊環境的監測,在廠區新增3個觀測點,密切注視鈽濃度變化。
東電公布的數據和信息接連出錯,其數據分析能力和所公布數據的可靠性受到多方質疑。
東電稱尚不清楚這些鈽來自那裡。其中兩處地點的土壤樣本中都檢測出鈽—238,看起來有可能來自出事機組,而非大氣層。這兩份土壤樣本均為乾燥土壤。鈽—238的半衰期為88年。
一些核能安全專家分析,這些鈽—238可能來自3號反應堆,後者是核電站6座反應堆中唯一以鈽鈾混合氧化物(MOX)為燃料的機組。
東電上周宣布在3號機組渦輪機房地下室積水中檢測出超高濃度放射性物質,可能泄漏自反應堆。3名員工24日在地下室作業時遭過量輻射而入院。
按照武藤28日晚在新聞發布會上的說法,這些鈽可能由乏燃料池部分熔毀的核燃料棒釋放。
不過,原子能安全保全院發言人西山英彥說,測出鈽元素意味著“燃料棒遭受一定程度損傷”,儘管核反應堆有多層防護殼,但發現這種有毒輻射物可謂“糟糕”。
“雖然現有鈽的濃度不足以威脅人體健康,但我並不感到樂觀,”援引西山的話報導,“這意味著安全殼出現破裂,我認為形勢令人不安。”
有關專家指出,無論本次泄漏的鈽有多少,處理起來都很麻煩,並且在它泄漏初期,應該及時將燃料棒取走,如果最後選擇對福島第一核電站幾個受損的反應堆進行封堆處理,卻不拿走含鈽的燃料,鈽仍然會污染地下水。因此,日本有關方面稱事態“嚴重”。
鈽的危險性還在於它對人體的毒性,與其他放射性元素相比鈽在這方面更強,一旦侵入人體,就會潛伏在人體肺部、骨骼等組織細胞中,破壞細胞基因,提高罹患癌症的風險。而且這一放射性元素的半衰期很長,在處理上更為困難。
日本囤積 日本通過各種途徑大量存儲核材料,其中包括武器級豐度的放射性物質鈽和鈾。日本存儲的這些核材料里,有300多公斤武器級鈽是美國在冷戰期間交給日本的。日本原先強烈反對歸還這批鈽,理由是需要這批鈽用於快中子反應堆研究。美國在過去幾年裡多次提出要求,日本最終答應歸還,美國計畫於2014年3月在荷蘭參加核安全峰會期間與日本敲定歸還協定。日本還囤積了超過1.2噸高濃縮鈾(包括215公斤攻擊武器級高濃鈾)以及約44噸分離鈽。
漏報事件 2014年年初,可以生產80枚核彈頭的640千克鈽在日本向國際原子能機構提供的報告中被蒸發。儘管日本政府給出並非故意漏報的說辭,但日本國內和國際社會的質疑與擔憂並未減弱。
日本保有大量敏感核材料一事就引發世人的擔心,這些敏感核材料甚至包括能夠直接用於製造核武器的武器級鈽和武器級鈾日本長期以來一直從核廢料中提取鈽,加上上面提到的640千克鈽,日本目前擁有45噸可用於生產核武器的鈽,共可生產約5500枚核彈頭。
日本已成為世界上唯一可以進行乏燃料後處理的無核武國家,擁有世界第一大後處理工廠。日本以和平利用核能的名號,大力開展核聚變、快中子增殖反應堆等尖端核技術研究,製作核聚變實驗裝置和核聚變反應堆,同時以民用核電需要為名,不遺餘力大量收購、儲存、提煉核原料。近來,日本加快了濃縮鈾製造“本土化”步伐,新建了離心法鈾濃縮工廠和雷射鈾濃縮工廠,其鈾原料的分離處理能力可達年產1500噸。
 格倫·西奧多·西博格
格倫·西奧多·西博格
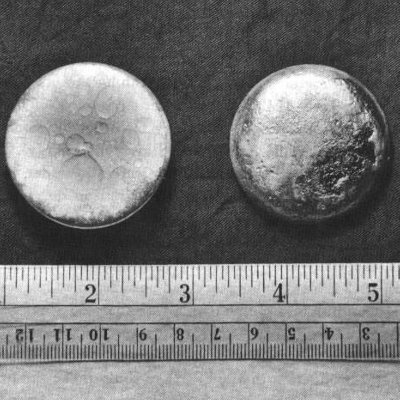 鈽金屬
鈽金屬 電解法精煉的武器級鈽元素環狀物
電解法精煉的武器級鈽元素環狀物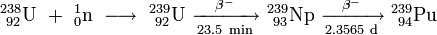 反應1
反應1 反應2
反應2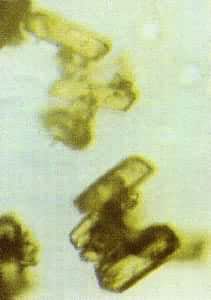 鈽化合物的結晶體
鈽化合物的結晶體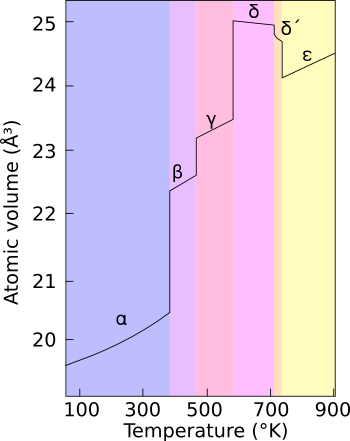 鈽因周圍壓力變化而有六種同素異形體
鈽因周圍壓力變化而有六種同素異形體 發出光、熱的鈽元素球狀礦
發出光、熱的鈽元素球狀礦
 金屬鈽
金屬鈽 鈽在溶液中的各種氧化態
鈽在溶液中的各種氧化態