所謂無機酸,是無機化合物的酸類的總稱,亦稱之為礦酸,如鹽酸HCl,硫酸,硝酸等。
無機酸是由氫和非金屬元素組成的化合物。
基本介紹
- 中文名:無機酸
- 外文名:inorganic acid
- 別名:礦酸
- 所屬:無機化合物中酸類
- 領域:化學
術語簡介
 無機酸
無機酸相關區別
酸式鹽
有機酸
分類
組成成分
 無機酸
無機酸電離程度
氫離子數



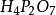

結構與性能
氫酸



 無機酸
無機酸


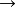

含級酸








所謂無機酸,是無機化合物的酸類的總稱,亦稱之為礦酸,如鹽酸HCl,硫酸,硝酸等。
無機酸是由氫和非金屬元素組成的化合物。
 無機酸
無機酸 無機酸
無機酸


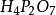




 無機酸
無機酸


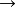








所謂無機酸,是無機化合物的酸類的總稱,亦稱之為礦酸,如鹽酸HCl,硫酸,硝酸等。無機酸是由氫和非金屬元素組成的化合物。...
有機酸是指一些具有酸性的有機化合物。最常見的有機酸是羧酸,其酸性源於羧基 (-COOH)。磺酸 (-SO3H)、亞磺酸(RSOOH)、硫羧酸(RCOSH)等也屬於有機酸。有機...
無機酸製造 ◇ 包括: —無機酸:硫酸、鹽酸、硼酸、磷酸、氯磺酸、氫氟酸等。 ◆ 不包括: —硝酸的生產,列入2621(氮肥製造)。 ...
無機酸緩蝕劑主要用於金屬酸洗過程中減緩酸對金屬基體的腐蝕,在各種化學酸洗過程中都有良好的緩蝕效果。在正常使用下使金屬的腐蝕率大大降低,並有優良的抑制鋼鐵在...
《飼料添加劑 無機酸通用要求(GB/T 22143-2008)》是由全國飼料工業標準化技術委員會提出並歸口的中華人民共和國國家標準GB/T 22143—2008。本標準起草單位:中國...
無機,化學名詞。原指化合物是跟非生物體有關或從非生物體而來,一般指除碳酸鹽和碳的氧化物外不含碳原子的化合物。如無機化學、無機化工、無機物、無機酸﹑無機...
無機化工是無機化學工業的簡稱,以天然資源和工業副產物為原料生產硫酸、硝酸 、鹽酸、磷酸等無機酸、純鹼、燒鹼、合成氨、化肥以及無機鹽等化工產品的工業。包括硫酸...
inorganic cellulose ester 纖維素的無機酸酯。隨所用酸的不同而有硝酸纖維素、黃原酸纖維素和磷酸纖維素之分。以硝酸纖維素用量最大,黃原酸纖維素次之。磷酸...
無機酸一類在水溶液中能電離產生H 的化合物的總稱,與鹼相對。鹽酸、硫酸、硝酸在水溶液中電離時,產生的陰離子(酸根)雖各不相同,但產生的陽離子(H )卻是相同...
酯化反應,是一類有機化學反應,是醇跟羧酸或含氧無機酸生成酯和水的反應。分為羧酸跟醇反應和無機含氧酸跟醇反應和無機強酸跟醇的反應三類。羧酸跟醇的酯化反應...
酸味是有機酸、無機酸和酸性鹽產生的氫離子引起的味感。適當的酸味能給人以爽快的感覺,並增進食慾。一般來說,酸味與溶液的氫離子濃度有關,氫離子濃度高酸味強,...
棓酸,讀作bànɡ suān,即沒食子酸。又稱五棓子酸,分子式CH67O5。白色或淺褐色針狀結晶或粉末。具有抗菌作用,可治療菌痢。具有收斂、止血、止瀉作用。可用作...
酸酐(英文:Anhydrides)是某含氧酸脫去一分子水或幾分子水,所剩下的部分。一般無機酸是一分子的該酸,直接失去一分子的水就形成該酸的酸酐,其酸酐中決定酸性的...
硫化鍺,是一種半導體材料,不溶於水和無機酸(包括強酸),易溶於熱鹼。...... 硫化鍺,是一種半導體材料,不溶於水和無機酸(包括強酸),易溶於熱鹼。...
定義 酸浸出acid leaehiaig以無機酸(硫酸、鹽酸、硝酸)為浸 取劑的浸出過程。硫酸浸出是最常用的鈾礦浸出過程,它對 鈾浸出率高,價格便宜。含矽酸鹽型、硫化物型...
