基本介紹
簡介
反應機理
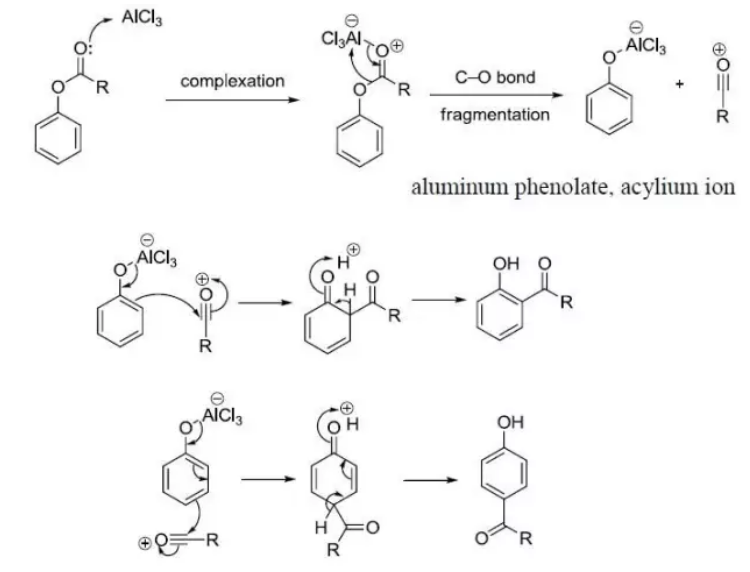 反應機理
反應機理反應舉例
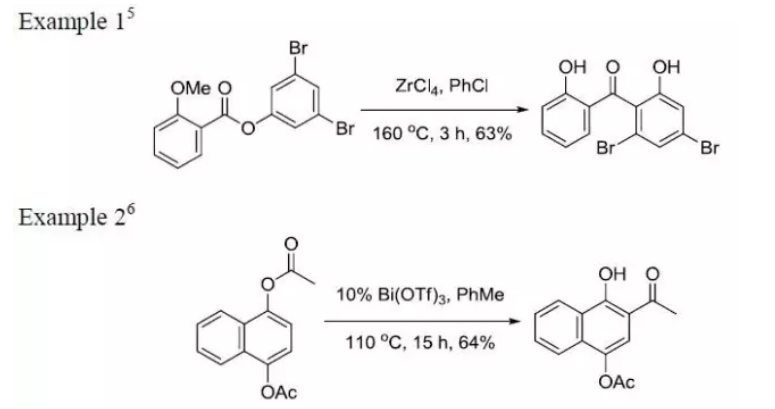 反應舉例
反應舉例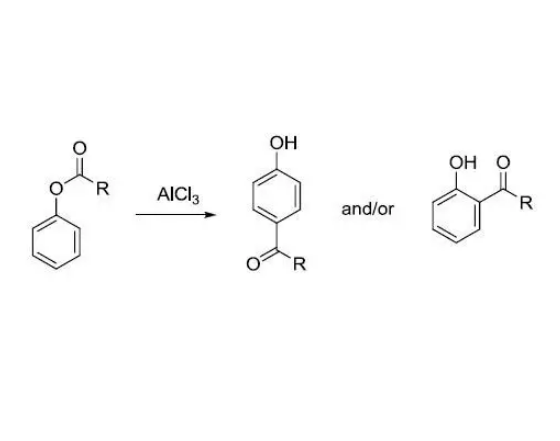
 反應機理
反應機理 反應舉例
反應舉例Fries重排反應(弗萊斯重排;弗賴斯重排;福萊斯重排)是酚酯在路易斯酸或布朗斯特酸催化下重排為鄰位或對位醯基酚的反應。反應由德國化學家 Karl Theophil Fries 首先報導...
Fries重排反應(弗萊斯重排;弗賴斯重排;福萊斯重排)是酚酯在路易斯酸或布朗斯特酸催化下重排為鄰位或對位醯基酚的反應。...
由Fries重排反應機理,醯基正離子作為親電試劑,與苯氧負離子發生親電取代,提高苯氧負離子的電子云密度有利反應的進行。因此酚酯上苯環帶有供電子基有利於重排反應,...
Wallach重排反應簡介 編輯 芳香氧化偶氮化物在(60~100%)硫酸作用下,重排為對位為酚羥基取代的芳香偶氮化合物。Wallach重排反應參見 編輯 Fries重排反應...
《重排反應原理》是2017年化學工業出版社出版的圖書,作者是孫昌俊、茹淼焱。...... 第一節芳環上的親電重排反應150一、Fries重排反應151二、Orton重排反應(氯胺重...
佛利斯重排(Fries rearrangement)是酚酯在路易斯酸或布朗斯特酸催化下重排為鄰位或對位醯基酚的反應。...
三、Wittig重排反應四、Smiles重排反應五、Fries重排第三節 σ?遷移重排一、氫的[1?j]遷移反應二、碳原子的[1?j]遷移反應三、碳原子的[i?j]遷移反應...
5.3.3 Fries重排5.3.4 Favorsky重排5.4 σ鍵遷移重排5.4.1 Claisen重排5.4.2 Cope重排習題*第6章 消除反應6.1 β-消除反應...
Cope重排272 Curtius重排反應275 Demjanov重排277 Dienone Phenol(二烯酮)重排反應280 Favorskii反應282 Favorskii重排283 Fries重排289 Hofmann重排293 Loss...
三、羥胺重排(N→C) 四、聯苯胺重排(N→C) 五、N-磺酸基芳胺重排(N→C) 六、Claisen重排(O→C) 七、Wittig重排(O→C) 八、Fries重排(O→C) 九、實...
4 3 9Demjanov Tiffeneau重排1974 3 10Dienone phenol(二烯酮 酚)重排1984 3 11di π 甲烷重排1984 3 12Favorskii 重排1994 3 13Fries重排200...
