基本介紹
- 中文名:酸度
- 外文名:acidity
- 單位:mg/g
- 酸度:H+的平衡濃度為酸度
- 分類:無機酸度、游離CO2酸度、總酸度
- 學科:化學
定義
概念
總酸度
有效酸度
揮發性酸度
牛乳酸度
外表酸度
真實酸度
組成分類
酸度測定
酸鹼指示劑滴定法
電位滴定法
優勢
酸度計
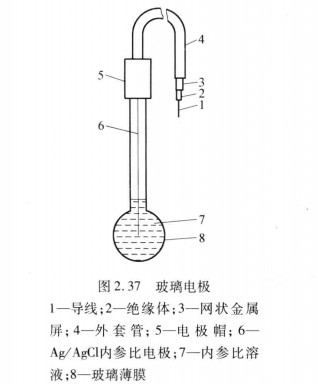 玻璃電極
玻璃電極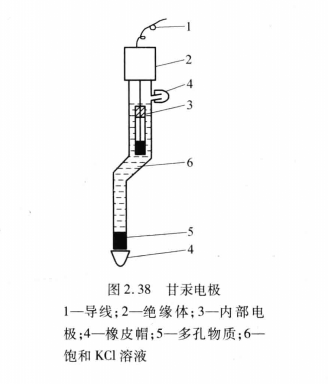 甘汞電極
甘汞電極
 玻璃電極
玻璃電極 甘汞電極
甘汞電極在化學中,酸度(或稱中和值、酸值、酸度)表示中和1克化學物質所需的氫氧化鉀(KOH)的毫克數 。酸度是對化合物(例如脂肪酸)或混合物中游離羧酸基團數量的一個...
在水中,由於溶質的解離或水解(產生無機酸類、硫酸亞鐵和硫酸鋁等)而產生氫離子,這些氫離子與鹼標準溶液作用至一定pH值時所消耗的量,即定義為酸度。酸度數值的...
食品酸度是指食品中所有酸性成分的總量。GB5009.239-2016 中規定了部分食品酸度可用酚酞指示劑法、PH計法或電位滴定儀法進行測定。食品酸度分為總酸度、有效酸度、...
總酸度包括游離酸結合酸和來自食物或細菌代謝的有機酸,如乳酸醋液以及酸性磷酸鹽等。...
酸度係數(pKa),又名酸離解常數,是酸解離平衡常數的常用對數的相反數,其定義式為pKa=-lg(Ka)。酸度係數是隸屬於酸鹼質子理論的概念,它反映了一種酸將質子傳遞...
潛在酸度又稱分子分子酸度或後備酸度。是在天然水中是指包含在弱酸分子中的未電離的H+ 的數量以及由強酸弱鹼未水解部分構成的酸度,常用mmol/100L 表示;在土壤中是...
胃總酸度包括游離酸結合酸和來自食物或細菌代謝的有機酸,如乳酸醋液以及酸性磷酸鹽等。正常空腹胃液的游離酸為0~30U平均18U;總酸度為10~50U平均30U服試餐1...
酸度電位滴定法是以pH玻璃電極為指示電極,飽和甘汞電極為參比電極,與被沒水樣組成原電池並接入pH計,用氫氧化鈉標準溶液滴定至pH計指示3.7和8.3,據其相應消耗的氫...
PH計是用來測量溶液pH值的儀器,也稱酸度計。雖然型號較多、結構各異.但它們的原理相同。...
活性酸度、交換性酸度 土壤酸性表現的強弱程度。含有二氧化碳雨水的長期淋溶作用,土壤中生物的呼吸作用,有機質的分解,土壤中硫化物的氧化以及酸雨和施用酸性肥料等,都...
又叫外表酸度,指剛擠出的新鮮牛乳本身所具有的酸度,主要來源於鮮牛乳中酪蛋白,白蛋白擰檬酸鹽及磷酸鹽等酸性成分。同發酵酸度一起稱作總酸度。...
然而一些酸性非溶劑中,拉平作用不會發生,酸度可達水溶液的10^10或更多倍。在稀溶液中,酸性可根據pH值確定:pH= -lg[H3O+] = -lg[H+]...
牛奶酸度=自然酸度+發酵酸度,酸度是一個代表牛奶新鮮程度的理化指標,通過它可以評判出牛奶的新鮮程度。...
發酵酸度,又叫真實酸度,是指牛乳放置過程中在乳酸菌作用下,乳糖發酵產生乳酸而升高的那部分酸度。發酵酸度同固有酸度一起稱之為總酸度。...
哈默特酸度函式是由哈默特提出表示強酸溶液酸度的函式關係。...... 哈默特酸度函式 (H0) 是一種用於衡量高濃度酸酸性的指標,包括超強酸。它是由物理有機化學家路易斯...
1.酸度係數。2.cAMP依賴蛋白激酶,簡稱激酶A(PKA——protein kinase A)。cAMP發揮各種效應主要是通過激活它來實現的。它的重要作用是使某些基因調節蛋白磷酸化,進而...
有效酸度是指被測液中H+ 的濃度,準確地說應是 溶液中H+ 的活度,所反映的是已離解的那部分酸 的濃度,常用PH值表示.其大小可借酸度計(即 pH計)來測定。pH...
Brönsted酸性強度實際上測得的是一個平衡酸度,即熱力學酸度。其數值還與溫度和溶劑有關。共軛鹼上有較高電荷密度的酸,溶劑對它的pKa影響較大。而共軛鹼上具有...
酸度調節劑亦稱pH調節劑,是用以維持或改變食品酸鹼度的物質。發麵酸了加的鹼面就是酸度調節劑。它主要用以控制食品所需的酸化劑、鹼劑以及具有緩衝作用的鹽類。...
酸度源於葡萄中的酒石酸和蘋果酸以及發酵產生的琥珀酸、乳酸和醋酸。酸度賦予葡萄酒清新、清脆的品嘗感。酸有潔淨嘴巴和讓上顎煥然一新的效果。通常,種植於涼爽地區...
酸度計的級別和儀器的準確度是不同的兩個概念,儀器級別與其準確度並不完全一致。酸度計的級別是按其指示器(簡稱電計)的分度值(解析度或最小顯示值)表示的,例如...
