來源 貽貝 是海洋
養殖業 中的重要種類,中國是全球最大的貽貝生產國,占全球年產的1/4。
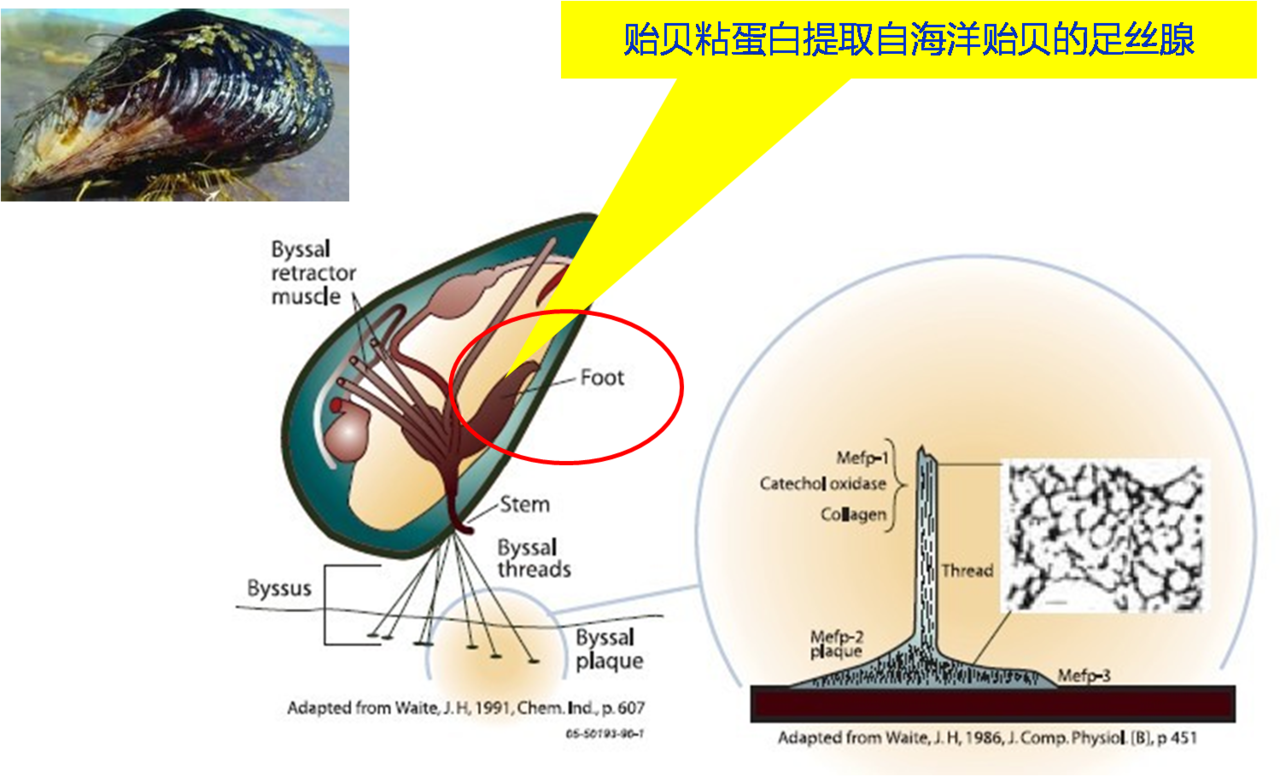
紫貽貝 在全球範圍內廣泛養殖。它的足絲腺分泌貽貝粘蛋白,形成強韌的蛋白絲,使貽貝固定於海水下的任何表面上,耐受風浪的衝擊。其海洋來源表現了兩個重要特點,一是隔水粘附:在海水中粘附於固體表面;二是耐受海水:形成粘附之後,耐受海水經年的沖刷。
貽貝粘蛋白
生產貽貝粘蛋白的原料是貽貝足絲,經過
粉碎 、
提取 、
色譜 純化 、
濃縮 等工藝步驟製備,獲得高純度的單一蛋白質。
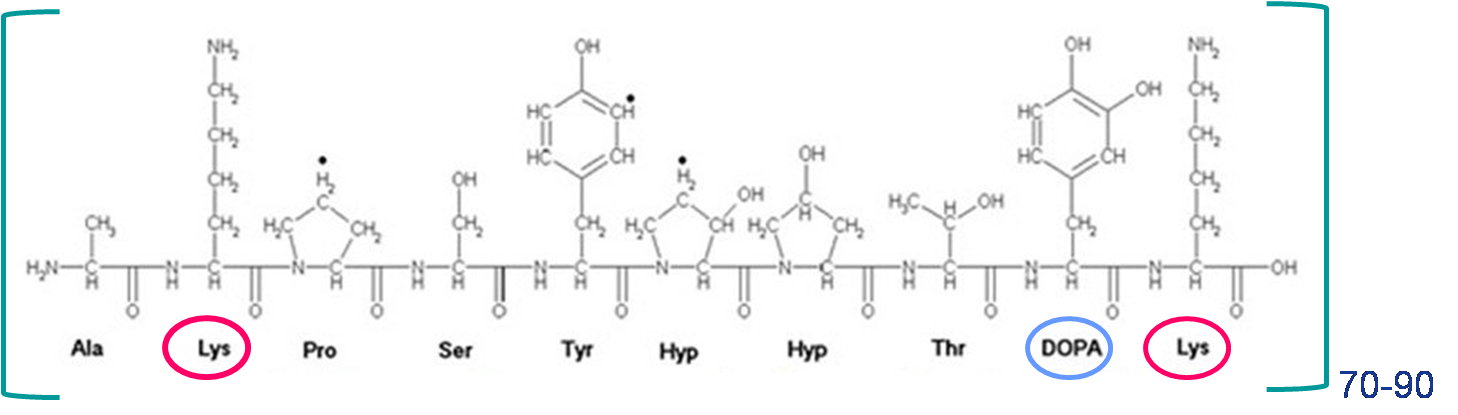
結構特點 貽貝粘蛋白有70-90個重複的多肽片段組成,每個多肽段由10個
胺基酸 組成,其中2個是
賴氨酸 。這使得蛋白具有較高的等電點,在人體生理pH值下帶有很強的正電荷。每個貽貝粘蛋白分子帶150以上正電荷。人體的各種細胞均帶負電荷,例如:
表皮細胞 、
成纖維細胞 、
成骨細胞 、
神經細胞 等。貽貝粘蛋白通過靜電相互作用與細胞結合,促進表皮細胞的貼壁、爬行替代,從而加速創面或
潰瘍 面的癒合。
貽貝粘蛋白肽鏈重複片段
2.多巴基團:形成非連續微觀生物支架
貽貝粘蛋白肽鏈片段中有10%的
DOPA 基團(3,4-二羥基苯丙氨酸)。在
PH值 5及以下,蛋白溶液可以溫室保存(保存期大於一年)。在
PH值 較高的情況下,
DOPA 中的一些酚羥基氧化成醌,這一過程在兒茶酚
氧化酶 存在下會被加速。氧化的
DOPA 和未氧化的
DOPA 交聯,形成高分子網狀
聚合物 。這張“網”將貽貝粘在海底。貽貝粘蛋白用於皮膚和疤痕治療時,這種集合物形成一個透明的、允許水蒸氣和空氣通透的膜。
3.疏水基團:強化細胞隔水黏附
組成貽貝粘蛋白的幾種胺基酸含有
疏水 基團,在生理溶液存在情況下,貽貝粘蛋白的部分疏水基團暴露出來,可與細胞膜的
脂質雙分子層 通過疏水作用相互結合。
研究進展 1.貽貝粘蛋白種類kinds of MAP
貽貝粘蛋白經常用於科學文獻的另一個名字是貽貝足蛋白(Mfp),它的一些結構已經確定:命名為Mfp-1,-2,-3,-4,-5和-6。其中Mfp-1是最主要的成分,也是第一個被分離出來的。它的分子量約為110Da,由70-90個多肽重複基序組成。(Mussel Adhesion: Finding the Tricks Worth Mimicking)
2.貽貝粘蛋白的製備方法PreparationofMAP
貽貝足絲蛋白的獲取方法主要有以下三種手段:
(1)直接從貽貝足腺中提取天然黏附蛋白成分,例如,瑞典Biopolymers公司自20世紀80年代開始直接貽貝足腺中提取並研製成組織培養用的
粘合劑 產品“Cell-Tak”,該產品主要是Mefp-1、Mefp-2和Mefp-3的混合物,可用於
細胞培養 過程中非
貼壁細胞 與
培養皿 的黏附。但由於貽貝足絲蛋白的分泌量很低,1萬個貽貝也只能提取1mg的粘附蛋白,導致這種直接提取的黏合劑產品價格昂貴,美國售價達到115美元/mg。
(2)由於組織提取方法成本高,學者們展開了
基因工程 手段生產貽貝粘蛋白的研究。如J.H.Waite等在1999年報導了將
紫貽貝 Mefp-3基因轉入
釀酒酵母 中進行表達;Dong Soo Hwang等於2004年報導了
地中海 貽貝的Mefp-5在
大腸桿菌 中的表達,
重組 的Mefp-5蛋白具有較好的粘結性能,有可能用於醫療及防水
黏合劑 的開發。韓國
浦項工業大學 (POSTECH)的Dong Soo Hwang等將
地中海貽貝 的mfp-5和mfp-3在
大腸桿菌 中的表達,得到重組的mfp-5和mfp-3蛋白生物化學
粘合劑 ,以用於醫療及防水
黏合劑 的開發。粘著蛋白原在貽貝足腺細胞中被合成時經歷了複雜的
糖基化 修飾、
羥基化 修飾及交聯反應,而利用
基因工程 途徑所得到的粘著蛋白產物則缺少這種嚴格而充分的修飾和加工過程。儘管學者們在體外對其進行了部分
糖基化 修飾,但所添加的
寡糖鏈 的數量、
羥基化 以及交聯程度與天然蛋白質相比均相差甚遠,致使所得蛋白產物的粘度遠遠不及天然蛋白質。
(3)由於利用基因工程途徑無法獲取理想粘度的粘著蛋白產品,因此,
貽貝 足腺 細胞 的
體外培養 與建系研究便成為獲取理想粘著蛋白產物的充滿希望的開發途徑,幫而引起了學術界的廣泛關注,早在20年前美國就率先開始了
貽貝 足腺 細胞 的體外培養研究,但由於無脊椎
動物細胞培養 困難,其培養仍屬世界性難題,
貽貝 足腺 細胞 的
傳代培養 及其建系一直未能成功。
因此從天然來源提取純化貽貝粘蛋白仍是該產品獲取的主要途徑。
3.貽貝粘蛋白的研究The study of MAP
貽貝粘蛋白的開創性研究是在20世紀70年代晚期由J H, Waite;M L, Tanzer和他的同事發起的。在20世紀80年代早期,他發表了關於貽貝粘蛋白的論文:《貽貝中
多酚 物質:含
左旋多巴 和
羥脯氨酸 的新型粘合劑》(Polyphenolic Substance of Mytilus edulis: Novel Adhesive Containing L-Dopa and Hydroxyproline)
自從貽貝粘蛋白的粘接性能發現後,它的其他功能也被逐漸發現。最初,他的用途是作為”
生物膠水 “用作手術縫合中的醫用膠粘劑。後來發現,貽貝粘蛋白還具有細胞貼壁和增殖的功能-促進傷口癒合及恢復。因此,貽貝粘蛋白對皮膚,黏膜組織,神經,骨,血管膜的創面有潛在的修復功能。它也可以與
銀離子 ,
肝素鈉 等其他藥物結合使用,還能與藥物洗脫支架以及
耐藥菌 組合使用。
與其他醫學修復材料和藥物相比,貽貝粘蛋白有它的生物起源和蛋白質的性質上具有一定的優勢。最新的研究表明,貽貝粘蛋白還可以用於手術切口,燒、燙傷,持久性潰瘍及皮膚病,止痛,抑菌以及促進癒合的功效。
4.貽貝粘蛋白的研究單位Research institutions with studies on MAP
(3)
美國西北大學 (Northwestern Univertsity):傾向於MAP吸附機理的研究及通過對MAP的研究模仿其開發新型的吸附材料;
(4)愛達荷國家工程和環境實驗室(Idaho National Laboratory):用於 生物醫用粘合,水下粘結,建築及特種膠粘。
作用機理 海洋貽貝粘附蛋白具有高強度、高韌性和防水性,以及極強的黏附基體的功能,這與其特殊的
分子結構 、多巴(DOPA)介導的鏈間交聯和與底材之間的相互作用方式有關,並且,它還具有很好的生物相容性和可降解性,是一類極具優勢和潛力的生物膠黏劑。
貽貝粘蛋白通過兩力一網
兩力指:靜電相互作用力;疏水相互作用力
一網指:氧化的多巴基團與未氧化的多巴基團
相互交聯形成微觀生物支架,強力粘附於創面,隔水發揮促進癒合和止癢止痛的作用。
1.貽貝粘蛋白的促癒合機理
貽貝粘蛋白形成隔水黏附帶正電荷的微觀生物支架促進癒合。貽貝粘蛋白MAP的等電點是9.5,在生理pH值下,因
賴氨酸 的存在帶有正電荷,在創面形成微觀支架,吸引帶負電的細胞,例如
表皮細胞 、
成纖維細胞 等快速貼壁、爬行替代和生長,促進創面癒合。
貽貝粘蛋白分子中含有大量的3,4-二羥基
苯丙氨酸 (
DOPA ),氧化的
DOPA 和未氧化的
DOPA 的氧存在的環境中自氧化交聯形成微觀非連續網狀生物支架,加固了隔水黏附。
黑色素 的合成在皮膚基底層的細胞中間發生的,不是在細胞內,色素的形成是色體內
酪氨酸 和
酪氨酸酶 反應形成
DOPA ,再形成多巴醌,最後形成多巴色素,整個過程都是氧化過程。
3.貽貝粘蛋白的止癢機理
貽貝粘蛋白(MAP)中具有10%含量的L-
DOPA 基團,L-
DOPA 跟
帕金森症 的治療藥物-多巴胺結構非常相近,它們都是神經遞質,可將信號從一段神經傳導至另一段,神經細胞具備它們的受體。
貽貝粘蛋白(MAP)在生理
PH值 下帶有很高載量的正電荷,人體的各種細胞帶負電荷,包括組成皮膚的各種細胞。每平方厘米皮膚表面包含至少150個
神經末梢 ,豐富的末梢上探到表皮層。靜電作用是微觀系統的強作用,貽貝粘蛋白首先通過
靜電作用 與
神經末梢 細胞結合,蛋白的
DOPA 繼而與細胞表面的
DOPA 受體結合,阻斷神經細胞的部分信號傳輸,從而起到止癢的作用。
套用價值 美國研究貽貝粘蛋白的套用已經30餘年,日本、韓國緊隨其後。我國對貽貝粘蛋白的實驗室研究已有10多年,2014年正式進入醫療市場。貽貝粘蛋白的套用主要集中於以下方面: