變旋現象(英文:Mutarotation)是環狀單糖或糖苷的比旋光度由於其α-和β-端基差向異構體達到平衡而發生變化,即旋光度發生改變,最終達到一個穩定的平衡值的現象。變旋現象往往能被某些酸或鹼催化。
基本介紹
- 中文名:變旋現象
- 外文名:Mutarotation
- 拼音:bianxuanxianxiang
- 簡述:旋光度改變的現象
- 催化:某些酸或鹼
- 出現:單糖都會出現
簡介
示例
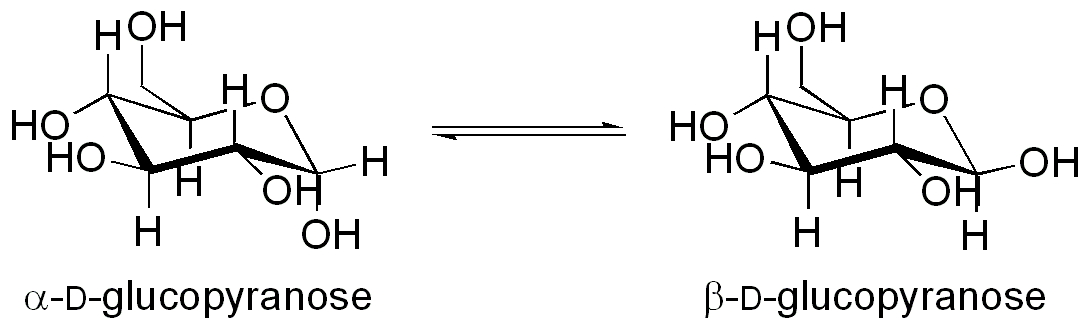 α-與β-D-吡喃葡萄糖之間的變旋。
α-與β-D-吡喃葡萄糖之間的變旋。旋光現象產生的原因
 手性碳原子
手性碳原子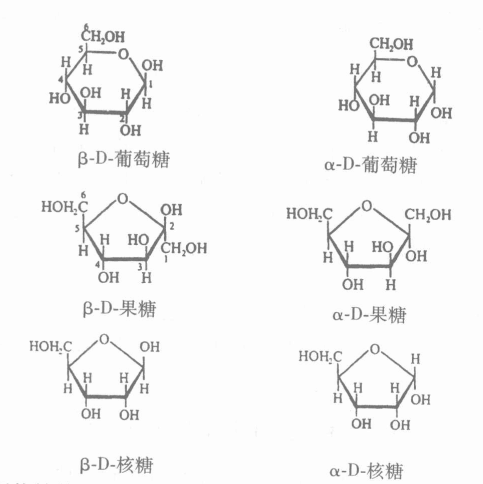 哈武斯(Haworth)式
哈武斯(Haworth)式 動態平衡
動態平衡變旋現象(英文:Mutarotation)是環狀單糖或糖苷的比旋光度由於其α-和β-端基差向異構體達到平衡而發生變化,即旋光度發生改變,最終達到一個穩定的平衡值的現象。變旋現象往往能被某些酸或鹼催化。
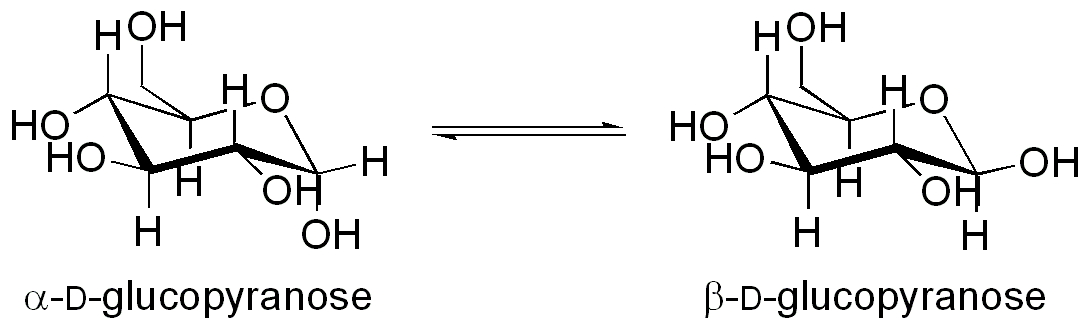 α-與β-D-吡喃葡萄糖之間的變旋。
α-與β-D-吡喃葡萄糖之間的變旋。 手性碳原子
手性碳原子 哈武斯(Haworth)式
哈武斯(Haworth)式 動態平衡
動態平衡變旋現象(英文:Mutarotation)是環狀單糖或糖苷的比旋光度由於其α-和β-端基差向異構體達到平衡而發生變化,即旋光度發生改變,最終達到一個穩定的平衡值的現象。...
變旋作用是指一個吡喃糖、呋喃糖或糖苷伴隨著它們的α-和β-異構形式的平衡而發生的比旋度變化。在生物化學中常常見到這種行為。...
葡萄糖的變旋現象,就是由於開鏈結構與環狀結構形成平衡體系過程中的比旋光度變化所引起的。在溶液中α-D-葡萄糖可轉變為開鏈式結構,再由開鏈結構轉變為β-D-...
D-型和L-型的蘇阿糖均有變旋現象 [1] 。參考資料 1. 邢其毅;裴偉偉;徐瑞秋;裴堅.基礎有機化學(第三版):高等教育出版社,2005 圖集 蘇阿糖圖冊 V百科往期...
當其溶於水時,會發生變旋現象。這種變旋現象是由於α氧環式和β氧環式中間經過開鏈式形成一個互變平衡體系而引起的。如下圖所示:糖的互變異構 ...
3. 旋光性及變旋現象一切糖類物質分子內都有手性碳原子,所以都具有旋光性,屬於“旋光活性物質”(或光學活性物質)。旋光活性物質使偏振光振動平面旋轉的角度稱為“...
這種二糖就沒有變旋現象和還原性,也不能生成糖脎,因此稱為非還原性二糖。 [2] 此外,三糖是水解後生成三分子的單糖。如棉子糖。澱粉是儲蓄物質,纖維素是組成...
α-異構體與β-異構體的互相轉化稱為變旋現象。α-異構體受端基異構效應影響而得到穩定。中文名 首選異構物(α,β差向異構物) 外文名 α,β-anomer[1] 目...
20.2糖類化合物的環狀結構和變旋現象 20.2.1糖類化合物的環狀結構 20.2.2糖類化合物的變旋現象 20.3糖類化合物的構象: 異頭碳效應 20.4自然界中存在的特...
α-異構體與β-異構體的互相轉化稱為變旋現象。α-異構體受端基異構效應影響而得到穩定。V百科往期回顧 詞條統計 瀏覽次數:次 編輯次數:6次歷史版本 最近更新...
α-異構體與β-異構體的互相轉化稱為變旋現象。α-異構體受端基異構效應影響而得到穩定。V百科往期回顧 詞條統計 瀏覽次數:次 編輯次數:5次歷史版本 最近更新...
這種雙糖就沒有變旋現象和還原性,也不能生成糖脎,因此稱為非還原性雙糖。V百科往期回顧 詞條統計 瀏覽次數:次 編輯次數:5次歷史版本 最近更新: 創建者:...
16.3單糖的性質16.3.1單糖的變旋現象16.3.2氧化反應16.3.3還原反應16.3.4糖脎的生成16.3.5差向異構化16.3.6羥基上的反應*16.3.7單糖的顯色反應...
D-赤蘚糖為糖漿狀液體,有變旋現象;比旋光度+1°→-14.5°(3天,水,C=11 )。L-赤蘚糖也為糖漿狀液體,有甜味,+11.5°→+ 30.5°(長期平衡,水,C=...
α-異構體與β-異構體的互相轉化稱為變旋現象。α-異構體受端基異構效應影響而得到穩定。在有機物中,差向異構體的區別通常位於單個非對稱碳原子上,一般地,這個...
多糖類一般不溶於水,無甜味,不能形成結晶,無還原性和變旋現象。多糖也是糖苷,所以可以水解,在水解過程中,往往產生一系列的中間產物,最終完全水解得到單糖。 中文...
=irahinc}e; pee}insu}er其晶體為止交品系無臭。有甜味。熔點I57 --- 160有變旋現象,旋光度毛a扮+1730 [ bruin )-y}a」穢+}f15.10 {22.$h, r=...
16.3單糖的性質16.3.1單糖的變旋現象16.3.2氧化反應16.3.3還原反應16.3.4糖脎的生成16.3.5差向異構化16.3.6羥基上的反應16.3.7單糖的顯色反應...
多糖類一般不溶於水,無甜味,不能形成結晶,無還原性和變旋現象。多糖也是糖苷,所以可以水解,在水解過程中,往往產生一系列的中間產物,最終完全水解得到單糖。...
1-5 葡萄糖溶液為什麼有變旋現象?1-6 在糖的化學中D、L、α、β、(+)、(-)各表示什麼?1-7 葡萄糖有鏈狀和環狀結構是根據什麼事實提出的?1-8 什麼是...
20.1糖類化合物的分類、命名與結構 20.2糖類化合物的環狀結構和變旋現象20.3糖類化合物的構象: 異頭碳效應20.4自然界中存在的特殊單糖 20.5單糖的反應...
14.6單糖的差向異構體: 變旋現象14.7單糖的反應14.8雙糖14.9多糖14.10其他重要的糖類14.11細胞表面的糖類與糖類疫苗14.12植物: 石油的替代物?連結甜味劑...
16.2.3單糖的環狀結構和變旋現象26416.2.4吡喃糖的構象26716.3單糖的化學性質26716.3.1氧化反應26716.3.2還原反應26816.3.3成脎反應269...
14.6單糖的差向異構體:變旋現象14.7單糖的反應14.8雙糖14.9多糖14.10其他重要的糖類14.11細胞表面的糖類與糖類疫苗14.12植物:石油的替代物?...
O-糖苷屬縮醛型結構,易被水解成相應的糖和配基。糖苷(不包括二糖)中無半縮醛羥基,故無變旋現象、無還原性,在鹼中較穩定。 [2] ...
