手性誘導又稱不對稱誘導是利用底物分子中的不對稱因素(手性中心)去誘導新的不對稱碳原子(乎性碳原子)的構型,使生成不等量的立體異構體。
基本介紹
- 中文名:手性誘導
- 外文名:chiral induction
- 學科:化學
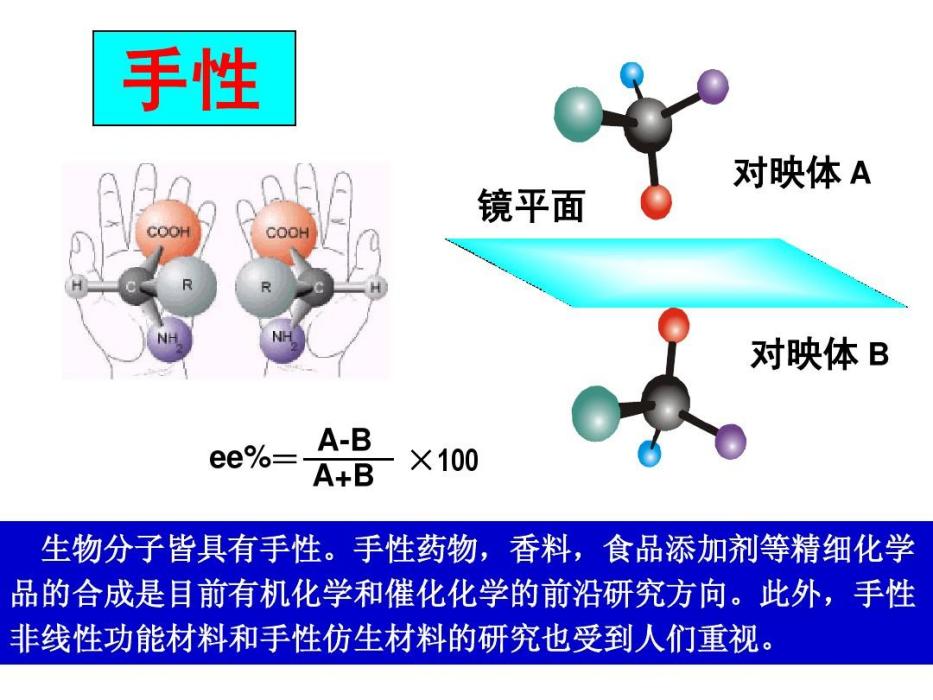
手性誘導又稱不對稱誘導是利用底物分子中的不對稱因素(手性中心)去誘導新的不對稱碳原子(乎性碳原子)的構型,使生成不等量的立體異構體。
手性誘導又稱不對稱誘導是利用底物分子中的不對稱因素(手性中心)去誘導新的不對稱碳原子(乎性碳原子)的構型,使生成不等量的立體異構體。定義手性誘導又稱不對稱誘導是利用底物分子中的不對稱因素(手性中心)去誘導新的不對稱碳原子...
《手性誘導合成手性金屬-生物分子多孔材料》是依託上海大學,由何翔擔任項目負責人的青年科學基金項目。中文摘要 手性多孔金屬-有機骨架材料在諸多領域都有著廣泛套用。利用手性誘導的方法製備手性物質,消除了對手性中心的依賴,給我們有目的...
《晶態手性超分子配合物中手性的誘導與傳遞的研究》是依託北京理工大學,由李暉擔任項目負責人的面上項目。項目摘要 本項目從分子對稱性和晶體對稱性的角度,以手性分子磁體為功能導向,設計合成具有各種分子識別作用和空間位阻效應的手性功能...
《新型支載化手性誘導試劑的合成及其套用研究》是依託湖北大學,由楊桂春擔任項目負責人的面上項目。項目摘要 本項研究設計以天然L-酪氨酸為手性源合成三類結構新穎的噻唑烷-2-硫酮、噁唑烷-2-硒酮、噁唑烷-2-苯亞胺手性單體,...
《手性“伴侶陰離子”誘導的不對稱催化反應》是依託中國人民解放軍第四軍醫大學,由張生勇擔任項目負責人的面上項目。中文摘要 以碳手性1,2-二醇、碳手性和螺環手性1,3-二醇、碳手性和軸手性1,4-二醇、螺環手性1,5-二醇、面手性...
手性源方法(Chiral pool)或者手性底物的誘導,該方法被稱為第一代手性合成方法,亦稱為底物控制法.它是通過底物中原有手性的誘導,在產物中形成新的手性中心.可簡略表述為:原料為手性化合物A*,經不對稱反應,得到另一手性化合物B*,即...
《手性氨基酚誘導的手性取代環胺的合成方法研究》是依託清華大學,由胡躍飛擔任項目負責人的面上項目。 項目摘要 特殊結構的有機小分子可對生物受體功能進行有效調控。手性環胺化合物是用此目的的分子類型之一。有關它們的合成和合成方法...
《光控客體手性小分子誘導聚合物螺旋結構研究》是依託中山大學,由楊建文擔任項目負責人的面上項目。 中文摘要 主鏈螺旋聚合物在生物醫藥、化學工業和光信息材料等領域具有強大套用潛力。按螺旋方向可分為左旋和右旋,多以手性側基或外源手性...
手性是自然界的基本屬性之一,與生命休戚相關。近年來,人們對單一手性化合物(如手性醫藥和農藥等)及手性功能材料的需求推動了手性科學的蓬勃發展。手性物質的獲得,除了來自天然以外,人工合成是主要的途徑。外消旋體拆分、底物誘導的手性...
《聚集誘導手性高分子設計與分子識別性質研究》是依託南京師範大學,由韋國擔任項目負責人的青年科學基金項目。項目摘要 以四苯乙烯為AIE活性官能團,並修飾較長烷烴鏈,增加溶解性。選擇手性聯萘酚、聯萘胺、環己二胺等手性基團,通過醛胺...
手性試劑法 手性試劑和前手性底物作用生成光學活性產物。目前,手性試劑誘導已經成為化學方法誘導中最常用的方法之一。如:q—蒎烯獲得的手性硼烷基化試劑已用於前列腺素中間體的製備。催化不對稱合成 在不對稱合成的諸多方法中,最理想的是...
深入研究了手性誘導程度對非對映體過量的影響,揭示摺疊體的動態平衡對其手性的影響,得到兩類具有單一螺旋性的摺疊體,為將來發展基於手性摺疊體的不對稱催化和圓偏振發光手性材料奠定理論基礎。另外,我們也合成了幾類具有陰離子識別性能的...
首先通過對DBSA/環己烷/水反相膠束體系、DBSA/CTAB復配體系等不同反應體系的研究,建立了血紅蛋白催化手性導電聚苯胺形成的條件。其次研究了血紅蛋白的結構和性質與手性導電聚苯胺形成之間的關係。研究結果顯示:在沒有其他手性誘導劑存在的...
在前期研究過程中,我們發現將手性小分子通過氫鍵作用複合到嵌段共聚物本體材料中,可以得到手性可控的手性納米螺旋結構。在本項目中,我們通過對手性誘導過程的調控機制的研究,成功製備了螺旋手性可控的單螺旋,雙螺旋以及環狀組裝納米結構。
至今已有1000餘個手性膦配體合成得到,而且人們對於手性氫化的機理、產生手性誘導的因素以及過渡金屬的作用等諸方面都進行了深入的研究。用過渡金屬催化的手性氧化,是Sharpless歷經十年努力才實現的催化性反應,成為了目前廣泛套用的手性合成...
項目合成了多種胺基酸卟啉及其金屬配合物;開展了手性胺基酸鐵卟啉的立體選擇性催化氧化研究。利用圓二色與磁圓二色光譜證實了手性胺基酸雙卟啉配合物存在二階磁手性效應(MChCD)。採用DeVoe極化率方法,建立了手性卟啉誘導圓二色光譜的激子...
《設計與合成新型雙、多卟啉及其在手性識別中的套用》是依託蘇州大學,由胡傳江擔任項目負責人的面上項目。項目摘要 手性識別是一種重要而特殊的分子識別,不僅對於從理論上闡述生命過程的化學本質具有重要理論意義,而且在手性誘導、記憶、...
許多具有生物活性的天然產物(如萜類、甾體類及生物鹼等)分子內都含有手性季碳中心,不對稱合成這些天然產物的關鍵問題之一是解決如何構築手性季碳中心。該研究項目利用手性源L-脯氨酸衍生物作為手性誘導物,與α-烴基-γ-(δ,ε)-...
不對稱誘導,是立體化學名詞,指在一個富手性的反應劑、化學試劑、催化物或環境的作用下,一個化學反應中的產物盡於某一種對映異構體或非對映異構體多於另一種。簡介 不對稱誘導,是立體化學名詞,指在一個富手性的反應劑、化學試劑、...
而手性催化、不對稱合成更是具有重大挑戰性的基礎和前沿研究方向。本項目擬結合上述幾方面的特點,從CO2參與的手性環狀碳酸酯電合成反應入手,圍繞手性誘導的立體選擇性和催化效率等核心問題,拓展不對稱電合成反應,詳細考察催化過程中的各...
新型手性無機材料的製備及其特有的手性選擇性質是本領域重要的研究課題。申請人在手性無機納米材料的設計合成和光學活性研究方面進行了深入細緻的研究,並發表了多項成果。本課題擬在前期課題基礎上,(1)通過控制結構導向分子、手性誘導分子...
《藥酶的誘導抑制對手性藥物異構體代謝的選擇性影響》是依託浙江大學,由劉志強擔任項目負責人的面上項目。項目摘要 本課題套用手性色譜學較系統地研究了氧氟沙星、安非他明類、苯妥英和普萘洛爾的體內體外立體選擇性代謝差異。實驗結果表明...
手性廣泛存在於自然界中,利用手性催化劑實現不對稱催化反應是製備手性化合物的最有效方法。本項目主要設計和合成新型的含過渡金屬的可見光手性催化劑,利用手性離子對效應,Lewis酸鹼效應和手性金屬絡合物骨架誘導手性,並實現一些環化或加成等...
利用柱芳烴類化合物在化學結構上、構象上以及對紫外光吸收上的特有性質,建立新型超分子手性誘導策略。通過該項目的實施可望實現光化學反應的高效手性誘導和立體選擇性可控的目標,並在以下幾方面獲得突破:1.合成具有對光反應底物有強包結...
非對映選擇性反應主要是指在反應體系不另外加入手性試劑,而是利用反應原料本身帶有手性,具有手性誘導作用,使得反應得到的產物表現出一定的對映選擇性的反應。Ostaszewski 等報導用 N保護具有手性的胺基酸來作為酸組分進行 PCR 反應,並考察...
handed sword 雙手劍 Single Handed 斷手記 Handed Swors 雙手劍 handed rule 安培右手定則 handed nut 右旋螺母 Mop handed 拖把桿 handed inducement 手性誘導 handed again 我不能再空著手回去了 ...
該研究有重要創新性及套用前景:光活性N-α,β-不飽和醯基-4-烴基四氫噻唑-2-硫酮的合成及在金屬試劑控制下進行的不對稱麥可加成反應,研究表明(R)-4-烴基四氫噻唑-2-硫酮手性誘導得到了(R)-β-苯基庚酸、(S)-4-烴基...
C2軸手性二膦化合物,用作手性反應誘導劑;2,2′-雙(二苯膦)-1,1′-二萘基及其銠和釕衍生物,具有高度選擇性均相催化劑,用於芳基酮,β-酮酯、α-氨基酮的還原反應;它們也用於不對稱羥基化反應以及烯烴的羥基形成反應,不對稱...
