概述
成體幹細胞: 存在於已分化組織中的未分化
細胞,可以自我更新,同時在一定的條件下也可以分化,產生各種特異的細胞類型。
成年動物的許多組織和器官,比如
表皮和
造血系統,具有修復和
再生的能力。成體
幹細胞在其中起著關鍵的作用。在特定條件下,成體幹細胞或者產生新的幹細胞,或者按一定的程式分化,形成新的功能細胞,從而使組織和器官保持生長和衰退的動態平衡。過去認為成體幹細胞主要包括
上皮幹細胞和
造血幹細胞。幹細胞,說明成體幹細胞普遍存在,問題是如何尋找和分離各種
組織特異性幹細胞。成體幹細胞經常位於特定的
微環境中。微環境中的
間質細胞能夠產生一系列生長因子或配體,與
幹細胞相互作用,控制幹細胞的更新和分化。
位於各種分化組織中未分化的幹細胞,這類幹細胞具有有限的自我更新和分化潛力。
優點分析
獲取相對容易
理論上,成體幹細胞致瘤風險很低,而且所受倫理學爭議較少
成體幹細胞還具有多向分化潛能
分化來源
研究人員已經在多種組織和器官內發現有成體
幹細胞的存在。關於成體幹細胞,有一點是非常重要的:在組織內只含有極少量的幹細胞。研究人員認為,幹細胞存在於組織的特定區域內,從而在數年內都維持靜止休眠狀態――也就是保持不分裂的狀態,直到組織受到損傷或發生疾病時被激活,才開始分裂。已經報導的含有幹細胞的成體組織包括:腦、骨髓、外周血液、血管、
骨骼肌、皮膚和肝臟。
檢測方法
科學家尚未就成體
幹細胞的鑑定標準達成一致,然而,經常被採用的鑑定方法包括:
 幹細胞的分化
幹細胞的分化1)利用
分子標記在活體組織中對細胞進行標記,然後確定它們所產生的特定細胞類型。
2)將細胞從活體動物上分離出來,在對其進行
細胞培養的過程中進行標記,之後將細胞移植入另一個動物體內,觀察該細胞是否可以再生其來源組織。
3)分離細胞,進行細胞培養,並對其分化進行控制,通常採用加入生長因子或向細胞內引入新基因的方法,進而觀察
細胞的分化方向。
研究歷史
成體
幹細胞的研究始於20世紀60年代人們對
造血幹細胞(hematopoietic stem cells, HSC)的研究。HSC 是目前研究得最為清楚、套用最為成熟的成體幹細胞,它移植治療
血液系統及其他系統
惡性腫瘤、自身免疫病和
遺傳性疾病等均取得令人矚目的進展,極大促進了這些疾病的治療,同時也為其他類型成體幹細胞的研究和套用奠定了堅實的基礎。成體幹細胞的套用研究是
再生醫學的一個重要組成部分,是很多疾病可供選擇的治療手段,同時又是一個多學科交叉的領域,需要分子和細胞生物學家、胚胎學家、病理學家、臨床醫生、
生物工程師和倫理學家等的共同參與。隨著對成體幹細胞可塑性研究的不斷深入和臨床套用研究的不斷擴展,成體幹細胞最終走向臨床套用的希望越來越大。
可塑性
隨著成體
幹細胞研究的深入,研究者觀察到成體幹細胞可以突破其“發育限制性”,跨系,甚至跨
胚層分化為其他類型組織細胞。例如,骨髓來源的幹細胞在特定環境中可向肝臟、
胰腺、肌肉及神經細胞分化;肌肉、
神經幹細胞也可向
造血細胞分化。人們稱這種現象為“幹細胞的可塑性”。
造血系統發育分化一直被認為是有嚴格的層次等級,多能的具有自我更新能力的HSC在最頂端,定向
祖細胞居於中間位置,而各個終末分化的細胞位於最底層;但是這個關於
幹細胞分化的經典模型受到嚴峻的挑戰,Blay 等對成體幹細胞可塑性的研究表明,這種分級分化模型已不再正確。成體幹細胞的這種特性為其在多種難治性、終末期疾病的治療中套用帶來希望。關於成體幹細胞可塑性仍然存在爭議,其中成體幹細胞
異質性假說和
細胞融合假說分別對幹細胞的可塑性提出了質疑,並有相關的實驗證據支持這種質疑。不過,成體幹細胞的跨系,甚至跨
胚層分化的能力,使得通過誘導成體幹細胞能得到各種我們所需要的細胞,用於各種疾病的治療,這為成體幹細胞治療研究進一步加溫,掀起了又一輪的熱潮。
 成體幹細胞的可塑性
成體幹細胞的可塑性比較研究
套用前景廣闊
與胚胎幹細胞相比,成體幹細胞具有許多優勢:
1、胚胎幹細胞具有
全能性和可以建系傳代等優點,因此理論上套用前景廣闊。但實際上由於每個個體的主要組織相容性複合體(
MHC)不同,同種異體
胚胎幹細胞及其分化組織細胞用於臨床會引起
免疫排斥,因此基於胚胎幹細胞的治療方案要求對患者進行長期
免疫抑制劑治療或將患者的
造血系統和外來細胞形成
嵌合體。
造血細胞,但小鼠胚胎幹細胞的實驗表明,來源於胚胎幹細胞的造血細胞在體內無法重建造血機制,因而限制了臨床套用。為了解決免疫排斥的問題,研究人員探索將患者的
體細胞核移植到去核的健康供體
卵細胞中,在體外克隆並隨後發育分化產生攜帶患者自己MHC的胚胎幹細胞。這些胚胎幹細胞及其衍生組織移植後不會產生
免疫排斥,因此可以用於患者病變組織及其功能的重建,這就是
治療性克隆。但一些研究觀察到,胚胎幹細胞發育分化過程中具有極高的
非整倍體發生率,美國
麻薩諸塞州耶尼德研究組的最新研究發現,克隆動物的基因在構成沒有缺陷的情況下,也不能像正常動物基因一樣準確表達出來,也就是說,克隆動物存在無法正確生長發育的危險。正是這個原因,造成當前98%的
動物克隆實驗失敗,而順利降生的克隆動物也經常出現體重超重等異常。研究還發現,利用當前的
克隆技術取患者體細胞核的細胞克隆培育出來的新組織一樣會存在缺陷,這項技術還有待完善、成熟。
體細胞克隆所需的
卵細胞難以獲得,成體
幹細胞則可從患者自身獲得,而不存在組織相容性的問題,治療時可避免長期套用
免疫抑制劑對患者的傷害。此外,少量的骨髓切除治療有助於形成部分造血嵌合,可使異體成體幹細胞的治療成為可能。
非定位性
2、雖然胚胎幹細胞能分化成各種細胞類型,但這種分化是“非定位性”的。當前尚不能控制胚胎幹細胞在特定的部位分化成相應的細胞,當前的做法容易導致
畸胎瘤。在套用胚胎幹細胞治療前,必須先進行初步的細胞誘導分化,以防止畸胎瘤的發生。套用胚胎幹細胞時,也必須確認胚胎幹細胞供者沒有諸如(肌)營養失調症之類的
遺傳性疾病。相對而言,成體
幹細胞不存在上述問題,例如
骨髓移植實驗並不引發畸胎瘤。
高度分化能力
3、成體
幹細胞也具有類胚胎幹細胞的高度
分化能力。現已建立了幹細胞平台技術,從肌肉、肝臟、骨髓中成功地發現和分離了成體幹細胞群,完成了幹細胞定向誘導分化成骨、
軟骨、神經細胞、
心肌細胞和
血管內皮細胞的研究;當前又研究發現,從
胰腺等組織可分離出
間充質表型的成體幹細胞群,具有多系分化潛能,國內外尚未見相關報導。另外,在體內和體外實驗證實,間充質表型幹細胞群可在幹細胞調控因子誘導下轉化成
造血幹細胞。在上述研究工作的基礎上,又提出了成體
幹細胞研究的新假說,即在人體發育的過程中,成體幹細胞是存留在多種組織中、具有多系
分化能力的
亞全能幹細胞群體,這些細胞都具有相同或相似的細胞
表型,在適合的
微環境下可分化成多種組織細胞。成體幹細胞移植是治療
血液系統疾病、先天性
遺傳疾病以及多發性和
轉移性惡性腫瘤疾病的最有效方法。
 胚胎幹細胞
胚胎幹細胞胚胎幹細胞優勢
但胚胎幹細胞也存在自身的優勢:
1、胚胎幹細胞能
永生化,可以傳代建系,且增殖能力強,來源充沛。
2、雖然成體
幹細胞具有向多系分化的能力,但這種分化的“效率”尚不理想。通過體外的擴增培養能提高轉化效率,但是體外的轉化是否會引起成體幹細胞遺傳變化還有待證實,而且這種分化是否是成體幹細胞多系分化的結果尚無法肯定。即使是成體幹細胞多系分化的結果,我們也不明了是何種信號誘導了整個過程的發生。而胚胎幹細胞的研究已經有三十多年的歷史。鼠胚胎幹細胞的研究已經證明了胚胎幹細胞的
全能性。相應的信號誘導機制的研究也取得了長足的進展。當前鼠胚胎幹細胞的研究成果給正在進行的人體胚胎幹細胞研究很大的助力。成體
幹細胞和胚胎幹細胞各有自身的優勢和缺陷。對於一個實驗室而言,同時開展對兩者的研究,不僅是可能的,而且能互為裨益,相得益彰。兩者的研究對幹細胞領域而言都是必要的。
疾病治療
心肌疾病
很多心臟疾病都可以通過各種治療手段得到有效的治療,但過量功能
心肌細胞的喪失導致的
心功能不全,仍然是影響疾病
預後的主要問題。同種異體
心臟移植非常昂貴,而且供體來源少,移植後的
心臟非常脆弱,不可能作為晚期
心力衰竭的常規治療方法。成體幹細胞治療的研究通過在受損傷的心臟中產生新的有功能的心肌細胞來修復受損傷的
心肌,治療心力衰竭。套用幹細胞治療心力衰竭通常被簡單地認為是產生新的心肌細胞,但實際上要複雜的多。心力衰竭通常是由特定的原因產生的,這些原因必須被消除,這是任何試圖重建心肌的努力成功的前提條件。更重要的是,與
骨髓移植不同,心肌的基本功能單位不僅僅是由單獨心肌細胞完成,而是由多種細胞互相配合共同完成的。幹細胞治療產生的
心肌細胞必須以正確的方向整合,避免導致心肌纖維排列紊亂(因為這本身就是一種病態);必須能通過
毛細血管網獲得營養;必須能夠被蒲肯野纖維系統激活產生快速有規律的電激活,以防止興奮折返和獨立的自發
起搏點活動;必須具有
交感神經興奮性等。總之,通過幹細胞治療心臟疾病面臨的挑戰遠遠大於
骨髓移植和輸血治療,離真正的臨床套用尚有待時日,需要開展全面、系統的研究。
 人體胚胎幹細胞群
人體胚胎幹細胞群神經退行性疾病
成體
幹細胞及其子代細胞移植或動員腦組織內的幹細胞被認為是將來治療
神經退行性疾病的有效方法。考慮到
人腦結構和功能的複雜性,通過替代疾病中丟失的細胞來恢復損傷的功能聽起來是不現實的,然而動物模型研究已證實
神經元替代修復損壞的神經通路是可行的,臨床試驗研究也證實在人腦中細胞替代治療同樣能達到症狀緩解。成體幹細胞用於治療帕金森氏病、中風、肌萎縮性側索硬化症、亨廷頓氏舞蹈病,甚至精神分裂症等神經系統疾病均進行了大量的基礎和試驗研究。帕金森氏病可能是研究最充分和效果最為肯定的。成體幹細胞治療神經退行性疾病的研究仍處在起始階段,必須謹慎前行,避免對患者開展無科學依據的臨床試驗。需要認真研究控制
幹細胞增殖的關鍵分子,以防止
神經幹細胞的
過度生長,當然還需要知道,如何更好地實現移植細胞與已存在的
神經突觸網路的功能整合。為進一步開展研究,使之最終走向臨床套用,需要儘快建立能夠很好地模擬人類
神經退行性疾病的動物模型。
骨骼疾病
臨床實踐中經常會遇到大範圍的
骨缺損,如在創傷、炎症和腫瘤外科手術治療以後等。重建大範圍的骨缺損仍是臨床治療面臨的一個難題,當前尚沒有有效的治療手段,骨髓來源
幹細胞及其他來源幹細胞都可以分化得到
成骨細胞,通過將細胞與支架材料結合後移植於受損部位,用於修復骨骼缺損的實驗研究首先在小動物體內實現,隨後在大動物體內亦得到證實,證明了成體幹細胞套用於修復
骨缺損的可行性,隨後的臨床試驗研究證明,此方法是治療骨骼疾病的一種有效方法。

肝臟疾病
早在60多年前研究者就認為在成體肝臟中存在著肝
幹細胞,但直到現在仍然存在爭議,很大一部分原因是沒有肝幹細胞的特異性基因得到確認,以及在部分嚴重
肝損傷後的
肝再生不需要激活肝乾/
祖細胞,成熟的原本處於
靜止期的
肝細胞通過分裂也能很大程度發揮肝再生的作用。成體幹細胞治療
肝臟疾病的另一個可能途徑是利用
造血幹細胞的跨系、跨
胚層分化能力誘導得到肝細胞。齧鼠動物的HSCs 在肝損傷模型中植入肝臟後能夠分化為有功能的肝細胞,並參與肝組織修復,在動物體內開展的研究結果是令人振奮的,但是臨床套用需要更確實的證據,證明人的HSCs在進行肝臟移植後具有和齧鼠動物同樣的特性。
成體神經幹細胞
工程研究
期刊簡介:
雜誌發表關於幹細胞;組織構建;生物材料;骨關節植入物;組織器官細胞移植以及計算機輔助數位化技術的套用基礎及臨床研究,轉化醫學和偱證醫學研究,表中國組織工程研究領域一流水平的學術、技術創新成果。
研究對象
研究內容
幹細胞研究的生物學特性、培養與分化、誘導技術、幹細胞與微環境、幹細胞與微小RNA調節、
幹細胞因子及相關因子、幹細胞表型與鑑定、
幹細胞移植與
免疫耐受、細胞移植與
基因表達、細胞編程與
表觀遺傳、幹細胞保存與質量、幹細胞實驗動物模型等學術和技術的熱點問題。
 幹細胞的分化
幹細胞的分化 成體幹細胞的可塑性
成體幹細胞的可塑性 胚胎幹細胞
胚胎幹細胞 人體胚胎幹細胞群
人體胚胎幹細胞群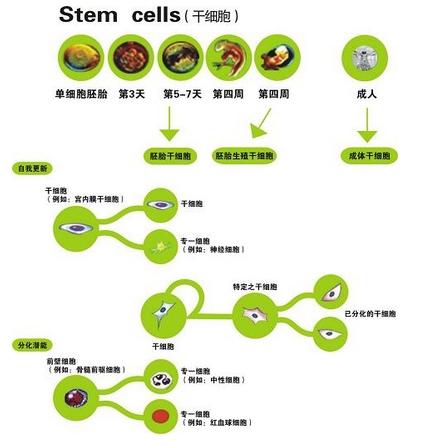
 幹細胞的分化
幹細胞的分化 成體幹細胞的可塑性
成體幹細胞的可塑性 胚胎幹細胞
胚胎幹細胞 人體胚胎幹細胞群
人體胚胎幹細胞群