簡易儀器,溫度計,托盤天平,試管,燒杯,燒瓶,蒸餾燒瓶,錐形瓶,漏斗,廣口瓶,細口瓶,燃燒匙,蒸發皿,酒精燈,本生燈,量筒,集氣瓶,滴管,滴瓶,曲頸瓶,表面皿,石棉網,玻璃棒,鐵架台,滴定管,泥三角,複雜儀器,啟普發生器,酒精噴燈,布氏漏斗,坩堝鉗,索氏提取器,索氏提取裝置,布氏燒瓶,砂芯漏斗,三梁天平,冷凝管,洗瓶,克氏燒瓶,稱量瓶,乾燥器,鹽橋,
簡易儀器
溫度計
溫度計是用於測量溫度的儀器。其種類很多,有數碼式溫度計,熱敏溫度計等。而實驗室中常用玻璃液體溫度計。
溫度計可根據用途和測量精度分為標準溫度計和實用溫度計2類,標準溫度計的精度高,它主要用於校正其它溫度計。實用溫度計是指所供實際測溫用的溫度計,主要有實驗用溫度計、工業溫度計、氣象溫度計、醫用溫度計等。中學常用棒式工業溫度計。其中酒精溫度計的量程為100℃,水銀溫度計用200℃和360℃2種量程規格。
使用注意事項
 溫度計
溫度計(1)應選擇適合測量範圍的溫度計。嚴禁超量程使用溫度計。
(2)測液體溫度時,溫度計的玻璃泡應完全浸入液體中,但不得接觸容器壁,測蒸汽溫度時玻璃泡應在液面以上,測蒸餾餾分溫度時,玻璃泡應略低於蒸餾燒瓶支管。
(3)在讀數時,視線應與液柱彎月面最高點(水銀溫度計)或最低點(酒精溫度計)水平。
(4)禁止用
溫度計代替
玻璃棒用於攪拌。用完後應擦拭乾淨,裝入紙套內,遠離熱源存放。
托盤天平
托盤天平是用來粗略稱量物質質量的一種儀器,每架天平都成套配備法碼一盒。
中學實驗室常用載重100 g(感量為0.1 g)和200 g(感量為0.2 g)2種。載重又叫載物量,是指能稱量的最大限度。感量是指天平誤差(±),例如感量為0.1 g的托盤天平。表示其誤差為±0.1 g,因此它就不能用來稱量質量小於0.1 g的物品。
使用注意事項
 托盤天平
托盤天平(1)稱量前應將天平放置平穩,並將游碼左移至刻度尺的零處,檢查天平的擺動是否達到平衡。如果已達平衡,指針擺動時先後指示的標尺上左、右兩邊的格數接近相等。指針靜止時則應指在標尺的中央。如果天平的擺動未達到平衡,可以調節左、右平衡螺母使擺動達到平衡。
(2)稱量物不能直接放在托盤上,應在2個托盤上分別放一張大小相同的同種紙,然後把要稱量的試劑放在紙上稱量。潮濕的或具有腐蝕性的試劑必須放在玻璃容器(如表面皿、燒杯或稱量瓶)里稱量。
(3)把稱量物放在左盤,砝碼放在右盤,砝碼要用鑷子夾取。先加質量大的砝碼,再加質量小的砝碼,最後可移動游碼,直至指針擺動達到平衡為止。
(4)稱量完畢後,應將砝碼依次放回
砝碼盒中。把游碼移回零處。
試管
規格:試管分普通試管、具支試管、離心試管等多種。普通試管的規格以外徑(mm)×長度(mm)表示,如5×150、18×180、25×200等。離心試管以容量毫升數表示。主要用途:普通試管用作少量試劑的反應容器、收集少量氣體、裝配小型氣體發生器。使用注意事項:普通試管可以直接加熱。裝溶液時不超過試管容量的1/2,加熱時不超過試管的1/3。加熱時必須用試管夾,夾在接近試管口部位。加熱時先使試管均勻受熱,然後在試管底部加熱,並不斷移動試管。這時應將試管傾斜約45。 加熱使用試管夾、試管口不能對著人,管口不要對著有人的方向。受熱要均勻以免暴沸或試管炸裂.加熱後不能驟冷,防止破裂。主要用途:(1)盛取液體或固體試劑.(2)加熱少量固體或液體. (3)製取少量氣體反應器. (4)收集少量氣體用. (5)溶解少量氣體、液體或固體的溶質.
 試管
試管試管是用作少量試劑的反應容器,也可用於收集少量氣體。試管根據其用途常分為平口試管、翻口試管和具支試管等。平口試管適宜於一般化學反應,翻口試管適宜加配橡膠塞,具支試管可作氣體發生器,也可作洗氣瓶或少量蒸餾用。
試管的大小一般用管外徑與管長的乘積來規定,常用為10×l00 mm、12×l00 mm、15×l50 mm、18×180 mm、20×200 mm和32×200 mm等。
使用注意事項
(1)使用前要預熱:
(2)使用試管時,應根據不同用量選用大小合適的試管。徒手使用試管套用拇、食、中三指握持試管上沿處。振盪時要腕動臂不動:
(3)盛裝液體加熱,不應超過容積的3分之一 ,並與桌面成45”角,管口不要對著自己或別人。若要保持沸騰狀,可加熱液面附近:
(4)盛裝粉末狀試劑,要用藥匙(或紙槽)送入管底,盛裝粒狀固體時,應將試管傾斜,使粒狀物沿試管壁慢慢滑入管底;
(5)夾持試管應在距管口 處。加熱時試管外部應擦乾水分,不能手持試管加熱。加熱後,要注意避免驟冷以防止炸裂:
(6)加熱固體試劑時,管底應略高於管口,防止冷凝水倒流使試管炸裂,完畢時,應繼續固定或放在石棉網上,讓其自然冷卻。
燒杯
燒杯通常用作反應物量較多時的反應容器。此外也用來配製溶液,加速物質溶解,促進溶劑蒸發等。燒杯的種類和規格較多,中學常用低型燒杯。為了在使用時便於添加一定量的液體,在一些燒杯外壁上印有白色的容積標線,,這種燒杯叫印標燒杯,有的叫它刻度燒杯。其分度並不十分精確,允許誤差一般在±5%,所以在分度表上印有“APPROX”字樣,它表示“近似容積”,因此,不能作量器使用。燒杯的規格以容積大小區分,常用為50 mL、100 mL、250 mL、500 mL等多種。
 燒杯
燒杯使用注意事項
(1)燒杯所盛溶液不宜過多,約為容積的1/2,但在加熱時,所盛溶液不能超過容積的1/3 。
(2)燒杯不能幹燒,在盛有液體時方能較長時間加熱,但必須墊上石棉網。
(3)拿燒杯時,要拿外壁,手指勿接觸內壁。拿加熱時的燒杯,要用燒杯夾。
(4)需用玻璃棒攪拌燒杯內所盛溶液時,應沿杯壁均勻旋動玻璃棒,切勿撞擊杯壁與杯底。
(5)燒杯不宜長期存放化學試劑,用後應立即洗淨、擦乾、倒置存放。
燒瓶
燒瓶是用作反應物較多且需較長時間加熱的、有液體參加反應的容器。其瓶頸口徑較小,配上塞子及所需附屬檔案後,也常用來發生蒸氣或作氣體發生器。燒瓶的用途廣泛,因此型式也有多種,中學常用圓底燒瓶和平底燒瓶2種。
 圓底燒瓶
圓底燒瓶圓底燒瓶一般用作加熱條件下的反應容器。而平底燒瓶用於不加熱條件下的氣體發生器,也常用來裝配洗瓶等。由於平底燒瓶底部平面較小,其邊緣又有棱,因此應力較大,加熱時容易炸裂。所以它一般不用於加熱條件下的反應容器。
燒瓶的規格以容積大小區分,常用為150 mL、250 mL和500 mL幾種。
使用注意事項
(1)圓底燒瓶底部厚薄較均勻,又無棱出現,可用於長時間強熱使用。
(2)加熱時燒瓶應放置在石棉網上,不能用火焰直接加熱。
(3)實驗完畢後,應撤去熱源,靜止冷卻後,再行廢液處理,進行洗滌。
蒸餾燒瓶
蒸餾燒瓶屬於燒瓶類,所不同者,在於瓶頸部位有一略向下的支管,它專用作蒸餾液體的容器。
 蒸餾燒瓶
蒸餾燒瓶蒸餾燒瓶有減壓及常壓2類。常壓蒸榴燒瓶也分支管在瓶頸上部、中部和下部的3種,蒸餾沸點較高的液體,選用支管在瓶頸下部的蒸餾燒瓶,沸點較低的則用支管在上都的蒸餾燒瓶。而支管位於瓶頸中者,常用來蒸餾一般沸點的液體。
蒸餾燒瓶的規格以容積大小區別,常用為150 mL和250 mL 2種。
使用注意事項
(1)配置附屬檔案(如溫度計等)時,應選用合適的橡膠塞,特別要注意檢查氣密性是否良好。
(2)加熱時應放在石棉網上,使之均勻受熱。
錐形瓶
錐形瓶又叫錐形燒瓶或稱三角燒瓶。
 錐形瓶
錐形瓶錐形瓶瓶體校長,底大而口小,盛入溶液後,重心靠下,極便於手持振盪,故常用於容量分析中作滴定容器。實驗室也常用它裝配氣體發生器或洗瓶。
錐形瓶的大小以容積區分,常用為150ml、250ml等幾種。
使用注意事項
(1)振盪時,用右手姆指、食指、中指握住瓶頸,無名指輕扶瓶頸下部,手腕放鬆,手掌帶動手指用力,作圓周形振動。
(2)錐形瓶需振盪時,瓶內所盛溶液不超過容積的 1/2。
(3)若需加熱錐形瓶中所盛液體時,必須墊上石棉網。
漏斗
普通型
漏斗是一個筒型物體,被用作把液體及幼粉狀物體注入入口較細小的容器。在漏斗咀部較細小的管狀部份可以有不同長度。漏斗通常以不鏽鋼或塑膠製造,但紙制漏斗亦有時被使用於難以徹底清洗的物質,例如引擎機油。一些漏斗在咀部設有可控制的活門,讓使用者可控制流質流入的速度。有時會使用濾紙以隔濾結晶物等化學物質。
 三角漏斗
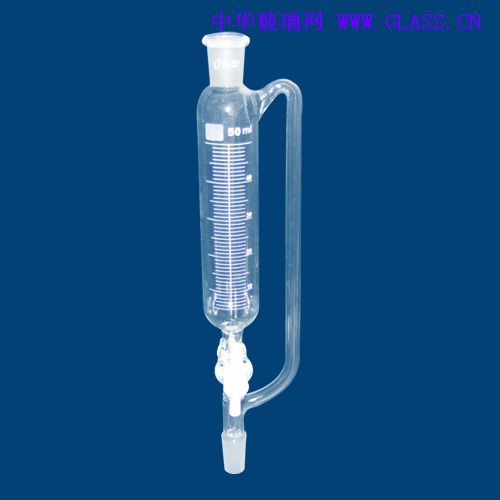
三角漏斗分液型
一種玻璃實驗器皿,特別是涉及一種做化學實驗用的
分液漏斗。包括斗體,蓋在斗體上口的斗蓋。斗體的下口安裝一三通結構的活塞,活塞的兩通分別與兩下管連線。使用本實用新型,可使實驗操作過程利於控制,減少勞動強度,當需要分離的液體量大時,只需搬動活塞的三通便可將斗體內的兩種液體同時流至下管,無需更換容器便可一次完成。在國中階段分液漏斗的主要作用則是控制化學反應的速率。本裝置是科學研究、化學實驗中一種功能較好的實驗器皿。
 分液漏斗
分液漏斗長頸型
漏斗的一種,主要用於固體和液體在錐形瓶中反應時添加液體藥品.一般還可以用
分液漏斗替代。
在使用時,注意漏斗的底部要在液面以下,這是為了防止生成的氣體從長頸漏斗口逸出,起到液封的作用。做實驗室製取二氧化碳和氧氣等實驗時會用到長頸漏斗。注意事項:試驗後應該清洗乾淨,避免有藥物殘留使下次實驗造成偏差。
 長頸漏斗
長頸漏斗廣口瓶
廣口瓶是用於盛放固體試劑的玻璃容器,有透明和棕色兩種,棕色瓶用於盛放需避光保存的試劑(例如硝酸銀)。廣口瓶一般用於存放試劑,瓶口內部磨砂,用於與瓶塞配合使用。
 廣口瓶
廣口瓶.不能用於加熱。
取用試劑時,瓶塞要倒放在桌上,用後加塞塞緊,必要時密封。由於瓶口內側磨砂,跟玻璃磨砂塞配套,因而玻璃塞的廣口瓶不能盛放強鹼性試劑。如果盛放鹼性試劑,要改用橡皮塞,因為強鹼的氫氧根離子與玻璃中的二氧化矽反應,生成物使口與塞粘連。
擺放時標籤向外。
細口瓶
細口瓶是用於盛放液體試劑的玻璃容器,有透明和棕色兩種,棕色瓶用於盛放需避光保存的試劑。細口瓶一般用於存放試劑,瓶口內部磨砂,用於與瓶塞配合使用。
不能用於加熱。
取用試劑時,瓶塞要倒放在桌上,取較多量試劑時,直接將試劑倒入容器,傾倒時,標籤向著手心。取較少量試劑時,使用滴管滴加。用後加塞塞緊,必要時密封。由於瓶口內側磨砂,跟玻璃磨砂塞配套,因而玻璃塞的廣口瓶不能盛放強鹼性試劑。如果盛放鹼性試劑,要改用橡皮塞,因為強鹼的氫氧根離子與玻璃中的二氧化矽反應,生成物使口與塞粘連。
擺放時標籤向外。
燃燒匙
燃燒匙大多由鐵絲和銅質小勺鉚合而成。用於盛放可燃性固體物質作燃燒試驗,特別是物質在氣體中的燃燒反應。燃燒匙在使用時,如果匙中盛放的物質(如:硫)能和鐵,銅反應,應盛放一層細沙 。

細砂是鋪在燃燒匙的裡邊,就如同我們平時用的勺子一樣,裡邊放砂子,但勺子一直朝上,砂子是不會掉下來的。鋪砂子的目的主要是在燃燒匙和藥品之間鋪一個保護層,從而防止藥品腐蝕燃燒匙。 燃燒匙是可以直接放在酒精燈上進行操作的儀器之一。很多的實驗儀器是不可以直接放在酒精燈上的,譬如
燒杯、燒瓶、錐形瓶。試管、坩堝、蒸發皿和燃燒匙是可用來直接加熱的儀器。
蒸發皿
用於蒸發濃縮溶液或
灼燒固體的器皿。口大底淺,有圓底和平底帶柄的兩種。最常用的為瓷製蒸發皿,也有
玻璃、
石英、鉑等製成的。質料不同,耐腐蝕性能不同,應根據溶液和固體的性質適當選用。對酸、鹼的穩定性好,可耐高溫,但不宜驟冷。
 蒸發皿
蒸發皿分無柄蒸發皿和有柄蒸發皿兩種,規格以直徑表示,有60~150mm等多種。
主要用途
能耐高溫,但不能驟冷,應使用坩堝鉗取放蒸發皿,加熱時用三腳架或鐵架台固定。液體量多時可直接在火焰上
使用注意事項
(1)加熱後不能驟冷,防止炸裂。
(2)加熱後不能直接放到實驗桌上,應放在石棉網上,以免燙壞實驗桌。
(3)液體量多時可直接加熱 ,量少或黏稠液體要墊石棉網或放在泥三角上加熱。
(4) 加熱蒸發皿時要不斷的用玻璃棒攪拌,防止液體局部受熱四處飛濺。
(5)加熱完後,需要用坩堝鉗移動蒸發皿。
(6)大量固體析出後就熄滅酒精燈,用餘熱蒸乾剩下的水分。
(7)加熱時,應先用小火預熱,再用大火加強熱。
(8)要使用預熱過的坩堝鉗取拿熱的蒸發皿。
酒精燈
酒精燈是以酒精為燃料的加熱工具,用於加熱物體。酒精燈由燈體、燈芯管和燈帽組成。酒精燈的加熱溫度400—500℃,適用於溫度不需太高的實驗,特別是在沒有煤氣設備時經常使用。
 酒精燈
酒精燈以
酒精(60%-75%乙醇溶液,C2H5OH)為燃料的加熱工具,用於加熱物體。
組成:酒精燈由燈壺、燈芯、燈芯管、酒精和燈帽組成。
酒精燈的容積:100ml,150ml。
(1)酒精燈是由燈帽、燈芯和盛有酒精的燈壺三大部分所組成。
(2)正常使用的酒精燈火焰應分為焰心、內焰和外焰三部分。加熱時套用外焰加熱。近年來的研究表明:酒精燈火焰溫度的高低順序為:外焰>內焰>焰心。 理論上一般認為酒精燈的外焰溫度最高,由於外焰與外界大氣充分接觸,燃燒時與環境的能量交換最容易,熱量釋放最多,致使外焰溫度高於內焰。
(3)若要燈焰平穩,並適當提高溫度可加金屬網罩。
使用注意事項
(1)絕對禁止向燃著的酒精燈里添加酒精,以免失火;
(2)絕對禁止用燃著的酒精燈引燃另一隻酒精燈;
(3)用完酒精燈之後,必須用燈帽蓋滅,不可用嘴去吹;
(4)不要碰倒酒精燈,萬一灑出的酒精在桌上燃燒起來,不要驚慌,應立刻用濕抹布撲蓋;
(5)酒精燈內酒精不應超過容積的2/3。
本生燈
德國化學家R.W.
本生的助手為裝備
海德堡大學化學實驗室而發明的用煤氣為燃料的加熱器具。在本生燈發明前,所用煤氣燈的火焰很明亮,但溫度不高,是因煤氣燃燒不完全造成的。本生將其改進為先讓煤氣和空氣在燈內充分混合,從而使煤氣燃燒完全,得到無光高溫
火焰。火焰分三層:內層為水蒸氣、一氧化碳、氫、二氧化碳和氮、氧的混合物,溫度約300℃,稱為焰心。中層內煤氣開始燃燒,但燃燒不完全,火焰呈淡藍色,溫度約500℃,稱還原焰。外層煤氣燃燒完全,火焰呈淡紫色,溫度可達800~900℃,稱為氧化焰,此處的溫度最高,故加熱時利用氧化焰。
 本生燈
本生燈使用步驟:
1.把實驗室的窗戶打開,保持空氣流通,避免強光照射。
3.先把燈腳的空氣調節器關閉,並點燃
火柴在出氣口上。
5.打開空氣調節器讓新鮮空氣進入,火焰轉為藍色及溫度變
高。
量筒
量筒(graduated cylinder, measuring cylinder or graduated glass) 是用來量取液體的一種玻璃儀器。量筒是量度液體體積的儀器。規格以所能量度的最大容量(ml)表示,常用的有10 ml、25ml、50 ml、100 ml、250 ml、500 ml、1000 ml等。外壁刻度都是以 ml為單位,10 ml量筒每小格表示0.2 ml,而50 ml量筒每小格表示1ml。可見量筒越大,管徑越粗,其精確度越小,由視線的偏差所造成的讀數誤差也越大。所以,實驗中應根據所取溶液的體積,儘量選用能一次量取的最小規格的量筒。分次量取也能引起誤差。如量取70ml液體,應選用 100ml量筒。
 量筒
量筒注意事項:
(1)讀數時,視線與凹液面最低點相齊平。
(2)量筒無零刻度線。
(3)不能加熱,不能作反應容器。
集氣瓶
一種廣口玻璃容器,瓶口平面磨砂,能跟毛玻璃保持嚴密接觸,不易漏氣。用於收集氣體、裝配洗氣瓶和進行物質跟氣體之間的反應。

注意事項
不能加熱
本儀器不可加熱,加熱容易炸裂,如需加熱需要用
圓底燒瓶和
燒杯。
鋪細沙或水
物質在集氣瓶中燃燒時要在瓶底鋪細沙或水,以防炸裂。
部分物質燃燒只能用沙土不能用水,如Na,濺落的Na與水反應放出氫氣,被點燃後易爆炸
尾氣處理
如果燃燒生成物包含有污染的氣體或煙霧需要進行處理,如
紅磷燃燒後蓋上玻璃片,防止五氧化二磷煙刺激呼吸道;硫燃燒後產生二氧化硫,瓶底要放氫氧化鈉溶液進行吸收。
滴管
用途
注意事項
滴加時,滴管要保持垂直於容器正上方,避免傾斜,切忌倒立,
不可伸入容器內部,不可觸碰到容器壁。除吸取溶液外,管尖不能接觸其他器物,以免雜質沾污。不可一管二用。
普通滴管用完需要清洗,而專用滴管不可清洗,需專管專用,防止污染試劑,用完就放回原試劑瓶即可。
使用時,不要只用拇指和食指捏著,用中指和
無名指夾住。
滴瓶
當使用的液體化學藥品每次的用量很少,或者是很容易發生
危險時,則多會選用
滴瓶來盛裝該溶液。通常液態的
酸鹼指示劑都是裝在滴瓶中使用。滴瓶瓶口內側
磨砂,與
細口瓶類似,瓶蓋部分用
滴管取代。
用來裝使用量很小的液體的容器,大多數在實驗室內使用。
 透明滴瓶
透明滴瓶注意事項
1.滴瓶上的滴管與滴瓶配套使用。
2.滴瓶上的滴管不要用水沖洗。
3.不可長時間盛放強鹼(玻璃塞),不可久置強氧化劑。
4.吸上的藥品剩餘不可倒回。
5.滴管不可倒放、橫放,以免試劑腐蝕滴管。
6.滴液時,滴管不能放入容器內,以免污染滴管,損傷容器。
 棕色滴瓶(裝見光易分解的溶液用)
棕色滴瓶(裝見光易分解的溶液用)曲頸瓶
曲頸瓶也叫曲頸瓶或稱曲頸甄(zèng),它是一件歷史較久、實用而簡單的儀器,除僅有的一個有磨口玻璃塞外,容器和曲頸相連,線條流暢,一氣呵成。它用作反應容器或蒸餾器。

曲頸瓶的最大優點是結構簡單,它可通過接受器與玻璃容器相連,或直接與斜置燒瓶相連,其間不需橡膠塞或橡膠管連給,所以耐腐蝕。例如:實驗室制硝酸時,可從塞口先放入固體硝酸鈉,再由此加入適當濃硫酸、塞緊瓶塞,微熱,蒸出的硝酸蒸氣直接由曲頸進入接受器,同時冷凝為液體。不致因連線處有橡膠製品而遭到硝酸腐蝕老化造成漏氣事故。
曲頸瓶的大小以容積區別,常用為125 mL、250 mL和500 mL幾種。
使用注意事項
(1)若需在鐵架台上固定時,應使其瓶塞在最上面,鐵夾來持曲頸近容器部位,讓曲頸自然與桌面成一夾角。
(2)加熱時必須墊上石棉網。
(3)實驗結束後,必須固定靜置,待其冷卻後,先將殘留物從曲頸口傾出,再從瓶塞口加水,反覆衝倒、洗淨、放置。
表面皿
表面皿是
玻璃制的,圓形狀,中間稍凹,與
蒸發皿相似。可以用來做一些蒸發液體的工作,它可以讓液體的表面積加大,從而加快蒸發。但是不能像蒸發皿那樣加熱。可以作蓋子,蓋在蒸發皿或
燒杯上,防止灰塵落入蒸發皿或燒杯;可以作容器,暫時呈放固體或液體試劑,方便
取用;可以作承載器,用來承載
pH試紙,使滴在
試紙上的酸
液或
鹼液不
腐蝕實驗台。
 表面皿
表面皿使用方法
先將
表面皿洗淨、烘乾才能使用。表面皿的用途很廣,但無論代替何種儀器使用,均要按照各種儀器的使用方法使用。如作氣室鑑定時,將兩片表面皿,利用磨成的平面合成氣室,用一張試劑浸濕的試紙,貼附在上面的一片表面皿上,被鑑定的化合物放在下面的一片表面皿上,必要時加溫,觀察反應中生成氣體,從試劑的顏色改變來鑑定氣體。如觀察白色沉澱或混濁物時,可把表面皿底壁放一張
黑紙,則白色生成物便可清晰可見。如做各種儀器蓋子,只要利用它的弧形放在儀器口上,放穩即可,但要注意按儀器的口徑選擇表面皿。一般表面皿直徑應大於儀器口徑ICm ,這樣使用較方便。如做燒杯蓋子,按燒杯容量選用不同直徑的表面皿。
注意事項
不能加熱。
 玻璃表面皿
玻璃表面皿石棉網
火焰長時間集中在容器的某個地點,最終會使容器爆裂.用了石棉網,火焰的熱量會分散到容器的每個角落,長時間燒容器也不會
爆裂。因為石棉不是可燃性物質,鐵絲可將火焰的熱量分散到空氣里,傳到容器上方,熱量均勻。
玻璃棒
化學實驗中使用,玻璃質細長棒狀簡易
攪拌器,也稱為
玻棒用來加速
溶解,促進互溶,引流,蘸取液體,在
蒸發皿中攪拌以防止因受熱不均勻而引起的飛濺等。尤以中學實驗中最為常用,是必不可少的實驗用品。
 玻璃棒
玻璃棒作用
1、在過濾等情況下轉移液體的導流
2、用於溶解、蒸發等情況下的攪拌
3、對液體和固體的轉移
4、過濾(引流)
5、引發反應,如引燃紅磷
6、使熱量均勻散開
鐵架台
鐵架台用於固定和支持各種儀器,
鐵環可代替
漏斗架使用。一般常用於過濾、加熱、滴定等實驗操作。是物理、化學實驗中使用最廣泛的儀器之一。常與
酒精燈配合使用。

使用方法:實驗時常常會用到較長的
滴定管或是要放置
燒杯加熱,此時就要藉助
鐵架台將這些裝置架在適宜的高度,以利實驗的進行。要支撐滴定管時,鐵架台上要夾一個滴定管夾,滴定管就可夾在滴定管夾上固定。要放置燒杯時,鐵架台上則要夾一個
鐵環,鐵環上再放置
石棉網,燒杯則放在石棉網上。
滴定管
 滴定管
滴定管滴定管(burette)分為鹼式滴定管和
酸式滴定管。前者用於量取對玻璃管有侵蝕作用的液態試劑;後者用於量取對橡皮有侵蝕作用的液體。滴定管容量一般為50mL,刻度的每一大格為1mL,每一大格又分為10小格,故每一小格為 0.1mL。精確度是百分之一。即可精確到0.01ml . 滴定管為一細長的管狀容器,一端具有活栓開關,其上具有
刻度指示量度。一般在上部的刻度讀數較小,靠底部的讀數較大。
泥三角
泥三角由三根鐵絲彎成,套有三截素燒瓷管,形如三角形而得名。它有大、小之分,視坩堝大小而選用。以耐熱陶瓷管和鐵線纏繞而成的三角形支撐物,用來支撐
坩堝以利加熱,防止炸裂。

泥三角因有耐熱的陶瓷管包著因此可耐高溫,而其中空的
管柱內又有鐵絲穿過故可承受重量。當有需要用本生燈強熱的物體時,通常都會將泥三角置於鐵環上做為該物的支撐。或者在需要酒精燈加熱坩堝的實驗中使用。
複雜儀器
啟普發生器
一種實驗室常用的氣體發生裝置,是荷蘭科學家
啟普(Petrus Jacobus Kipp 1808~1864)發明,並以他的姓命名。它用普通
玻璃製成,構造見圖。它由球形
漏斗、容器和
導氣管三部分組成。適用於
塊狀固體與液體在
常溫下反應
製取氣體,如氫氣、
硫化氫等。
如果生成氣體難溶於反應液,可以使用。如二氧化碳可溶於水,但難溶於鹽酸;故用石灰石與鹽酸反應制二氧化碳時可用啟普發生器。
 啟普發生器
啟普發生器注意:啟普發生器不能用於加熱!
氣密性檢查
方法:開啟旋塞,向球形漏斗中加水。當水充滿容器下部的半球體時,關閉旋塞。繼續加水,使水上升到長頸漏斗中。靜置片刻,若水面不下降,則說明裝置氣密性良好,反之則說明裝置漏氣。漏氣處可能是容器上氣體出口處的橡皮塞、導氣管上的旋塞或長頸漏斗與容器接觸的磨口處。如漏氣,應塞緊橡皮塞或在磨口處塗上一薄層
凡士林。
具體操作
固體試劑由容器上的氣體出口加入,加固體前應在容器的球體中加入一定量的玻璃棉或放入橡膠墊圈,以防固體掉入半球體中。加固體的量不得超過球體容積的1/3。液體試劑從長頸漏斗口注入,注液方法與上述注水方法相同。液體的量以反應時剛剛
浸沒固體,
液面不高過
導氣管的橡膠塞為宜。
使用時,打開導氣管上的
旋塞,
長頸漏斗中的液體進入容器與固體反應,氣體的
流速可用旋塞
調節。停止使用時,關閉旋塞,容器中的氣體壓力增大,將液體壓回長頸漏斗,使液體和固體脫離,反應停止。為保證安全,可在
球形漏斗口加
安全漏斗,防止氣體
壓力過大時炸裂容器。
 啟普發生器
啟普發生器特點:
符合“隨開隨用、隨關隨停”的原則。能
節約藥品,控制反應的發生和停止,可隨時向裝置中添加液體藥品。
酒精噴燈
常用的酒精
噴燈有座式酒精噴燈和掛式酒精噴燈兩種。座
式酒精噴燈的
酒精貯存在燈座內,掛式噴燈的酒精貯存罐懸掛於高處。酒精噴燈的
火焰溫度可達1000℃左右。使用前,先在
預熱盆中注入酒精,點燃後銅質
燈管受熱;待盆中酒精將近燃完時,開啟燈管上的開關(逆時針轉);來自貯罐的酒精在燈管內
受熱氣化,跟來自氣孔的空氣混合;
這時用火點燃管口氣體,就產生高溫火焰;調節開關閥來控制火焰的大小。用畢後,掛式噴燈座旋緊開關,同時關閉酒精
貯罐下的活塞,就能使燈焰熄滅。
構造
學校實驗室用的座式酒精噴燈,由燈管、空氣調節器、引火碗、螺旋蓋、貯酒精罐等部分構成(如圖)。
火焰溫度在800℃左右,最高可達1000℃,每耗用酒精200毫升,可連續工作半小時左右。
使用
1.旋開加注酒精的螺旋蓋,通過
漏斗把酒精倒入貯酒精罐。為了安全,酒精的量不可超過罐內容積的80%(約200毫升)。隨即將蓋旋緊,避免
漏氣。然後把燈身傾斜70度,使燈管內的燈芯沾濕,以免燈芯燒焦。
2.
燈管內的酒精蒸氣噴口直徑為0.55毫米,容易被灰粒等堵塞,堵塞後就不能引燃,所以每次使用前要檢查噴口,如發現堵塞,就應該用通針或細鋼針把噴口刺通。
 掛式酒精噴燈
掛式酒精噴燈3.在引火碗內注2/3容量的酒精,用火柴把酒精點燃,對燈管加熱(此時要轉動空氣調節器把入氣孔調到最小),待酒精氣化,從噴口噴出時,引火碗內燃燒的火焰便可把噴出的酒精蒸氣點燃。如不能點燃,也可用火柴來點燃。
4.當噴口火焰點燃後,再調節空氣量,使火焰達到所需的溫度。在一般情況下,進入的空氣越多,也就是
氧氣越多,火焰溫度越高。
5.熄滅噴燈,可用事先準備的廢木板平壓燈管上口,火焰即可熄滅,然後墊著布旋鬆螺旋蓋(以免燙傷),使罐內溫度較高的
酒精蒸氣
逸出。
注意
1.噴燈工作時,燈座下絕不能有任何熱源,環境溫度一般應在35℃以下,周圍不要有易燃物。
2.當罐內酒精耗剩20毫升左右時,應停止使用,如需繼續工作,要把噴燈熄滅後再增添酒精,不能在噴燈燃著時向罐內
加注酒精,以免引燃罐內的酒精蒸氣。
3.使用噴燈時如發現罐底凸起,要立即停止使用,檢查噴口有無堵塞,酒精有無溢出等,待查明原因,排除故障後再使用。
4.每次
連續使用的時間不要過長。如發現燈身溫度升高或罐內酒精
沸騰(有氣泡破裂聲)時,要立即停用,避免由於罐內
壓強增大導致
罐身崩裂。
 酒精噴燈
酒精噴燈布氏漏斗
布氏漏斗是實驗室中使用的一種陶瓷儀器,也有用塑膠製作的,用來使用真空或負壓力抽吸進行過濾。普遍認為發明者為1907年
諾貝爾化學獎獲得者
愛德華·比希納,事實上布氏漏斗是由化學家Ernst Büchner發明的。
形狀為扁圓筒
狀,
圓筒
底面上開了很多
小孔。下連一個狹長的筒狀出口。
使用的時候,一般先在圓筒底面墊上
濾紙,將漏斗插進
布氏燒瓶上方開口並將接口密封(例如用橡膠環)。布氏燒杯的側口連抽氣系統。然後將欲分離的固體、液體混合物倒進上方,液體成分在
負壓力作用下被抽進燒杯,固體留在上方。常用於
有機化學實驗中
提取結晶。這種情況的過濾完成後,還可以在上方用少量純溶劑來洗掉結晶表面的雜質。
 布氏漏斗
布氏漏斗坩堝鉗
坩堝鉗(crucible tongs),一種常見的化學儀器。通常用來夾取
坩堝。一般由不鏽鋼,或不可燃、難氧化的硬
質材料製成。
 坩堝鉗
坩堝鉗 注意事項
1.必須使用乾淨的坩堝鉗。
2.用坩堝鉗夾取灼熱的坩堝時,必須將鉗尖先
預熱,以免坩堝因局部
冷卻而破裂,用後鉗尖應向上放在桌面或
石棉網上。
3.實驗完畢後,應將
坩堝鉗擦乾淨,放入實驗器材櫃中,乾燥
放置。
5.坩堝鉗不一定與坩堝配合使用。
索氏提取器
主詞條:索氏提取器
索氏提取器是由
提取瓶、提取管、
冷凝器三部分組成的,提取管兩側分別有
虹吸管和
連線管,各部分連線處要嚴密不能漏氣。提取時,將待測樣品包在脫脂濾紙包內,放入提取管內。提取瓶內加入
石油醚,加熱提取瓶,石油醚氣化,由連線管上升進入冷凝器,凝成液體滴入提取管內,浸提樣品中的脂類物質。待提取管內石油醚液面達到一定高度,溶有
粗脂肪的石油醚經虹吸管流入提取瓶。流入提取瓶內的石油醚繼續被加熱氣化、上升、冷凝,滴入提取管內,如此循環往復,直到抽提完全為止。
 索氏提取器
索氏提取器 從固體物質中萃取化合物的一種方法是,用溶劑將固體長期浸潤而將所需要的物質浸出來,即
長期浸出法。此
法花費時間長.溶劑用量大、效率不高。
萃取前先將固體物質研碎,以增加固
液接觸的面積。然後,將固體物質放在濾紙包內,置於提取器中,提取器的下端與盛有浸出溶劑的圓底燒瓶相連,上面接回流
冷凝管。
加熱圓底燒瓶,使溶劑
沸騰,蒸氣通過連線管上升,進入到
冷凝管中,被冷凝後滴入提取器中,溶劑和固體接觸進行萃取,當提取器中溶劑液面達到虹吸管的最高處時,含有萃取物的溶劑虹吸回到燒瓶,因而萃取出一部分物質。然後圓底燒瓶中的浸出溶劑繼續蒸發、冷凝、浸出、回流,如此重複,使固體物質不斷為純的浸出溶劑所萃取,將萃取出的物質富集在燒瓶中。 液—固萃取是利用溶劑對固體混合物中所需成分的溶解度大,對雜質的溶解度小來達到提取
分離的目的。
 索氏提取器
索氏提取器索氏提取裝置
索氏提取裝置,又稱脂肪抽取裝置或脂肪抽出裝置。將液體滴入提取管內,如此循環往復,直到抽提完全為止。
 索氏提取裝置
索氏提取裝置布氏燒瓶
形狀類似錐形瓶,但有兩個不同:側面有一個細頸,與真空泵連線。為了抗衡真空造成的負氣壓,
布氏燒瓶的壁比錐形瓶要厚。
抽濾瓶的外形極似
錐形瓶,只是在管口處多開了一個側向的連線口,用來接上塑膠管再接到水流抽氣幫浦(即水流抽氣泵)上。當抽濾瓶口放上
漏斗過濾時,此時水流抽氣幫浦(即水流抽氣泵)開始抽氣,使抽濾瓶內的空氣壓力降低;若漏斗上的濾紙內有任何的溶液存在,由於大氣壓力和重力的作用,這些溶液即會經過濾紙流入下方的抽濾瓶中,殘餘的固體則留在
濾紙上,而達到過濾的目的。利用吸濾瓶過濾時,通常使用瓷漏斗置於其上,不能用錐
形漏斗。還可以用
吹風機對著濾紙吹,加快氣流,從而加速
抽濾過程。
砂芯漏斗
注意事項
1、新購置的
濾過儀器使用前需用酸溶液進行抽濾,並用蒸餾水沖洗乾淨,烘乾後使用。對於除菌濾器,使用前需
高壓滅菌,使用後套用洗滌液進行
抽濾,然後放入洗滌液中浸泡48小時,取出用
蒸餾水沖洗、抽濾、
烘乾、
保存。在烘乾過程中,切勿中途開
烘箱,要待烘箱降至室溫後再打開烘箱取出,以防炸裂。
三梁天平
三梁天平因其有三支具
刻度的橫桿
量尺而得名。三梁天平有三組騎碼但沒有砝碼 先使用刻度最大的騎碼若指針沒歸零再調較小刻度的騎碼。三梁天平有三支橫桿,每支橫桿各有不同質量的
砝碼置於其上,移動砝碼的位置即可調整以天平支點為中心,和物體相對邊的
抗力大小。待
測物則盛裝在稱量紙或是稱量盤內再放於天平的稱盤上。
 三梁天平
三梁天平 使用方法
B.零點校正:把天平橫桿支點下方之
固定鎖鎖住,再將三根橫桿上的砝碼放置在零刻度的刻齒或刻度上。打開固定鎖,使橫桿自由擺動,當橫桿靜止時,橫桿最右端之水平指針是否指在標度盤之中央零點上?如果指針恰好指在零
標度,則天平已
歸零,可以使用。如果指針指在零標度的下方,則鎖住固定鎖,旋轉
平衡調整器之調整螺使向左移,一直到打開固定鎖而指針恰指在零標度為止。如果指針指在零標度的上方,
則使調整螺向右
移。
C.測質量(
稱重):鎖住固定鎖,把等測物體置於物盤中央,如果物體會腐蝕稱物盤,則用適當容器或紙張盛墊。預估物體的質量(重量),把
砝碼移在預估質量的相應刻度上,打開固定鎖,由指針之平衡位置判定物體質量是大於或小於預估質量,改變或移動三根橫桿上砝碼的位置,直至橫桿平衡靜止時,指針恰指在零標度。而由三根橫桿上之砝碼位置,讀記物體的質量值。
D.重複上述各步驟,測量待測物體之質量三次,求取
平均值,並用有效數字表示其質量大小。
冷凝管
利用熱交換原理使冷凝性氣體冷卻凝結為液體的一種
玻璃儀器。有直形、球形、蛇形三種,規格以長度(mm)表示,有150~300等多種。
用途
使用範圍:蒸汽的溫度大於140攝氏度,用空氣
冷凝管,溫度小於140攝氏度,用直形冷凝管。
冷凝管通常使用於欲在回流狀況下做實驗的
燒瓶上或是欲蒐集冷凝後的液體時的
蒸餾瓶上。蒸氣的冷凝發生在內管的內壁上。內外管所圍出的空間則為行水區有吸收蒸氣熱量並將這熱量移走的功用。進水口處通常有較高的水壓,為了防止水管脫落,塑膠管上應以管束綁緊。當在回流狀態下使用時,冷凝管的下端玻璃管要插入一個橡皮塞,以便能塞入燒瓶口中,承接燒瓶內往上蒸發的蒸氣。
回流冷凝管
有易揮發的液體反應物時,為了避免反應物損耗和充分利用原料,要在發生裝置設計冷凝回流裝置,使該物質通過冷凝後由
氣態恢復為液態,從而回 流並收集。實驗室可通過在發生裝置安裝長玻璃管或冷凝回流管等實現。
 回流冷凝管
回流冷凝管直形冷凝管
由內外組合的直
玻璃管構成,多用於蒸餾操作蒸汽溫度小於140度,不可用於回流。在其外管的上下兩側分別有連線管接頭,用作出水口和進水口。
使用方法:使用時,將靠下端的連線口以塑膠管接上水龍頭,當作進水口。因為進水口處的水溫較低而被蒸氣加熱過後的水,溫度較高;較熱的水因密度降低會自動往上流,有助於冷卻水的循環。
 直形冷凝管
直形冷凝管空氣冷凝管
空氣冷凝管和直形冷凝管主要是蒸出產物時使用(包括蒸餾和分餾),當蒸餾物沸點超過140度時,一般使用空氣冷凝管,以免直形冷凝管通水冷卻導致玻璃溫差大而炸裂。
球形冷凝管
內管為若干個
玻璃球連線起來,用於有機製備的
回流,適用於各種沸點的液體。
長期使用後,隔套中的
鐵鏽可以用鹽酸洗去。缺點:
冷凝後的液體凝固後容易卡在玻璃球中。由於進水口水壓較高所以膠管容易脫落,使用時要用
鐵絲綁住。
 球形冷凝管
球形冷凝管蛇形冷凝管
洗瓶
化學實驗室中用於裝
純水的一種容器,並配有發射細液流的裝置。常用的有吹出型和擠壓型兩種。吹出型由平底玻璃燒瓶和瓶口裝置一短吹氣管和長的出水管組成;
擠壓型由塑膠
細口瓶和
瓶口裝置出水管組成。
 洗瓶
洗瓶 洗瓶用於溶液的定量轉移和
沉澱的
洗滌和轉移。經濟洗瓶(常用500ml經濟洗瓶)、安全洗瓶(蒸餾水洗瓶、甲苯洗瓶、乙醇洗瓶、甲醇洗瓶、丙酮洗瓶、異丙醇洗瓶、
次氯酸鈉洗瓶)、耐溶劑
洗瓶,塑膠洗瓶(紅)(即紅嘴洗瓶)
克氏燒瓶
1883年發明測定
有機化合物中氮含量的方法:他將一定重量的試樣與硫酸作用,使試樣中的氮全部轉變為硫酸銨,然後往
硫酸銨溶液中加入
鹼,再將生成的
氨蒸餾到一定體積的標準酸溶液中,再滴定過量的酸,就能測出試樣的含氮量。此法普遍用於化學和醫學研究及農業生產和藥物工業。後人稱此法為
克氏定氮法。
 克氏燒瓶
克氏燒瓶此法所用的儀器是一種梨形長頸燒瓶,容量通常約300毫升,微量分析用的可以小到10毫升,後人稱這種燒瓶為
克氏燒瓶。
稱量瓶
磨口塞的筒
形玻璃瓶,用於差減法
稱量試樣的容器。因有磨口塞,可以防止瓶中的
試樣吸收空氣中的水分和
CO2等,適用於稱量易吸潮的試樣。
 稱量瓶
稱量瓶 稱量瓶的蓋子是磨口配套的,不得丟失、弄亂。稱量瓶使用前應洗淨烘乾,不用時應洗淨,在磨口處墊一小紙,以方便打開
蓋子。
稱量瓶主要用於使用
分析天平時稱取一定質量的
試樣,也可用於烘乾試樣。稱量瓶平時要洗淨,烘乾,存放在乾燥器內以備隨時使用。稱量瓶不能用火直接加熱,
瓶蓋不能互換,稱量時不可用手直接拿取,應帶指套或墊以潔淨紙條。
常見的稱量瓶有高型和扁型兩種,高型的瓶高40mm至60mm不等;扁型的瓶高40mm至60mm不等。扁
型用作
測定水分或在
烘箱中
烘乾基準物;高型用於稱量基準物、樣品。
稱量瓶不可蓋緊磨口塞
烘烤,
磨口塞要
原配。
 扁型稱量瓶
扁型稱量瓶乾燥器
乾燥器是通過加熱使物料中的濕分(一般指水分或其他可揮發性液體成分)
汽化逸出,以獲得規定濕含量的固體物料的機械設備。
 真空乾燥器
真空乾燥器注意事項
(2)搬移乾燥器時,要用雙手拿著,用
大拇指緊緊按住
蓋子。
(3)打開乾燥器時,不能往上掀蓋,套用左手按住乾燥器,右手小心地把蓋子稍微推開,等冷空氣徐徐進入後,才能完全推開,蓋子必須仰放在桌子上。
(4)不可將太熱的物體放入乾燥器中。
(5)有時較熱的物體放入乾燥器中後,空氣受熱膨脹會把蓋子頂起來,為了防止蓋子被打翻,應當用手按住,不時把蓋子稍微推開。
(6)灼燒或烘乾後的坩堝和沉澱,在乾燥器內不宜放置過久,否則會因吸收一些水分而使質量略有增加。
 乾燥器的結構
乾燥器的結構(7)
變色矽膠乾燥時為藍色,受潮後變粉紅色。可以在120℃烘受潮的矽膠待其變藍後反覆使用,直至破碎不能用為止。
鹽橋
鹽橋常出現在原電池中,是由瓊脂和飽和氯化鉀或飽和硝酸銨溶液構成的。用來在兩種溶液中轉移電子。常用於
原電池實驗,材料:
瓊脂+飽和
氯化鉀溶液或飽和
硝酸銨溶液。 為了減小液界電位,通常在兩種溶液之間連線一個高濃度的電解質溶液作“鹽橋”。
作用原理:
在兩種溶液之間插入鹽橋以代替原來的兩種溶液的直接接觸,減免和穩定液接
電位(當組成或活度不同的兩種
電解質接觸時,在溶液接界處由於正負離子擴散通過界面的離子遷移速度不同造成正負電荷分離而形成雙電層,這樣產生的電位差稱為液體接界擴散電位,簡稱液接電位),使液接電位減至最小以致接近消除。 防止試液中的有害離子擴散到參比電極的內鹽橋溶液中影響其電極電位。
原理:
飽和KCl溶液的濃度高達4.2mol·dm-3,當鹽橋插入到濃度不大的兩電解質溶液之間的界面時,產生了兩個接界面,鹽橋中K+和Cl-向外擴散就成為這兩個接界面上離子擴散的主流。由於K+和Cl-的擴散速率相近,使鹽橋與兩個溶液接觸產生的液接電勢均很小,且兩者方向相反,故相互抵消後降至1~2mV。 選擇鹽橋中的電解質的原則是高濃度、正負離子遷移速率接近相等,且不與電池中溶液發生
化學反應。常採用KCl、NH4NO3和KNO3的飽和溶液。
 溫度計
溫度計 托盤天平
托盤天平 試管
試管 燒杯
燒杯 圓底燒瓶
圓底燒瓶 蒸餾燒瓶
蒸餾燒瓶 錐形瓶
錐形瓶 三角漏斗
三角漏斗 分液漏斗
分液漏斗 長頸漏斗
長頸漏斗 廣口瓶
廣口瓶
 蒸發皿
蒸發皿 酒精燈
酒精燈 本生燈
本生燈 量筒
量筒
 透明滴瓶
透明滴瓶 棕色滴瓶(裝見光易分解的溶液用)
棕色滴瓶(裝見光易分解的溶液用)
 玻璃表面皿
玻璃表面皿 滴定管
滴定管 啟普發生器
啟普發生器 啟普發生器
啟普發生器 掛式酒精噴燈
掛式酒精噴燈 布氏漏斗
布氏漏斗 索氏提取器
索氏提取器 索氏提取裝置
索氏提取裝置 回流冷凝管
回流冷凝管 直形冷凝管
直形冷凝管 克氏燒瓶
克氏燒瓶 扁型稱量瓶
扁型稱量瓶 乾燥器的結構
乾燥器的結構

 滴管
滴管 表面皿
表面皿 石棉網
石棉網 玻璃棒
玻璃棒

 酒精噴燈
酒精噴燈 坩堝鉗
坩堝鉗 索氏提取器
索氏提取器 布氏燒瓶
布氏燒瓶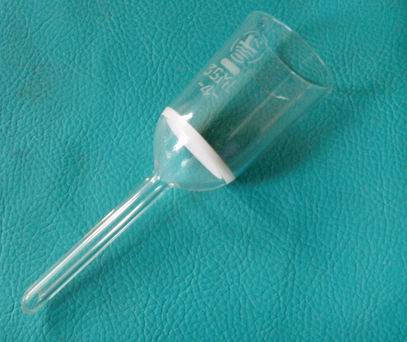 砂芯漏斗
砂芯漏斗 三梁天平
三梁天平 球形冷凝管
球形冷凝管 蛇形冷凝管
蛇形冷凝管 洗瓶
洗瓶 稱量瓶
稱量瓶 真空乾燥器
真空乾燥器