結構 在
脫氧核糖核酸 和
核糖核酸 中,起配對作用的部分是含氮鹼基。5種鹼基都是雜環化合物,氮原子位於環上或取代氨基上,其中一部分(取代
氨基 ,以及嘌呤環的1位氮、嘧啶環的3位氮)直接參與鹼基配對。鹼基共有5種:
胞嘧啶 (縮寫作C)、
鳥嘌呤 (G)、
腺嘌呤 (A)、
胸腺嘧啶 (T,DNA專有)和
尿嘧啶 (U,RNA專有)。顧名思義,5種鹼基中,腺嘌呤和鳥嘌呤屬於嘌呤族(縮寫作R),它們具有雙環結構。胞嘧啶、尿嘧啶、胸腺嘧啶屬於嘧啶族(Y),它們的環系是一個六元雜環。RNA中,尿嘧啶取代了胸腺嘧啶的位置,值得注意的是,胸腺嘧啶比尿嘧啶多一個5位甲基,這個甲基增大了遺傳的準確性。
鹼基置換類型及缺失和插入突變示意圖 鹼基通過共價鍵與核糖或脫氧核糖的1位碳原子相連而形成的化合物叫核苷。核苷再與磷酸結合就形成核苷酸,磷酸基接在五碳糖的5位
碳原子 上。
新成員 上世紀80年代初,由這四種“經典”DNA鹼基組成的家族中迎來了第五名成員:甲基
胞嘧啶 (mC),其源於胞嘧啶。mC的出現引發了科學家們極大的關注,並獲得了廣泛的研究。上世紀90年代後期,mC被廣泛看成是表觀遺傳機制的主要原因:它能夠根據每個組織的生理需要,打開或關閉基因。而且,隨著研究的進一步深入,科學家們現在知道,作為一種重要的表觀遺傳修飾,mC參與基因表達調控、X-染色體失活、基因組印記、轉座子的長期沉默和癌症的發生。
近日,西班牙科學家在最新出版的《細胞》雜誌上撰文指出,或許存在著第六種鹼基——甲基腺嘌呤(mA),其主要作用是確定表觀基因組的性質,並因此在細胞的
生命 過程中發揮重要作用。
據每日科學網4日報導,西班牙Bellvitge生物醫學研究所表觀遺傳學和癌症生物學計畫負責人、巴塞隆納大學遺傳學教授曼奈·埃特雷在《細胞》雜誌上發表文章,描述了第六種鹼基——mA存在的可能性,他認為,這種鹼基也幫助確定表觀基因組,並因此在細胞生命過程中發揮著重要作用。
埃特雷在論文中表示:“早在數年前,我們就知道,在我們生物學上的遠親——細菌的基因組內就存在mA,主要作用保護其免受其他生物體遺傳物質的入侵,但當時科學家們認為,這一現象只出現在原始細胞內。”
埃特雷繼續解釋說:“現在《細胞》雜誌發表的三篇論文表明,藻類、蠕蟲以及蒼蠅都擁有mA,這些生物的細胞像人體細胞一樣都是真核細胞,說明人體細胞內也可能擁有第六種鹼基。研究表明,mA的主要功能是調控某些基因的表達,因此,構成了一種新的表觀遺傳標記。在我們所描述的這些基因組內,mA的濃度都很低,但隨著擁有高靈敏度分析方法的發展,使得這項研究成為了可能。除此之外,mA可能也在幹細胞和發育初期發揮重要作用。”
種類 近幾年,有人將表觀遺傳學修飾——5-胞嘧啶甲基稱為第5種鹼基,5-羥甲基胞嘧啶(5-hmC)稱為第6種鹼基。在最新的研究成果中,研究人員發現了第7種,和第8種DNA鹼基:5-胞嘧啶甲醯(5-formylcytosine),5-胞嘧啶羧基(5-carboxylcytosine)。這兩種鹼基實際上都是由胞嘧啶經由張毅教授研究組一直研究的關鍵蛋白:Tet蛋白修飾後形成。
作用 組成DNA DNA(脫氧核糖核酸)的結構出奇的簡單。DNA分子由兩條很長的糖鏈結構構成骨架,通過鹼基對結合在一起,就象梯子一樣。整個分子環繞自身中軸形成一個雙螺旋。兩條鏈的空間是一定的,為2nm。在形成穩定螺旋結構的鹼基對中共有4種不同鹼基。根據它們英文名稱的首字母分別稱之為A(ADENINE 腺嘌呤)、T(THYMINE 胸腺嘧啶)、C(CYTOSINE 胞嘧啶)、G(GUANINE 鳥嘌呤),另有U(URACIL尿嘧啶)。DNA與RNA共有的鹼基是腺嘌呤、胞嘧啶和鳥嘌呤。胸腺嘧啶存在於DNA中,而尿嘧啶則存在於RNA中。每種鹼基分別與另一種鹼基的化學性質完全互補,嘌呤是雙環,嘧啶是單環,兩個嘧啶之間空間太大,而嘌呤之間空間不夠。這樣A總與T配對,G總與C配對。這四種化學“字母”沿DNA骨架排列。“字母”(鹼基)的一種獨特順序就構成一個“詞”(
基因 )。每個基因有幾百甚至幾萬個鹼基對。
鹼基 嘌呤和嘧啶都有酮-烯醇式互變異構現象,一般生理pH條件下呈酮式。 AGCT(U)四種鹼基在DNA中的排列遵循
鹼基互補配對原則 有些核酸中含有修飾鹼基(或稀有鹼基),這些鹼基大多是在上述嘌呤或嘧啶鹼的不同部位甲基化(methylation)或進行其它的化學修飾而形成的衍生物。例如有些DNA分子中含有5-甲基胞嘧啶(m5C),5-羥甲基胞嘧啶(hm5C)。某些RNA分子中含有1-甲基腺嘌呤(m1A)、2,2-二甲基鳥嘌呤(m22G)和5,6-二氫尿嘧啶(DHU)等。
構成物質 鹼基還構成一些生命必須物質或是重要的
輔酶 ,如ATP,GTP,CoA等,對生命活動的作用非常大。
互補原則 (the principle of complementary base-pairing)在DNA分子結構中,由於鹼基之間的
氫鍵 具有固定的數目和DNA兩條鏈之間的距離保持不變,使得鹼基配對必須遵循一定的規律,這就是Adenine(A,腺嘌呤)一定與Thymine(T,胸腺嘧啶)配對,Guanine(G,鳥嘌呤)一定與Cytosine(C,胞嘧啶)配對,反之亦然。鹼基間的這種一一對應的關係叫做鹼基互補配對原則。
鹼基 腺嘌呤與胸腺嘧啶之間有兩個氫鍵,鳥嘌呤與胞嘧啶之間有三個氫鍵,即A=T,G≡C。根據鹼基互補配對的原則,一條鏈上的A一定等於互補鏈上的T;一條鏈上的G一定等於
互補鏈 上的C,反之如此。
在DNA轉錄成RNA時,有兩種方法根據鹼基互補配對原則判斷:1)將模板鏈根據原則得出一條鏈,再將得出的鏈中的T改為U(尿嘧啶)即可;2)將非模板鏈的T改為U即可。如:DNA:ATCGAATCG(將此為非模板鏈)TAGCTTAGC(將此為模板鏈)轉錄出的mRNA:AUCGAAUCG(可看出只是將非模板鏈的T改為U,所以模板鏈又叫無義鏈。這也是中心法則和鹼基互補配對原則的體現。)
計算規律 規律一:在一個雙鏈DNA分子中,A=T、G=C。即:A+G=T+C或A+C=T+G。也就是說,嘌呤鹼基總數等於嘧啶鹼基總數,各占全部鹼基總數的50%。
5種鹼基 規律二:在雙鏈DNA分子中,兩個互補配對的鹼基之和的比值與該DNA分子中每一單鏈中這一比值相等。(A1+A2+T1+T2)/(G1+G2+C1+C2)=(A1+T1)/(G1+C1)=(A2+T2)/(G2+C2)。
規律三:DNA分子一條鏈中,兩個不互補配對的鹼基之和的比值等於另一互補鏈中這一比值的倒數,即DNA分子一條鏈中的比值等於其互補鏈中這一比值的倒數。(A1+G1)/(T1+C1)=(T2+C2)/(A2+G2)。
規律四:在雙鏈DNA分子中,互補的兩個鹼基和占全部鹼基的比值等於其中任何一條單鏈占該鹼基比例的比值,且等於其轉錄形成的mRNA中該種比例的比值。即雙鏈(A+T)%或(G+C)%=任意單鏈(A+T)%或(G+C)%=mRNA中(A+U)%或(G+C)%。
規律五:不同生物的DNA分子中,其互補配對的鹼基之和的比值(A+T)/(G+C)不同,代表了每種生物DNA分子的特異性。
相關信息 鹼基互補配對規律的計算的生物學知識基礎是基因控制蛋白質的合成。由於基因控制蛋白質的合成過程是:
鹼基配對 (1)微觀領域———分子水平的複雜生理過程,學生沒有感性知識為基礎,學習感到非常抽象。
(2)涉及到多種鹼基互補配對關係,DNA分子內部有A與T配對,C與G配對;DNA分子的模板鏈與生成的RNA之間有A與U配對,T與A配對,C與G配對。學習過程中,學生不易認識清楚。
(3)涉及許多數量關係(規律),在DNA雙鏈中,①A等於T,G等於C,A+G/T+C等於A+G/T+C等1;②一條單鏈的A+G/T+C的值與另一條互補單鏈的A+G/T+C的值互為倒數。③一條單鏈的A+T/C+G的值,與另一條互補鏈的A+T/C+G的值相等;④在雙鏈DNA及其轉錄的RNA之間有下列關係:一條鏈上的(A+T)等於另一條鏈上的(A+T)等於RNA分子中(A+U)等於12DNA雙鏈中的(A+T)等,學生往往記不住。再加之轉錄、翻譯是在不同場所進行的,學生分析問題時難以把二者聯繫起來。以上分析說明,關於鹼基互補配對規律的計算既是教的一個難點,也是學的一個難點。教學中,如果能做到:①把複雜抽象的生理過程用簡單直觀的圖示表現出來;②把在不同場所進行的生理過程放在一起思考;③把記憶複雜繁瑣的公式(規律)轉變成觀察圖示找出數量關係;④在計算時把表示數的符號註上腳標,以免混淆,就能輕輕鬆鬆闖過這一難關。
醫學套用 DNA鹼基序列決定其光敏性假設獲證實。DNA分子在所有生命形態中扮演著遺傳信息載體的角色,對紫外光的修改具有高度的抵抗性,但要理解其光穩定性的機制還存在一些令人費解的問題。一個重要方面是,構成DNA分子的4種鹼基之間的相互作用。德國基爾大學的研究人員成功地證明,DNA鏈因其鹼基序列而有不同的光敏感性。相關研究結果發刊登在《科學》雜誌上。科學家們早就了解到,對包含在DNA中的遺傳信息進行編碼的個別鹼基具有高度光穩定性,當它們吸收了來自紫外光輻射的能量時,這些能量會立刻再次釋放。但令人驚訝的是,科學家們發現在包含有眾多鹼基的DNA中,這些機制變得失效或只是部分有效。因此,科學家們推斷,紫外光激發的DNA分子的失活,必定由某種完全不同的、DNA特有的機制所取代。通過以各種方法測量具有不同鹼基序列的DNA分子,德國的基爾大學理化研究所弗里德里希·泰姆普斯教授所領導的研究小組終於證實並闡明了該種假設。
鹼基 泰姆普斯教授表示,DNA通過其複雜的
雙螺旋結構 達成其高度的光穩定性。在單股DNA鏈中,鹼基之間的相互作用是一個堆疊在另一個之上,而且在雙螺旋中,兩個互補單股的鹼基對之間的氫鍵發揮了關鍵作用。通過觀察到的不同互動作用,DNA在某種程度上自己達成了“太陽防護”。論文作者尼娜·施瓦爾博在合成DNA分子中的過程中研究了各種不同的鹼基組合。利用飛秒脈衝雷射光譜學,她測量了每種組合所釋放出來的特徵能量。她發現,對某些鹼基組合而言,這些螢光發射的“壽命”只有約100飛秒,但對其他組合而言,時間可長達數千倍。
對於該研究結果,尼娜評論道:“我們研究了光物理特性,發現不同的鹼基組合具有廣泛的螢光發射壽命差異,這將導致開發出一種利用雷射直接識別某些遺傳序列的新診斷方法,而無須像現有方法那樣以染料標記DNA。”
泰姆普斯解釋說,在納米電子學領域中,合成DNA已被證明能當作“納米線”使用。基於這些分子不同的反應時間,有朝一日或許能使用雷射脈衝來“開關”特定分子。在某些情況下,甚至有可能用DNA製造出通過氫鍵的鍵合來工作的電晶體。
發展前景 涉及到
RNA 的試驗,經常會要求對RNA分子進行固定化處理,這個過程通常由生物素進行標記,並輔以抗生物素蛋白作為支持物。人們可以將
UMP 、CMP之類的生物素化核苷酸單磷酸鹽整合到RNA之中去,或者通過在轉錄反應中使用核苷酸單磷酸鹽5'端衍生物類生物素,從而達到僅僅對RNA的5'端進行標註的目的。當然,人們也可以對純化的RNA進行5'端或3'端的化學修飾。目前最簡單的方法,就是在轉錄過程中對標記過程進行整合;但對於一些試驗來說,對RNA進行特定位點的標記,比起對5'端進行標記或者為避免改變RNA的功能而僅僅使用單個標記物來說,似乎更為重要。
為達到上述目標,IchiroHirao及其在東京大學和RIKEN的合作夥伴對非天然鹼基對進行了修飾,這些生物素化的鹼基能被T7RNA聚合酶以特定位點的方式整合到RNA之中去。例如,2-氨基-6-(2-噻吩基)嘌呤(s)可以被整合到一個DNA模板之中去;接著,在一個標準化的轉錄反應中,已經被生物素化的2-氧-(1H)吡啶(y)在s補足位點被整合到了RNA轉錄過程中。這一方法很容易被一般性的試驗室掌握,也可以通過引入T7RNA聚合酶的方式作為商業性的轉錄工具包加以套用。Hirao說:“除了那些包括像s和y或修飾性y底物這類非天然鹼基的DNA模板外,這一工具包可在原始協定不加修改的情況下進行套用。”
在一篇新近出版的有關“核酸研究”的論文中,研究小組套用上述方法,在感測器上對一個反義的Raf-1RNA寡聚核苷酸適配子成功進行了生物素化和固定化的處理;這一寡聚核苷酸適配子準確地找到了它的目標靶點。
Hirao認為,這一由非天然鹼基對組成的系統對於RNA技術將非常有用。如果這些非天然鹼基對能和原核RNA聚合酶、真核RNA聚合酶一起發揮作用的話,這一系統的套用範圍將大大擴展,甚至可以套用到體內試驗。Hirao也計畫將這一系統的套用擴展到複製、轉錄和翻譯這些功能過程中。他說:“如果那些包含非天然鹼基對的DNA片段能通過PCR手段進行擴增的話,這一系統作為工具進行使用的前景將更為廣闊!”
 鹼基置換類型及缺失和插入突變示意圖
鹼基置換類型及缺失和插入突變示意圖 鹼基
鹼基 鹼基
鹼基 5種鹼基
5種鹼基 鹼基配對
鹼基配對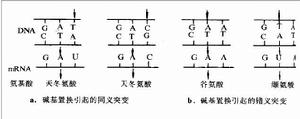 鹼基
鹼基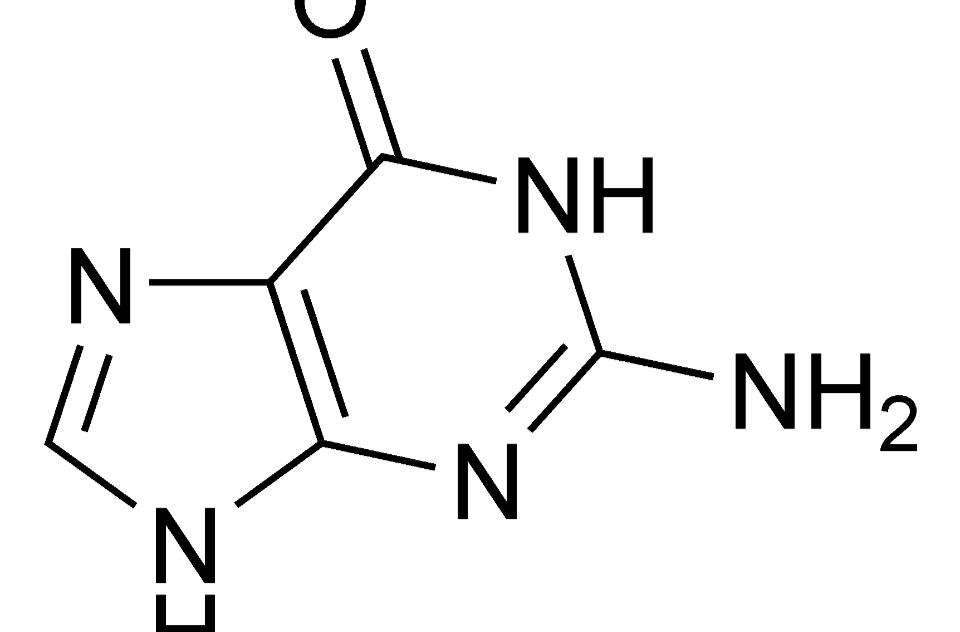
 鹼基置換類型及缺失和插入突變示意圖
鹼基置換類型及缺失和插入突變示意圖 鹼基
鹼基 鹼基
鹼基 5種鹼基
5種鹼基 鹼基配對
鹼基配對 鹼基
鹼基