基本介紹
- 中文名:軌道重疊
- 外文名:Orbital overlap
- 類型:正重疊、負重疊、零重疊
- 利用:原子軌道線性組合形成分子軌道
形成條件

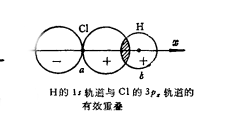
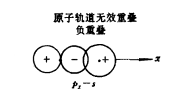
分類

解釋共價鍵形成







軌道重疊其實是分子中的原子的原子軌道線性組合,原子軌道相加形成成鍵軌道,原子軌道相減形成反鍵軌道,電子填充在了成鍵軌道上體系能量下降。原子軌道重疊後,就形成分子軌道,原來的電子就在分子軌道上運動。 分子軌道理論認為,在分...
軌道重疊布居數是2016年公布的化學名詞。 定義 馬利肯布居數分析中A原子的μ軌道與B原子的軌道之間的重疊布居數稱為軌道重疊布居數,其定義為。這裡對占有的分子軌道i求和,是這兩個原子軌道的重疊積分,為B原子的軌道參與第i號分子...
而是屬於整個分子的分子軌道,分子軌道是多中心的;分子軌道由原子軌道組合而成,形成分子軌道時遵從能量近似原則、對稱性一致(匹配)原則、最大重疊原則,即通常說的“成鍵三原則”;在分子中電子填充分子軌道的原則也服從能量最低原理、...
這兩個π鍵不同於σ鍵,軌道重疊也較少並不穩定,因而容易斷開,所以含三鍵的炔烴也容易發生加成反應。雜化軌道限於最外層電子,而在第一層的兩個電子不參與反應,而在其他層上有許多的軌道,電子會從能量低的層“躍遷”到能量高的...
[軌道]重疊積分 [軌道]重疊積分([orbital] overlap integral)是2019年公布的物理學名詞,出自《物理學名詞》 (第三版)。公布時間 2019年經全國科學技術名詞審定委員會審定發布。出處 《物理學名詞》 (第三版)
分子軌道理論認為化學鍵是原子軌道重疊產生的。有幾個原子軌道就能線性組合成幾個分子軌道。那么,當兩個原子軌道重疊時,可以形成兩個分子軌道Ψ=Ψ±Ψ。Ψ和Ψ分別代表兩個原子軌道。其中一個分子軌道是由兩個原子軌道的波函式相加而...
重疊(英語:Stacking,又譯堆積)在超分子化學中是指芳香性分子的一類排列堆積形式。例如DNA中連續性鹼基的堆積系統,或是某些具有兩個非極性環的酵素,會以π軌道重疊的方式而堆積在一起。超分子 超分子(supermolecule)是在1937年由...
兩個原子軌道形成的分子軌道,能級低於原子軌道的稱為成鍵軌道;能級高於原子軌道的稱為反鍵軌道;能級接近原子軌道的一般為非鍵軌道。兩個原子軌道要有效的組合成分子軌道,必須滿足對稱性匹配、能級相近和軌道最大重疊三個條件。其中對稱...
分子軌道理論(簡稱MO法)是一種套用較為普遍共價鍵理論,它將分子看作一個整體,由分子中各原子間的原子軌道重疊組成若干分子軌道,幾個原子軌道組合後可得幾個分子軌道,然後將電子逐個填入分子軌道,如同原子中將電子安排在原子軌道一樣...
星下點軌跡周期性出現重疊現象的人造地球衛星軌道。重疊出現的周期稱為回歸周期。工程中回歸周期的大小根據衛星的使命確定。同一個回歸周期對應有很多條軌道。如回歸周期為一天時,運行的軌道周期可近似為24小時、8小時……,從中可以選出...
靜止衛星導航重疊是指為了提高全球導航衛星系統(指GPS或GLONASS)的可用性、連續服務性,增加用戶視見衛星的數目,採取在地球靜止軌道上的某些原供通信服務的衛星,即第三代INMARSAT衛星上載入導航轉發器,發射類GPS導航信號,使其發揮導航功能...
沿鍵軸(兩原子核的連線)方向以“頭碰頭”的方式發生原子軌道(電子云)重疊,軌道重疊部分呈現圓柱形對稱沿著鍵軸而分布,具有軸對稱特徵的共價鍵稱為σ鍵。釋義 由兩個相同或不相同的原子軌道沿軌道對稱軸方向相互重疊而形成的共價鍵...
π鍵指原子軌道垂直於鍵軸以“肩並肩”方式重疊所形成的化學鍵。形成π鍵時,原子軌道的重疊部分對等地分布在包括鍵軸在內的平面上、下兩側,形狀相同,符號相反,呈鏡面反對稱。名字中的希臘字母π代表了p軌道,因為π鍵的軌道對稱性與...
同共軛效應又稱 p 軌道與 p 軌道的 型重疊。甲基以上的烷基,除有超共軛效應外,還可能產生同共軛效應。 所有同共軛效應,原是指 碳原子上的 C—H 鍵與鄰近的 鍵間的相互作用。大量的化學活性和電子光譜的數據表明,在丙烯基離子...
在δ軌道運動的電子就是δ電子,由δ電子形成的共價鍵就是δ鍵。用途 兩個原子軌道重疊時,重疊程度越大,形成的共價鍵越穩定,δ鍵是原子軌道沿軸向重疊的,所以具有較大重疊程度,比較穩定、鍵能較大,δ鍵不容易極化,可以單獨存在...
在化學反應中元素的原子都有使最外層電子達到穩定結構的趨勢。在共價鍵理論中,成鍵的兩個原子的軌道發生重疊,一對電子位於兩個原子之間。例如氯元素的原子在化學反應中易得到一個電子,而氫元素的原子容易失去一個電子形成穩定結構、這...
又稱d軌道接受共軛。是指一個原子的p軌道與另一個原子的d軌道重疊而產生的一種共軛現象,例如有機矽化合物結構中的d-p共軛;在這裡,苯環上的一部分π電子云進入矽的3d軌道,形成d-p共軛,使矽原子與苯環結合得更牢。此外,共軛...
其本質是原子軌道重疊後,高機率地出現在兩個原子核之間的電子與兩個原子核之間的電性作用。歷史 早期歷史 在古希臘,化學還沒有從自然哲學中分離的時代,原子論者對化學鍵有了最原始的構想,恩培多克勒(Empedocles)認為,世界由“氣、...
價鍵理論valence-bond theory,一種獲得分子薛丁格方程近似解的處理方法。又稱電子配對法。歷史上最早發展起來的化學鍵理論。其核心思想是原子間相互接近軌道重疊,原子間共用自旋相反的電子對使能量降低而成鍵。產生 1927年W.H.海特勒和F...
時 ,在H的影響下,C的1個2s軌道和3個 2p軌道進行sp³雜化,形成4個sp³雜化軌道,每個sp³雜化軌道中各有一個未成對電子。C用4個sp³雜化軌道分 別與4個H的1s軌道重疊形成4個σ鍵。由於C的4個sp³雜化軌道間的夾角...
但由於原先s 軌道中已含一對孤對電子,因此雜化後4 個 Sp3雜化軌道所含s、P 的成分不完全相等。成鍵時,N 原子用 3 個各含一個未成對電子的sP3成鍵雜化軌道分別與3 個 H 原子的1s 軌道重疊,形 成 3 個 N- H 鍵 ,而...
這些雜化軌道相互重疊,形成分子σ骨架,故所有原子處於同一平面。每個碳原子還有一個未參與雜化的p軌道,垂直於分子平面,每個p軌道裡面有一個電子,故丁二烯分子中存在一個“4軌道4電子”的p-p大π鍵。通常用πₐ來表示,其中a為...
簡單一點說,是一種特殊的共價鍵(從價鍵理論的觀點看),價鍵理論要求兩個原子之間通過各自提供一個滿足要求的原子軌道的重疊來形成共價鍵。簡介 由於氫原子價軌道為1S軌道,是球形對稱的,當同時有兩個滿足條件的原子軌道從不同的方向...
C用4個Sp3雜化軌道分 別與4個H的1s軌道重疊形成4個σ鍵。由於C的4個sp3雜化軌道間的夾角為109°28',所以生成的CH₄的幾何構型為正四面體。sp3d雜化 由一個ns、三個np軌道和一個nd軌道雜化形成五個能量等同的sp3d雜化軌道。
(3)成鍵電子的原子軌道重疊越多,其核間機率密度就越大,形成的共價鍵越牢固,分子越穩定,由此可知共價鍵的形成在可能範圍內將沿著原子軌道最大重疊的方向,此即子軌道最大重疊原理。共價化合物的特點 以共用電子對形成分子的化合物叫...
又稱 p 軌道與 p 軌道的 型重疊。甲基以上的烷基,除有超共軛效應外,還可能產生同共軛效應。所有同共軛效應,原是指 碳原子上的 C—H 鍵與鄰近的 鍵間的相互作用。大量的化學活性和電子光譜的數據表明,在丙烯基離子和類似的烯...
由於一個p軌道可以和左右相鄰的兩個碳原子的p軌道同時重疊,因此形成的分子軌道是一個包含六個碳原子在內的封閉的或稱為是連續不斷的共軛體系,如圖1所示。π軌道中的π電子能夠高度離域,使π電子云完全平均化,從而能量降低,苯分子...
