基本介紹
相關問題
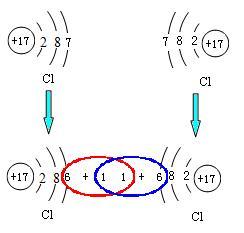 共用電子對
共用電子對 共用電子對
共用電子對在化學反應中元素的原子都有使最外層電子達到穩定結構的趨勢。在共價鍵理論中,成鍵的兩個原子的軌道發生重疊,一對電子位於兩個原子之間。例如氯元素的原子在化學...
共用電子對偏移...... 共用電子對.就是指當物質以共價鍵形成物質時,期間是通過相互共用電子以達到結合的目的.比如H2,2者共享彼此的2個電子形成穩定的物質. 電子對...
原子通過共用電子對而形成的化學鍵叫電子對鍵,又叫共價鍵(covalent bonding)。兩原子間共用一對電子的共價鍵叫共價單鍵(single covalent bonding),共用兩對、三對...
必須正確地表示出共用電子對數,並滿足每個原子的穩定結構。電子式離子 陽離子 簡單陽離子由於在形成過程中已失去最外層電子,所以其電子式書寫方式就是其離子符號...
價層電子對互斥模型是將共用電子對與孤對電子的概念,與原子軌道的概念相結合,且電子斥力達到最小。在這個模型中電子對相互排斥,成鍵電子與孤對電子距離越遠越好。...
配位鍵,又稱配位共價鍵,或簡稱配鍵,是一種特殊的共價鍵。當共價鍵中共用的電子對是由其中一原子獨自供應,另一原子提供空軌道時,就形成配位鍵。配位鍵形成後...
雙鍵是共價鍵的一種,共價鍵,就意味著共用電子對的存在。簡單的說,就是這一對電子,由鍵的兩方各出一個,彼此共用。因此,一個共價鍵就可以填補一個最外層電子的...
在分子中,同種原子形成共價鍵,兩個原子吸引電子的能力相同,共用電子對不偏向任何一個原子,因此成鍵的原子都不顯電性。這樣的共價鍵叫做非極性共價鍵,簡稱非極性...
共價鍵的共用電子對由成鍵的兩個原子各提供一個電子組成的, 稱為正常共價鍵。此外,還有一類共價鍵,其共用電子對完全是由一個成鍵原子單獨提供的。這種由一個...
(1) 按共用電子對的數目分,有單鍵(Cl—Cl)、雙鍵(C=C)、三鍵(N≡N,C≡C)等。(2) 按共用電子對是否偏移分類,有極性鍵(H—Cl)和非極性鍵(Cl—Cl)。...
兩個或多個原子共同使用它們的外層電子,在理想情況下達到電子飽和的狀態,由此組成比較穩定的化學結構,像這樣由幾個相鄰原子通過共用電子並與共用電子之間形成的一種...
共價鍵是電負性相同或相差不大的兩個元素的原子相互作用時,原子之間通過共用電子對所形成的化學鍵。由共價鍵形成的化合物稱為共價化合物。為了闡明這一類型的化學鍵...
原子之間通過共用電子對所形成的相互作用叫共價鍵,可以是吸引力,也可是排斥力。而在化合物分子中,不同種原子形成共價鍵時,因為原子吸引電子的能力不同,共用電子對...
在化合物分子中,不同種原子形成的共價鍵,由於兩個原子吸引電子的能力不同,共用電子必然偏向吸引電子能力較強的原子一方,因而吸引電子能力較弱的原子一方相對的顯正...
和電子親合能,首先由萊納斯·卡爾·鮑林於1932年引入電負性的概念,用來表示兩個不同原子間形成化學鍵時吸引電子能力的相對強弱,是元素的原子在分子中吸引共用電子的...
配位原子指的是配位化合物中直接和中心原子(或離子)配位的配位體的原子。配位原子提供弧對電子被中心離子接受形成配位鍵。例F、I、Br等電負性較大的非金屬...
氧化-還原反應 (oxidation-reduction reaction, 也作redox reaction)是化學反應前後,元素的氧化數有變化的一類反應。氧化還原反應的實質是電子的得失或共用電子對的...
所以,了解和熟悉共價鍵,是研究和掌握有機化合物的結構與性質之間關係的關鍵。共價即電子對共用(或說電子配對)。中文名 共價鍵結合 外文名 covalent bond 類別 ...
如果親電試劑進攻鄰、對位,有比較穩定的極限式(c、e),這是由於氯原子的非共享電子對向苯環轉移,使(c、e)的每個原子均具有穩定的八隅體結構,由穩定極限式參與...
