親電加成反應(EA),簡稱親電加成,是親電試劑(帶正電的基團)進攻不飽和鍵引起的加成反應。反應中,不飽和鍵(雙鍵或三鍵)打開,並與另一個底物形成兩個新的σ鍵。親電加成中最常見的不飽和化合物是烯烴和炔烴。
基本介紹
- 中文名:親電加成
- 外文名:electrophilic addition reaction
- 常見化合物:烯烴和炔烴
- 套用學科:有機化學
基本性質
化學反應
反應機理
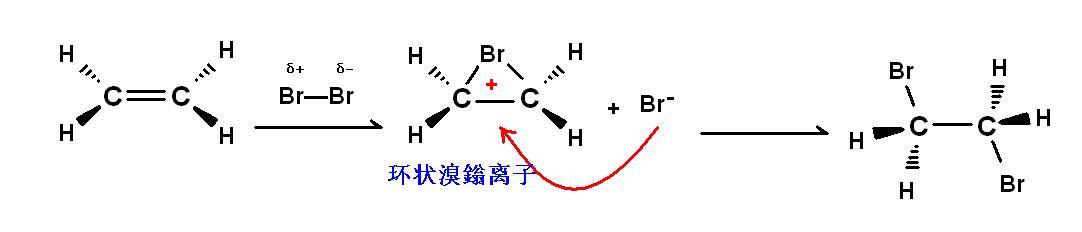 乙烯與溴親電加成(環狀鎓離子歷程)
乙烯與溴親電加成(環狀鎓離子歷程)舉例分析
與鹵素的加成
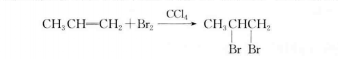
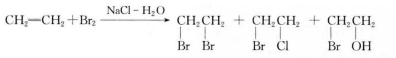
與水的加成
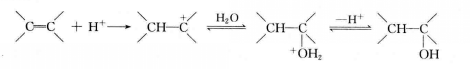
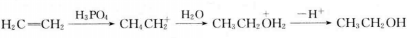

親電加成反應(EA),簡稱親電加成,是親電試劑(帶正電的基團)進攻不飽和鍵引起的加成反應。反應中,不飽和鍵(雙鍵或三鍵)打開,並與另一個底物形成兩個新的σ鍵。親電加成中最常見的不飽和化合物是烯烴和炔烴。
 乙烯與溴親電加成(環狀鎓離子歷程)
乙烯與溴親電加成(環狀鎓離子歷程)
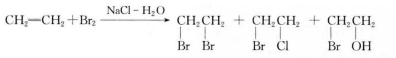

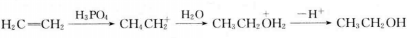
親電加成反應(EA),簡稱親電加成,是親電試劑(帶正電的基團)進攻不飽和鍵引起的加成反應。反應中,不飽和鍵(雙鍵或三鍵)打開,並與另一個底物形成兩個新的σ鍵...
親電加成反應,是不飽和鍵的加成反應,是π電子與試劑作用的結果。...... (氫多加氫)廣義的親電加成反應是由任何親電試劑與底物發生的加成反應。親電加成反應機理 ...
加成反應一般是兩分 子反應生成一分子,相當於無機化學的化合反應。根據機理,加成反應可分為親核加成反應,親電加成反應,自由基加成,和環加成。加成反應還可分為順...
親電反應指缺電子(對電子有親和力)的試劑進攻另一化合物電子云密度較高(富電子)區域引起的反應。親電反應屬於離子型反應(ionic reaction)的一種,是有機化學的...
親電加成反應是烯烴的加成反應。廣義的親電加成親反應是由任何親電試劑與底物發生的加成反應。在烯烴的親電加成反應過程中,氫正離子首先進攻雙鍵(這一步是定速...
不對稱烯烴與鹵化氫等親電試劑發生加成反應的取向與按馬氏規則預測的取向不一致時,稱為反馬氏加成(反馬爾可夫尼可夫規則)。反馬氏規則的情況大致有兩種:(1)過氧化...
鍵相結合。得到一種飽和或比較飽和的加成產物。烯烴與無機酸和強有機酸都能發生親電加成,與弱有機酸的加成要在強[1] 酸催化下才能進行,產物為酚 }如乙烯與...
苯炔的親電加成反應 3、親電加成三烷基硼、鹵素、鹵化汞、鹵化錫、鹵化矽等親電試劑易於苯炔發生親電加成。例如:與碘的親電加成反應 ...
親電反應可分為親電取代反應和親電加成反應等。 另外,還有一類反應,它不同於以上兩類反應,反應過程中舊鍵的斷裂和新鍵的生成同時進行,無活性中間體生成,這類...
其內容即:當發生親電加成反應(如鹵化氫和烯烴的反應)時,親電試劑中的正電基團(如氫)總是加在連氫最多(取代最少)的碳原子上,而負電基團(如鹵素)則會加在...
當有過氧化物(如H2O2,R-O-O-R等)存在,氫溴酸與丙烯或其他不對稱烯烴起加成反應時,反應取向是反馬爾科夫尼科夫規則的。此反應不是親電加成反應而是自由基加成...
(1)親電加成乙炔及其取代物與烯烴相似,也可以發生親電加成反應,但由於sp碳原子的電負性比sp2碳原子的電負性強,使電子與sp碳原子結合得更為緊密,儘管三鍵比雙鍵多...
因此,馬氏規則可以用來預示親電加成反應的方向。馬氏規則可用另一種方法表述:不對稱烯烴與極性試劑加成時,試劑中正離子或帶部分正電荷部分加到重鍵中帶有部分負電荷...
吡環上親電加成反應 氮原子的電負性比碳原子的強,吡啶環上的電子云密度不苯環低,尤其是吡啶環的α位。 吡催化加氫反應 吡啶比苯容易還原 另見pǐ 吡 pǐ ...
羥汞化反應,簡稱羥汞化。它屬於有機反應中的親電加成反應,能把烯烴轉換成飽和的醇類,炔烴轉換成乙烯醇,再經過互變異構化生成相應的醛、酮化合物。例如烯烴和...
藍色數據是連線普通共振基團(乙烯基、苯基和環丙基)的烯烴,它們的PA值都比乙烯的大得多,表明共振基團的引入將提高親電加成反應的活性。黃色數據是針對連線吸電子...
在這兩大類型反應中.又根據反應進行的方式分為取代反應、加成反應、消除反應等,分別稱為親核取代、親核加成、親電取代、親電加成、親核消除和親電消除等。...
addition reaction[化學]加成反應 ; 加聚反應 ; 加成反響 ; 加成反映electrophilic addition親電加成反應 ;[有化]親電加成 ; 親電子加成addition agent添加劑 ; ...
又例如,在高交聯St−DVB共聚物的氯甲基化反應中,氯甲醚可加成到懸掛雙鍵上,生成−CH(OCH3)CH2CH2Cl基團。脂肪族取代氯進行親電加成反應的活性遠不如苄氯...
不飽和烴的雙鍵和三鍵不太牢固,比較容易斷裂,易發生親電取代反應和親電加成反應。中文名 不飽和烴 外文名 unsaturated hydrocarbon ...
一、 親電加成反應二、 自由基加成反應三、 催化氫化(或稱催化加氫)反應和氫化熱四、 氧化反應五、 聚合反應六、 α氫的自由基鹵化反應...
不對稱烯烴與鹵化氫等親電試劑發生加成反應的取向與按馬氏規則預測的取向不一致時,稱為反馬爾可夫尼可夫規則。反馬氏規則的情況大致有兩種:1、在光及過氧化物作用下...
普林斯反應原名Prins反應(Prins reaction),醛或酮與烯烴或炔烴在酸催化下的縮合反應。其中關鍵性的中間體是質子化的羰基化合物對烯烴的親電加成所生成的碳正離子...
雙烯親電加成反應 1,2-加成和1,4-加成:極性試劑有利於1,4-加成;低溫有利於1,2-加成,高溫有利於1,4-加成。共軛二烯烴同普通烯烴一樣,容易與鹵素、鹵化氫...
第二節親電加成反應109 一、親電加成反應歷程109 二、親電加成反應的立體化學111 三、取代基的性質對烯烴加成反應的影響113 四、親電加成反應的實例114 第三節...
乙炔及其取代物與烯烴相似,也可以發生親電加成反應,但由於sp碳原子的電負性比sp2碳原子的電負性強,使電子與sp碳原子結合得更為緊密,儘管三鍵比雙鍵多一對電子,也...
