硫化物的定義
-2價硫的化合物,
金屬硫化物可以看成氫硫酸的鹽。金屬與硫直接反應或者將
硫化氫氣體通入金屬
鹽溶液,或者往鹽溶液中加入
硫化鈉,都可製得金屬硫化物。
鹼金屬硫化物和硫化銨易溶於水,由於
水解其溶液顯鹼性。
鹼土金屬、鈧、釔和鑭系元素的硫化物較為難溶。當陽離子的外層
電子構型為18電子和18+2電子時,往往由於較強的
極化作用而形成難溶的、有顏色的硫化物。大多數不溶於水的硫化物可溶於酸並釋放出硫化氫,極難溶的少數金屬硫化物(如CuS、HgS)可用
氧化性酸將其溶解,此時S被氧化成硫而從溶液中析出。難溶金屬硫化物在溶液中存在溶解-沉澱平衡。控制溶液的酸度,可以改變溶液中S
2- 離子的濃度,從而將溶解度各不相同的難溶
金屬硫化物分別沉澱出來。這是定性分析中用
硫化氫分離、鑑定金屬離子的基礎。
硫化物合成
無機硫化物通常可通過以下方法合成:(註:K為國際溫度單位開爾文)
Na2SO4 + 4C→ Na2S + 4CO 1373K
FeCl2 + H2S → FeS↓ + 2HCl
3SiO2 + 2Al2S3→ 3SiS2 + 2Al2O3 1373K
(NH4)2MoO4+ 4(NH4)2S + 4H2O → (NH4)2[MoS4] + 8NH3·H2O
(NH4)2MoO4+ 2HCl --(加熱)→ MoS3 + H2S + 2NH4Cl
5、高價硫化物加熱分解,例如:
MoS3 --(加熱)→ MoS2 + S
物理性質
顏色
| 幾種硫化物的顏色 |
|---|
| 黃 | GeS | 灰黑 | P4S5 | 亮黃 | | 黃 |
Ga2S3 | 黃 | SnS2 | 黃 | P4S10 | 黃 | | 紅/黑 |
In2S3 | 黃/紅 | | 棕黑 | As4S4 | 紅 | | 綠/肉 |
| 酒紅 | PbS | 黑 | As4S6 | 黃 | MoS3 | 紅棕 |
Tl2S3 | 藍黑 | | As4S10 | 淡黃 | RuS2 | 灰藍 |
Tl2S | 黑 | | | 橙紅 | | 黃 |
| Bi2S3 | 棕黑 | | |
溶解性
金屬的酸式硫化物都可溶於水,但正鹽中只有
鹼金屬硫化物和
硫化銨可溶。一般地講,
金屬硫化物的溶解度可通過
陽離子極化力(離子電荷數/離子半徑,Z/r)的大小來預測。陽離子極化能力的增強,將導致化合物共價性的增加,
極性減小,因而
溶解度也降低。
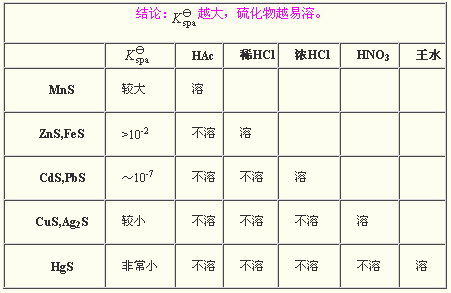 金屬硫化物在酸中溶解性
金屬硫化物在酸中溶解性化學性質
水解
S2-+ H2O ⇌ HS-+ OH-
HS-+ H2O ⇌ H2S + OH-
H2S的p
Ka分別約為:p
Ka1 = 6.89 和 p
Ka2 = 15±2, 因此金屬硫化物溶液會呈不同程度的鹼性,而鹼金屬的硫化物溶液的鹼性更是可以與相應的
氫氧化物匹敵。
灼燒
硫化物轉化為相應的氧化物,硫則轉化為二氧化硫。例如由
方鉛礦製取鉛時有一步為: 2PbS + 3O
2 → 2PbO + 2SO
2硫化物被氧化為相應的可溶
硫酸鹽。
以上兩步都是冶鍊金屬時,轉化硫化物礦石的重要方法。
氧化
S2-- 2e-= S; -0.407V
硫化物酸鹼性
硫化物和相應的氧化物類似,其酸鹼性隨周期和族的變化也和氧化物的類似,但硫化物的鹼性不如氧化物強。
H2S | NaHS | Na2S | As2S3 | As2S5 | Na2S2 |
H2O | NaOH | Na2O | As2O3 | As2O5 | Na2O2 |
\ | 鹼性 | 鹼性 | 兩性 | 酸性 | 鹼性 |
同周期元素最高
氧化態硫化物從左到右酸性增強;同族元素相同氧化態的硫化物從上到下酸性減弱;同種元素的硫化物中,高氧化態的硫化物酸性更強。因此As
2S
5酸性強於Sb
2S
5,而Sb
2S
5的酸性則要強於SnS
2和Sb
2S
3。
重要的硫化物
硫化氫是一種無色有毒的氣體,臭雞蛋氣味,空氣中硫化氫的容許含量不超過0.01mg/L。硫化氫能夠與人體的血紅素中的亞鐵離子結合生成硫化亞鐵,使其失去反應活性。經常與硫化氫接觸會引起嗅覺遲鈍,消瘦,頭痛等慢性中毒。實驗室里常用金屬硫化物與酸作用製備硫化氫。硫化氫的水溶液是氫硫酸,二元弱酸。無論在酸性介質還是鹼性介質中,硫化氫的還原性都很強。
多硫化物
多硫化物是含有多硫離子Sn的化合物,n=2,3,4,5,6,...,9。多硫化物可由硫在硫化物溶液中煮沸製得,其溶液一般都為黃色,且顏色隨n值的增加而加深。
多硫離子存在過硫鍵,類似於
過氧化物,具有
氧化性,但不及過氧離子氧化性強,反應發生歧化:
多硫化物在酸性溶液里很不穩定,酸化時即放出
硫化氫和硫:
多硫離子還可作
配體。例如Na
2Sn作用於(
η-C
5H
5)2TiCl
2時,會生成含有TiS
5環的
配位化合物。
硫化物的鑑定
點滴法點滴法是鑑定硫離子和硫氫根離子的靈敏方法,其步驟為:在點滴板上混合可溶硫化物的鹼性溶液和1%的硝普酸鈉Na
2[Fe(CN)
5NO](
亞硝基鐵氰化鈉)溶液,若試樣中存在S離子則會出現不同深度的紅紫色,靈敏度1:50000。其機理是[Fe(CN)
5(NOS)]4-離子的生成。 除此之外,向點滴板中加入試液、濃鹽酸、幾顆對氨基二甲基苯胺晶體和0.1mol/L
氯化鐵溶液,若在2~3分鐘後出現藍色,也可證明硫離子的存在。機理是生成了藍色的
亞甲基藍。
硫化物來源
硫化物(sulfides)及其類似化合物包括一系列金屬、
半金屬元素與S、Se、Te、As、Sb、Bi結合而成的礦物。礦物種數有350種左右,硫化物就占了2/3以上,其他為硒化物(selenides)、
碲化物(tellurides)、
砷化物(arsenides),及個別
銻化物(antimonides)和鉍化物(bismuthides)。
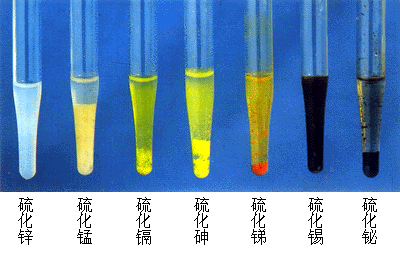 一些金屬硫化物
一些金屬硫化物本大類礦物只占地殼總質量的0.15﹪,其中絕大部分為鐵的硫化物,其他元素的硫化物及其類似類似化合物只相當於地殼總質量的0.001﹪。儘管其分布量有限,但卻可以富集成具有工業意義的礦床,主要有有色金屬,如Cu、Pb、Zn、Hg、Sb、Bi、Mo、Ni、Co等均以本大類礦物為主要來源,故本大類礦物在國民經濟中具有重大意義。
依據
成分中硫離子價態的不同和絡
陰離子的存在與否,硫化物礦物相應分為三類: 單硫化物:硫以S2-形式與
陽離子結合而成,絕大多數為黑色; 過硫化物,硫以啞鈴狀對陰離子[S2]2-形式與陽離子結合而成;
硫鹽礦物,硫與半金屬元素
砷、銻或鉍組成錐狀絡陰離子[AsS
3]
3- 、[BiS
3]
3- ,以及由這些錐狀絡陰離子相互聯接組成複雜形式的絡陰離子與陽離子結合而成。
硫化物的套用
硫化氫系統是傳統且較廣泛的分析
陽離子的方法,主要依據各離子硫化物溶解度的顯著差異,將常見的陽離子分成五組。
組試劑 | HCl | 0.3 mol/L HCl, H2S
或 0.2~0.6 mol/L HCl
TAA,加熱 | NH3 + NH4Cl
(NH4)2S 或
TAA,加熱 | / |
組的名稱 | I組
銀組
鹽酸組 | II組
銅 錫組
硫化氫組 | III組
鐵組
硫化銨組 | IV組
鈣鈉組
可溶組 |
組內離子 | Ag
Hg2
Pb | II A
Pb
Bi
Cu
Cd | II B
Hg
As(III,V)
Sb(III,V)
Sn(II,IV) | Al Mn
Cr Zn
Fe Co
Fe Ni | Ba K
Ca Na
Mg NH4 |
由於H
2S氣體毒性大,且儲存不便,故一般多以
硫代乙醯胺(CH
3CSNH
2,TAA)水溶液作沉澱劑。
在酸性溶液中TAA水解產生H
2S,可替代H
2S: CH
3CSNH
2 + H + 2H
2O ⇌ CH
3COOH + NH
4 + H
2S↑ 在
氨性溶液中水解生成HS,可替代(NH
4)
2S: CH
3CSNH
2 + 2NH
3 ⇌ CH3-C(-NH
2)=NH + NH
4 + HS在鹼性溶液中水解生成S,可替代Na
2S: CH
3CSNH
2 + 3OH ⇌ CH
3COO + NH
3 + H
2O + S 硫化物的其他套用還有:


 金屬硫化物在酸中溶解性
金屬硫化物在酸中溶解性


 一些金屬硫化物
一些金屬硫化物
