基本介紹
- 中文名:平衡態
- 外文名:equilibrium state
- 特徵:無外界影響系統巨觀性質不變
- 學科:熱力學
- 狹義:穩定的平衡態
動態平衡
熱動平衡條件
統計解釋
實例和解釋
以x1,x2,...,xn表示系統的狀態。系統的連續時間動態方程如下:
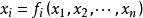
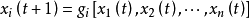
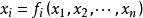
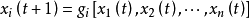
平衡態(equilibrium state)是指在沒有外界影響條件下熱力學系統 的各部分巨觀性質在長時間裡不發生變化的狀態。這裡所說的沒有外界影響,是指系統與外界沒有相互...
處於平衡狀態的物體,由於外界某種微小的作用而偏離了平衡狀態時,因穩度的不同,物體的平衡狀態可分為四種情形:穩定平衡;不穩定平衡;亞穩平衡;隨遇平衡。這些平衡...
熱力平衡狀態是指熱力系統在不受外界影響的條件下,系統的狀態能夠始終保持不變的狀態。熱力系統的各部分之間沒有熱量傳遞,系統就處於熱的平衡;各部分之間沒有相對...
平衡態與非平衡態是對於某個物理量,在系統內部的各處相等、均勻分布,則稱系統在巨觀上呈現出的完全均勻狀態為系統的平衡態。反之,則稱之為非平衡態。這些物理量...
在一定條件下,當一個可逆反應的正反應速率與逆反應速率相等時,反應物的濃度與生成物的濃度不再改變,達到一種表面靜止的狀態,即"化學平衡狀態". 其中,正反應速率...
熱平衡態(thermalequilibrium,stateof),是在沒有外界影響的條件下,熱力學系統的巨觀性質不隨時間變化的狀態。...
化學平衡是指在巨觀條件一定的可逆反應中,化學反應正逆反應速率相等,反應物和生成物各組分濃度不再改變的狀態。可用ΔrGm=ΣνΑμΑ=0判斷,μA是反應中A物質...
stable equilibrium 熱力學系統的平衡態的穩定程度。 在0℃以上,水和水蒸氣的平衡比冰和水蒸氣的平衡更穩定。0℃以下,冰和水蒸氣的平衡比水和水蒸氣平衡更穩定,...
在力學系統里,平衡是指慣性參照系內,物體受到幾個力的作用,仍保持靜止狀態,或勻速直線運動狀態,或繞軸勻速轉動的狀態,叫做物體處於平衡狀態,簡稱物體的“平衡”。...
在一定的溫度下,電子從低能量的量子態躍遷到高能量的量子狀態及電子從高能量的量子態躍遷到低能量的量子態這兩個相反過程之間建立起動態平衡,稱為熱平衡狀態。...
《一般平衡態的理論與證明(英文)》旨在講述研究自由市場經濟的性質和運轉的平衡態理論。這個領域是解決walras提出的有關市場運作的問題和frankhahn提出的問題,frank...
《平衡態統計物理學》是2010年世界圖書出版公司出版的圖書,作者是普利史可。...... 《平衡態統計物理學》是2010年世界圖書出版公司出版的圖書,作者是普利史可。...
從哲學的維度來講,平衡是自然的狀態保持,世界萬物原本就是這樣和諧地交融在一起。這種狀態間或並必然會被打破,但終究會達成更高層次的恢復。以此往復,人們看到了...
平衡系統equilibrium system,熱力學術語,指處於平衡態的系統。不處於平衡態的系統叫非平衡系統。...
平衡態熱力學方法又稱經典熱力學方法。是從能量觀點出發,研究巨觀平衡系統的性質,並建立平衡的一般規律的方法。它研究平衡系統的有序穩定結構,以及從一個平衡狀態...
《平衡態和非平衡態統計熱力學 》是2007年北京世圖出版社出版的圖書,作者是Michel Le Bellac。...
即研究對象將要失去而尚未失去平衡的狀態,一般套用於土質邊坡或土石壩的穩定性分析研究中,通過研究極限平衡狀態下岩質滑坡滑動面,可以較準確的確定相關參數,為滑坡...
幾個力作用在同一個物體上,如果這個物體仍然或變成處於 靜止狀態或勻速直線運動狀態,或者是合力為零則這幾個力的作用合力為零,我們就說這幾個力平衡。...
平衡理論這個理論認為人們用一種平衡的方式自發地組織他們的好惡。當兩個人互相喜歡對方而且發現他們在很多方面具有相似性時,這就表現為平衡( balance),而且平衡是...
