
鿔(第112號化學元素)
本詞條是多義詞,共2個義項
更多義項 ▼
收起列表 ▲
鿔是第112號化學元素,於1996年被合成出來,被正式命名為“Copernicium”,符號為Cn,中文譯名為“鿔”。此名稱是為了紀念著名天文學家哥白尼(Copernicus)而得名的。
鿔元素最早由德國達姆施塔特重離子研究所(GSI)西格·霍夫曼(Sigurd Hofmann)和維克托·尼諾夫(Victor Ninov)領導的研究團隊在1996年合成出來。他們在重離子加速器中用高速運行的鋅原子束轟擊鉛靶獲得一顆(另一顆被擊散)半衰期僅為0.24毫秒的Cn原子。
基本介紹
- 中文名:鿔(部分設備無法顯示簡體,繁體為“鎶”)
- 外文名:Copernicium
- 別名:112號元素
- CAS登錄號:54084-26-3
- 密度:23.7 g/cm
- 原子量:285
- 原子半徑:110pm(預測)
- 族:過渡金屬,第7周期,IIB族
- 共價半徑:122pm(預測)
- 半衰期:0.24ms
簡述,理化特性,發展歷史,發現,名稱,核合成,冷聚變,熱聚變,衰變產物,推算的化學屬性,
簡述
於2010年
2月19日被命名。第112號
化學元素,英文copernicium,縮寫Cn(為紀念
哥白尼),中文命名為“鿔”(繁體為“鎶”),讀音為“
gē”。
 鎶的簡化漢字
鎶的簡化漢字 理化特性
已知/預測的性質
名稱,符號,序數:Cn、112、Copernicium
系列:過渡金屬
族,周期,元素分區:12族,7,d
顏色和外表:未知;可能是金屬態;
銀白色或灰色
核內質子數:112
核內中子數:173
核外電子數:112
核內質子質量:1.87376E-25g
核內質子相對質量:112.784
所屬周期:7
所屬族數:IIB
物質狀態:常溫下可能是液態或氣態
價電子排布:可能為[Rn]5f、6d、7s
電子在每能層的排布:2、8、18、32、32、18、2
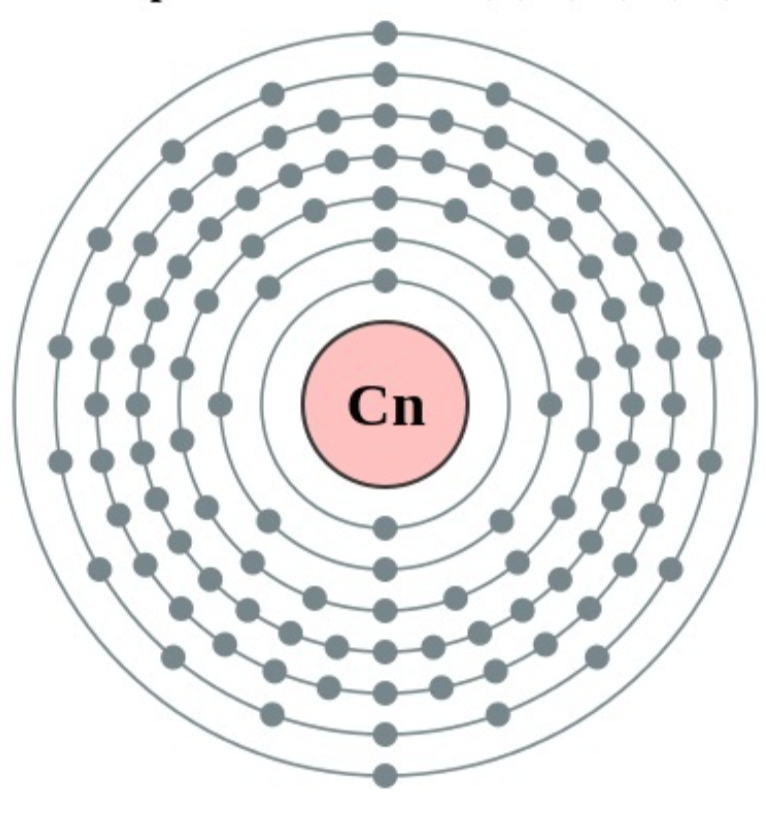 鎶的電子層
鎶的電子層 為紀念著名天文學家哥白尼(Nicolaus Copernicus),德國重離子研究中心於2009年7月向國際純粹與套用化學聯合會提出了上述命名建議,但該中心建議新元素的元素符號為“Cp”。由於“Cp”已有其他科學含義,為避免歧義,國際純粹與套用化學聯合會經與發現第112號化學元素的研究小組協商,最終將新元素的元素符號定為“Cn”。該聯合會選擇2月19日為新元素正式冠名是因為這一天是哥白尼(1473年-1543年)的生日。
德國重離子研究中心於1996年在粒子加速器中用鋅離子轟擊鉛靶首次成功合成了第112號化學元素的一個原子,2002年重複相同的實驗又製造出一個第112號化學元素的原子。此後,日本的一個研究機構於2004年也合成了這種元素的兩個原子,從而證實德國科學家的發現。
名稱
國際純化學與套用化學聯盟(IUPAC)在經過長期驗證後,於2009年6月正式承認第112號元素的合成,並隨後邀請Hofmann團隊為112號元素提出一個永久名稱。2009年7月17日,該團隊提議將112號元素命名為
Copernicium,縮寫Cp,以紀念著名天文學家
哥白尼(Copernicus)。他們稱,將其命名為Cp的原因,是由哥白尼所提出的
日心說與化學中的
原子結構(
盧瑟福模型)有很多相似之處。
Cp這個名稱未獲得IUPAC的正式承認。IUPAC在此後6個月的時間內進行審議,聽取科學界的意見,並於2010年1月公布審議的結果。2009年9月,有人在
自然雜誌上發表文章指出符號Cp曾是元素鑥(
Lutetium)的舊稱(
Cassio
peium),在配位化學中亦用於指
環戊二烯(茂,
Cyclo
pentadiene)配體。根據IUPAC對元素的命名規則,新元素的提議名稱是不得與其他元素名稱或符號重複的。考慮到上述情況,為了避免歧義,IUPAC已把提議中的符號Cp改為
Cn(
Coper
nicium)。
2010年2月19日,德國重離子研究所正式宣布,經國際純粹與套用化學聯合會確認,由該所人工合成的第112號化學元素從即日起獲正式名稱“Copernicium”,相應的元素符號為“Cn”。
在台灣,此元素之中文名稱由
國立編譯館化學名詞審議委員會和中國化學會名詞委員會開會討論後決定命名為
鎶。
核合成
主條目:鿔的同位素
超重元素如鿔是由
粒子加速器轟擊輕元素,誘導核聚變反應。大部分鿔的同位素可用這種方式直接合成,一些較重的只能作為更重元素的衰變產物被觀測到。
核融合反應根據所涉及的能量被分為“熱聚變”和“冷聚變”。在熱核聚變反應,很輕和高能量彈加速撞向非常重的目標(多數都是
錒系元素),從而引發複合核在高激發能(40-50
MeV),可能會蒸發掉幾個(3至5個)中子。在
冷聚變反應,產生的融合原子核有一個相對較低的激發能(10-20MeV),從而降低發生裂變反應的機率。由於融合核冷卻到
基態,它們需要排放的只有一個或兩個中子,因此,允許產生更多的富含中子的產物。後者是一個獨特的概念,從這個地方核聚變聲稱要實現在室溫條件下(見
冷聚變)。
冷聚變
在1996年重離子研究所首次進行合成鿔的
冷核聚變反應,並報告檢測到兩個Cn的衰變鏈。
2000年,他們撤回了此前的發表。在2000年重複的反應,他們希望能夠進一步合成鿔原子。他們企圖測量1N激發能,但在2002年的Zn束遭受了失敗。
Cn的發現在2004年被
日本理化學研究所證實,那裡的研究人員進一步發現兩個原子的同位素,並能確認整個衰變鏈的衰變數據。
Cn合成成功後,重離子研究所在1997年使用Zn進行了反應,研究
同位旋(富含中子)對化學產量的影響。
該實驗開始後,採用Ni離子合成一個𫟼同位素。由於沒有檢測到Cn的衰變鏈導致截面限制在1.2 PB。
1990年,一些初步跡象顯示,鿔的同位素在多GeV的質子照射鎢靶的情況下形成,重離子研究所和
耶路撒冷大學合作研究了下列反應。
他們探測到一些
自發裂變活動和12.5MeV的
α衰變,這兩者給指向輻射俘獲產品Cn或1N蒸發殘渣Cn。技術工作組和聯合工作方案的結論是需要更多的研究來證實這些結論。
熱聚變
1998年,俄羅斯杜布納Flerov核研究實驗室(FLNR)開始了一個研究項目:使用鈣-48核的“暖”聚變反應,合成超重元素。
新合成的Cn自發裂變成較輕的核素,半衰期約為5分鐘。
該產物的長半衰期使科學家發起第一次針對鿔的化學氣態實驗。2000年,杜布納的Yuri Yukashev重複實驗,但未能證實任何半衰期為5分鐘的自發裂變。2001年實驗被重複,自發裂變造成的八塊碎片被發現積累於低溫部分,表明了鿔類似氡的屬性。不過,有些科學家嚴重懷疑這些結果的由來。為了確認鿔的合成,同樣的團隊在2003年1月成功地重複了反應,證實了衰變模式和半衰期。他們還能夠計算出估計的自發裂變活動質量至285。
在2003-2004年杜布納的團隊使用稍微不同的設定:杜布納天然氣填充反衝分離器(DGFRS)重複反應。這一次,Cn被發現以9.53MeV進行α衰變,半衰期約為4分鐘。Cn也在4N通道被觀察到(蒸發掉4中子)。
2003年,德國重離子研究所進行了搜尋五分鐘自發裂變活性的化學實驗。像杜布納的團隊,他們能夠在低溫部分探測到七塊自發裂變碎片。然而,這些自發裂變事件不相關,這表明他們不是從實際直接自發裂變的鎶原子核,並對原本得出類似氡般的化學性能提出質疑。
在杜布納公布Cn不同的衰變屬性後,重離子研究所的團隊在2004年9月重複實驗。他們無法檢測到任何自發裂變事件和計算的截面限制1.6PB為檢測一個事件,而不是由杜布納報導的2.5PB產量。
2005年5月,重離子研究所進行了物理實驗,並確定了Cn的單個原子具有半衰期短的自發裂變,暗示以前未知的自發裂變分支。然而,杜布納初步共觀察了數次直接自發裂變事件,但已經錯過了母核的α衰變。這些結果表明情況並非如此。
Cn的新衰變數據被證實在2006年的PSI-FLNR聯合實驗(旨在探測鿔的化學性質)。Cn的兩個原子,被觀察到在Fl的衰變產物中。實驗表明,鿔表現為典型的12族成員,是化學性質不穩定的金屬。
最後,重離子研究所的小組在2007年1月成功地重複他們的物理實驗和檢測Cn的三個原子,確認雙方的α衰變和自發裂變的衰變模式。
因此,5分的自發裂變活動仍未經證實和不明。它可能是一個核異構體,即Cn,其截面依賴於準確的生產方法。
衰變產物
原子
鿔有基態電子組態[Rn]5f6d7s,所以鿔應該屬於周期表的12族,根據構造原理。因此,它應該表現為汞較重的同系物,形成強大的汞化合物與二元貴金屬如金。實驗探測反應性方面,鿔都集中在吸附的112號元素到金表面在不同溫度下進行,以計算出吸附焓值。由於相對穩定的7S電子,鿔表現出類似氡的屬性。實驗是同時形成的汞和氡放射性同位素,允許比較吸附特性。
第一個實驗使用了U(Ca,3n)Cn反應。檢測到自發裂變同位素與半衰期為5分鐘。分析數據表明,鿔比汞更不穩定和似乎具有惰性氣體的屬性。然而,就合成Cn懷疑這些實驗結果。由於這不確定性,JINR,FLNR-PSI團隊在2006年4月5月做了探查這同位素的綜合試驗Pu(Ca,3n)Fl。在這個實驗中,Cn的兩個原子被明確標識和吸附性能表示鿔是一個更不穩定的汞同系物,由於與黃金形成弱的金屬-金屬鍵,它被置於周期表的12族。
2007年4月,該實驗重複和另外三個Cn原子被驗明正身。吸附特性被證實,並表示鿔是具有吸附性能的。
推算的化學屬性
氧化態
鿔是6d系的最後一個過渡金屬,是
元素周期表中12族最重的元素,位於鋅、
鎘和汞下面。科學家預測,鿔與其他較輕的12族元素在屬性上有顯著差異。由於7s電子軌域的穩定加上
相對論效應,6d軌域較不穩定性,因此Cn離子的
電子排布很可能是[Rn]5f6d7s,這和同族元素是不同的。在水溶液中,鿔很可能形成+2和+4
氧化態,後者更穩定。在較輕的12族元素里,+2氧化態是最常見的,而只有汞能呈+4氧化態,但極少見。唯一一個已知的四價汞化合物(四氟化汞,HgF
4)也只能在極端條件下存在。類似的鎶化合物CnF
4、CnO
2預計將更加穩定。雙原子離子Hg中汞具有+1態,但是Cn離子預計將不穩定,甚至不存在。
原子氣態
鿔有基態電子排布為[Rn]5f6d7s,所以根據
構造原理,鿔應該屬於周期表的12族。因此,它的屬性應表現為汞的較重同系物,可與金等貴金屬形成
二元化合物。鿔的化學實驗主要研究鿔在不同溫度下在金箔表面的
吸附作用,從而計算出吸附焓值。由於7s軌域電子相對穩定,鿔表現出類似氡的屬性。實驗同時形成了汞和氡的
放射性同位素,這使科學家能夠比較這些元素的吸附特性。
最初的化學實驗使用了U(Ca,3n)Cn反應。實驗檢測到目標同位素的自發裂變,半衰期為5分鐘。分析數據表明,鿔的揮發性比汞高,並似乎具有
惰性氣體的屬性。然而,由於未能確定Cn同位素的發現,因此科學家對這些化學實驗結果是持著疑問的。2006年4月至5月,Flerov核研究實驗室和保羅謝爾研究所的聯合團隊在聯合核研究所進行了Fl的合成實驗:Pu(Ca,3n)Fl,並在衰變產物中對Cn進行研究。該實驗明確探測到兩個Cn原子,並發現鿔和金會產生弱金屬-金屬鍵。這意味著鿔是具高揮發性的鿔同系物,明確屬於12族。
2007年4月,科學家重複進行了這條反應,又合成了三個Cn原子。該實驗證實了鿔的吸附特性,結果表示鿔完全具有12族中的最重元素的應有屬性。




