高烯丙基醇,分子式C4H8O,分子量72.11。是合成某些天然產物、藥物、香料和農藥等的重要的中間體。
基本介紹
- 中文名:高烯丙基醇
- 外文名:3-Buten-1-ol
- 別名:3-丁烯-1醇
- 分子式:C4H8O
- 分子量:72.11
編號系統
物性數據
生態學數據
分子結構數據
計算化學數據
性質與穩定性
貯存方法
合成方法
電化學合成法
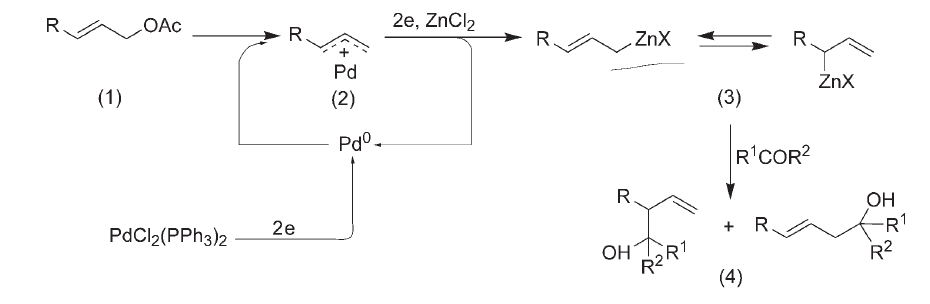
水相中高烯丙醇的電化學合成研究
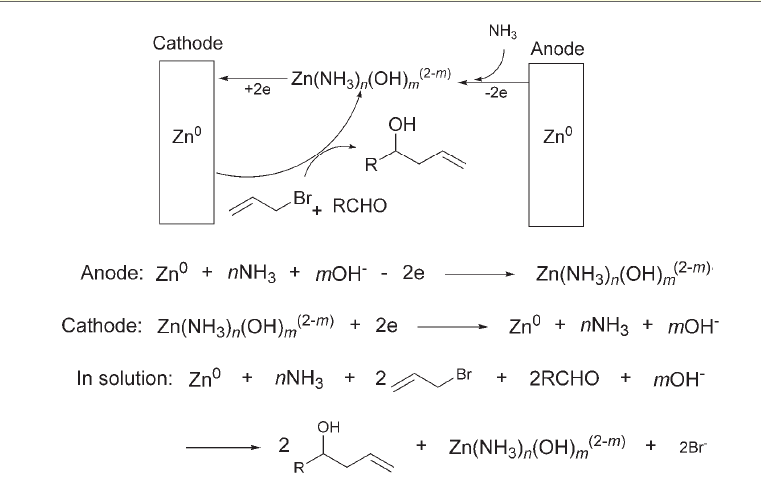
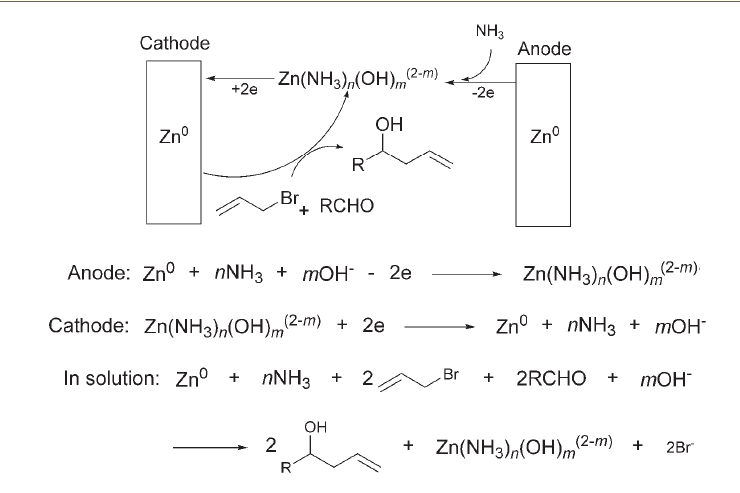
高烯丙基醇,分子式C4H8O,分子量72.11。是合成某些天然產物、藥物、香料和農藥等的重要的中間體。


高烯丙基醇,分子式C4H8O,分子量72.11。是合成某些天然產物、藥物、香料和農藥等的重要的中間體。編號系統CAS號:627-27-0MDL號:MFCD00002959EINECS號:210-991-3BRN號:163...
烯丙醇,又名蒜醇、2-丙烯-1-醇,是一種有機化合物,化學式為C₃H₆O,有劇 毒 ,是生產甘油、醫藥、農藥、香料和化妝品的中間體,也是生產鄰苯二甲酸二烯丙酯及雙(2,3-二溴丙基)反丁烯二酸酯的原料。基本信息 化學式...
d.與三乙基氯化矽發生親電取代反應生成烯丙基矽試劑;e.烯丙基的a氫經活化生成高烯丙醇;f . Grubbs催化劑催化作用下發生複分解反應生成新的烯烴;g.發生還原反應生成烷烴;h.發生聚合反應套用於高分子材料(圖6)。
1-丙烯-3-醇,又名2-丙烯-1-醇,丙烯醇,烯丙醇,乙烯甲醇。無色液體,有刺激性芥子氣味及催淚性。對眼睛有刺激性,有毒,其蒸氣與空氣形成爆炸性混合物。為製備甘油的原料,也用於製備增塑劑、樹脂、藥物等。用途 1-丙烯-3-醇...
環氧丙醇,又名縮水甘油,是一種有機化合物,化學式為C₃H₆O₂,為無色液體,主要用作環氧樹脂稀釋劑、塑膠和纖維改性劑、鹵代烴類的穩定劑、食品保藏劑、殺菌劑、製冷系統乾燥劑和芳烴萃取劑等。2017年10月27日,世界衛生組織...
烯丙醇縮水甘油醚,是一種有機化合物,化學式為C₆HO₂,主要用作合成偶聯劑,也可用作纖維改性劑、氯化有機物的穩定劑、合成樹脂反應性稀釋劑。理化性質 密度:0.962g/cm³ 熔點:-100℃ 沸點:154℃ 閃點:57℃ 折射率...
季碳中心的立體選擇性構築一直以來都是有機合成領域中的一個熱點內容,而半頻哪醇重排反應是實現該結構單元高效構築的重要策略之一。基於前期在相關領域的工作基礎,系統地開展了烯丙醇及其衍生物的半頻哪醇重排反應的研究。以金雞納鹼...
Geminal Bis(silane)]開展了系統的研究,並取得了以下三個方面的進展:(1)解決了構建偕雙矽這一空間極度擁擠結構的挑戰性難題,開發了偕雙矽烯醇衍生物、烯醛、二烯、高烯丙醇等結構多樣的偕雙矽合成子,實現了功能性偕雙矽多樣...
以氯化亞鐵為催化劑,實現了含三氟甲基烯烴底物的硼化/脫氟反應,生成了偕二氟烯丙基硼酸酯產物,生成的偕二氟烯丙基硼酸酯化合物具有較高的反應活性,易於轉化為相應的偕二氟烯丙醇、二氟甲基取代的硼酸酯、二氟取代高烯丙醇...
原料烯丙醇和含有過乙酸的乙酸乙酯溶液送入塔後,塔釜控制在60~70 ℃、13-20 kPa。塔頂蒸出乙酸乙酯溶劑和水,塔釜得至甘油水溶液。此法選擇性和收率均較高,採用過乙酸為氧化劑,可不用催化劑,反應速度較快,簡化了流程。生產1...
107-18-6指丙烯醇,分子式為C3H6O,分子量為58.08,是一種化學物質。物理化學性質 蒸汽密度:2 (vs air)蒸汽壓:23.8 mm Hg ( 25℃)凝固點:-129℃儲存條件:Flammables areaWGK Germany:2RTECS:BA5075000 危險品標誌 T ...
7.5.4 環烯丙醇、非環烯丙醇及高烯丙醇結構研究中的ECCD方法 286 7.5.5 ECCD差譜方法 289 7.5.6 非環狀-羥基酸及相關結構研究中的ECCD方法 290 7.5.7 非環狀多元醇結構研究中的ECCD方法 291 7.5.8 紅移效果...
原料烯丙醇和含有過乙酸的乙酸乙酯溶液送入塔後,塔釜控制在60-70℃、13-20kPa。塔頂蒸出乙酸乙酯溶劑和水,塔釜得至潔達水溶液。此法選擇性和收率均較高,採用過乙酸為氧化劑,可不用催化劑,反應速度較快,簡化了流程。生產1t...
烯丙型亞碸在P(OMe)₃存在下加熱,發生[2,3]-σ-單電子重排,得到次磺酸酯,進而在P(OMe)₃作用下轉化為烯丙醇的反應。此反應立體選擇性高。反應機理 此反應也可以利用烯丙位硫醚為底物,通過氧化,重排一鍋法得到烯丙醇類...
本課題的研究目標是衝擊合成高分子與生物大分子的界限。從合成高分子這邊出發,我們建立了一個基於烯丙醇類單體在原子轉移自由基聚合(ATRP)鏈端逐步單加成的方法,證明了其在單體水平上控制碳碳鏈序列結構的可行性,也就是我們其實可以...
步驟1)中所述起始劑為羥酯或端烯醇,前述羥酯或端烯醇選自丙烯酸羥乙酯,甲基丙烯酸羥乙酯,丙烯酸羥丙酯或甲基丙烯酸羥丙酯,烯丙醇;所述催化劑選自K₂O、Na₂O、NaOH、KOH、蒙脫土、累脫石、雙金屬氰化物、多金屬氰化物絡...
用鈉或鈉汞齊還原生成烯丙醇:與硫化氫反應生成1-氯-3-巰基-2-丙醇:與醇和酚在催化劑存在下發生反應,生成α-氯乙醇-γ-醚、縮水甘油醚或甘油-α,γ-二醚:環氧氯丙烷與氨或胺反應,生成1,3-二氨基丙醇或N-取代產物:與醛或...
規律:其反應難易程度取決於醇或酚的親核能力、位阻及醯化劑的活性。(1)醇的O-醯化一般規律是伯醇易於反應,仲醇次之,叔醇最難醯化。(2)伯醇中的苄醇、烯丙醇雖然不是叔醇,但由於易於脫羥基形成穩定的碳正離子,所以也表現出...
