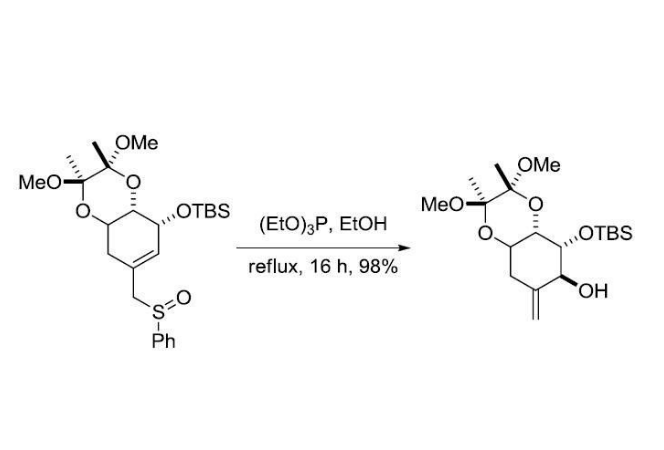
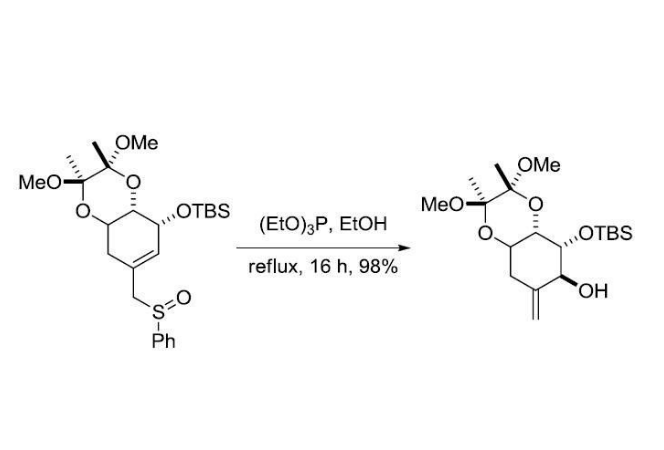
烯丙型亞碸在P(OMe)3存在下加熱,發生[2,3]-σ-單電子重排,得到次磺酸酯,進而在P(OMe)3作用下轉化為烯丙醇的反應。此反應立體選擇性高。
基本介紹
- 中文名:Mislow-Evans重排
- 底物:烯丙型亞碸
- 過程:[2,3]-σ-單電子重排
- 特點:立體選擇性高
反應機理,決定速率的因素,離去基團的鹼性,親核試劑的親核性,溶劑,空間效應,反應機理,
反應機理
此反應也可以利用烯丙位硫醚為底物,通過氧化,重排一鍋法得到烯丙醇類產物。常見的氧化劑有高點酸鈉,MoO5-Pyr-HMPA(MoOPH)和mCPBA。此反應的選擇性和取代基的大小有關,取代基越大,選擇性越好。
底物先進行[2,3]-σ-單電子重排,得到次磺酸酯,P(OMe)3再對次磺酸酯進行SN2取代脫硫,然後質子化得到烯丙醇產物。
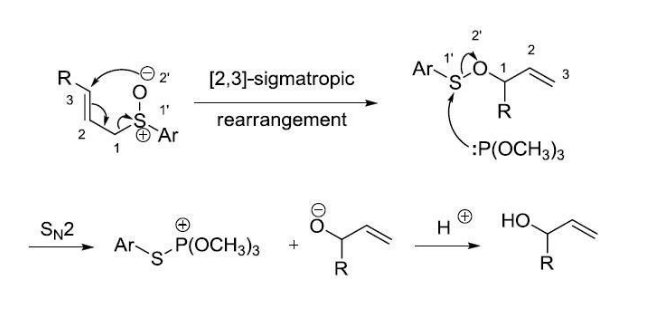
反應原理
SN2反應最常發生在脂肪族sp3雜化的碳原子上,碳原子與一個電負性強、穩定的離去基團(-X)相連,一般為鹵素陰離子。親核試劑(Nu)從離去基團的正後方進攻碳原子,Nu-C-X角度為180°,以使其孤對電子與C-X鍵的σ反鍵軌道可以達到最大重疊。然後形成一個五配位的反應過渡態,碳約為sp2雜化,用兩個垂直於平面的p軌道分別與離去基團和親核試劑成鍵。C-X的斷裂與新的C-Nu鍵的形成是同時的,-X很快離去,形成含C-Nu鍵的新化合物。
SN2反應一般發生在伯碳原子上,很難成為有位阻分子的反應機理,並且取代基越多,按SN2機理反應的可能性越小。基團在空間上比較擁擠的分子一般採用SN1機理,可以緩解一部分的位阻,也可生成較穩定的碳正離子(通常為三級碳正離子)。
由於親核試劑是從離去基團的背面進攻,故如果受進攻的原子具有手性,則反應後手性原子的立體化學發生構型翻轉,也稱“瓦爾登翻轉”。這也是SN2反應在立體化學上的重要特徵。反應過程類似於大風將雨傘由里向外翻轉。
決定速率的因素
離去基團的鹼性
離去基團的鹼性越強,其離去能力越弱,反之亦然。離子的鹼性隨著所在周期的增加而降低。對於鹵素離子而言,碘離子的鹼性最弱,因此碘離子是一個很好的離去基團;氟離子則相反,氟代烴也因此很難發生SN2反應。
親核試劑的親核性
親核性需要與上面的鹼性相區別。鹼性是試劑對質子的親和能力,而親核性是試劑形成過渡態時,對碳原子的親和能力。一般來講,試劑的負電性、鹼性和可極化性越強,其親核性也越強。實際上通常需要綜合考慮這幾個因素以及溶劑的影響。
溶劑
SN2反應在質子溶劑中進行時,一方面,溶劑化作用有利於離去集團的離去;另一方面,溶劑也會與親核試劑發生作用,使親核試劑與底物的接觸變得困難。最後的影響是這兩種因素的綜合結果。相對而言,非極性溶劑分子很少包圍負離子,因此對SN2反應是有利的。
空間效應
反應機理