編號系統
MDL號:MFCD00044636
EINECS號:232-148-9
RTECS號:ZC0230000
BRN號:暫無
PubChem號:24882119
物性數據
1. 性狀:無色、無味的液體,具有吸濕性,可與H2O任意混溶。
3. 相對蒸汽密度(g/mL,空氣=1):未確定
6. 沸點(ºC,5.2kPa):未確定
10. 自燃點或引燃溫度(ºC):未確定
12. 飽和蒸氣壓(kPa,60ºC):未確定
13. 燃燒熱(KJ/mol):未確定
16. 油水(辛醇/水)分配係數的對數值(25℃):未確定
17. 爆炸上限(%,V/V):未確定
18. 爆炸下限(%,V/V):未確定
生態學數據
對水是稍微危害的,若無政府許可,勿將材料排入周圍環境。
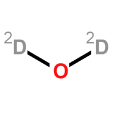
分子結構數據
計算化學數據
1.疏水參數計算參考值(XlogP):-0.5
2.氫鍵供體數量:1
3.氫鍵受體數量:1
4.可旋轉化學鍵數量:0
5.互變異構體數量:無
6.拓撲分子極性表面積1
7.重原子數量:1
8.表面電荷:0
9.複雜度:0
10.同位素原子數量:2
11.確定原子立構中心數量:0
12.不確定原子立構中心數量:0
13.確定化學鍵立構中心數量:0
14.不確定化學鍵立構中心數量:0
15.共價鍵單元數量:1
性質與穩定性
如果遵照規格使用和儲存則不會分解
避免接觸水分/潮濕
水溶液與
鹼金屬,
鹼土金屬和許多有機無機的活性化學藥品是不相溶的。25℃時的密度為1.1044kg/L,最大密度時的溫度為11.2℃。pKa=14.955(25℃)。
發現過程
1931年美國H.C.
尤里和F.G.布里克維德在液氫中發現氘,
1933年美國G.N.路易斯和R.T.麥克唐南利用減容
電解法得到0.5毫升重水,
純度為65.7%,再經電解,得0.1克接近純的重水。1934 年,
挪威利用廉價的水力發電,建立了世界上第一座重水生產工廠。
特性
重水在外觀上和普通水相似,只是密度略大,為1.1079克/立方厘米,
冰點略高,為3.82℃,沸點為101.42℃。參與化學反應的
速率比普通水緩慢、重水的一個分子是由兩個
重氫原子和一個氧原子組成,其分子式為D
2O,
相對分子質量是20。
重水與普通水看起來十分相像,是無臭無味的液體,它們的化學性質也一樣,不過某些物理性質卻不相同。普通水的密度為1克/厘米,而重水的密度為1.056克/厘米;普通水的沸點為100℃,重水的沸點為101.42℃;普通水的冰點為0℃,重水的冰點為 3.8℃。此外,普通水能夠滋養生命,培育萬物,而重水則不能使種子發芽。人和動物若是喝了重水,還會引起死亡。不過,重水的特殊價值體現於原子能技術套用中。製造威力巨大的核武器,就需要重水來作為原子核裂變反應中的減速劑,作中子的減速劑,也可作為制重氫的材料,普通水中含量約為0.02%(質量分數)。
| | |
相對密度 (20℃)
凝固點/℃
沸 點/℃
蒸發熱/kJ·mol-1
熔化熱/kJ·mol-1
凝固點降低/℃ | 0.997
0.00
100
40.67
6.008
1.86 | 1.108
3.79
101.41
41.6
6.276
2.00 |
重水製成的冰會沉入水中。
重水主要用於
核反應堆中作
減速劑,它可以減小
中子的速率,使之符合發生裂變過程的需要。重水也是研究化學和生理變化中使用過的材料。濃而純的重水不能維持動植物的生命,其致死濃度為60%~80%。
重水和普通水一樣,也是由
氫和
氧化合而成的液體化合物,不過,重水分子和普通水分子的氫原子有所不同。我們知道,氫有3種同位素。一種是氕,它只含有一個
質子。它和一個氧原子化合可以生成普通的水分子。另一種是
重氫——
氘。它含有一個質子和一個中子。它和一個氧原子化合後可以生成重水分子。還有一種是
超重氫——
氚。它含有兩個
中子和一個質子。
重水外觀上和普通水相似,是無色、無嗅無味的液體.密度比普通水大,熔點、沸點比普通水高.由於重水分子量大,運動速度慢,所以在高山上的冰雪中,特別是在南極的冰雪中重水含量微乎其微,水(氧化氫)的密度最小,是地球上最輕的水。重水在自然界中分布較少,在普通水中約含重水0.015%。由於含量少,製備難,所以它的售價較高(約16元/毫升)。
重水雖然在尖端技術上是寶貴的資源,但對人卻是有害的.人是不能飲用重水的,微生物、魚類在純重水或含重水較多(超過80%)的水中,只要數小時就會死亡.相反,含重水特別少的輕水,如
雪水,卻能刺激生物生長。
主要作用
重水的主要用途是在核反應堆中做“減速劑”,減小中子速度,控制核裂變過程,也是冷卻劑。重水和氘在研究化學和生理變化中是一種寶貴的示蹤材料,例如,用稀重水灌溉樹木,可以測知水在這些植物中每小時可運行十幾米到幾十米。測定飲過大量稀重水的人尿中的氘含量,知道水分子在人體中停留時間平均為14天。用氘代替普通氫,可以研究動植物消化和新陳代謝過程。濃的或純重水不能維持動植物生命,重水對一般動植物的致死濃度為60%。
重水的特殊價值體現於原子能技術套用中,要製造威力巨大的核武器,就需要重水作為
原子核裂變反應中的減速劑。
使用核磁共振分析時倘若溶劑是水,而研究的對象是氫,可以使用重水作溶劑。中子減速劑:某些核子反應堆使用重水來減慢中子的速度,讓它們有機會與鈾反應。輕水亦可以作減速劑,但因為輕水會吸收中子,因此輕水式反應堆必須使用濃縮鈾,而不能使用普通鈾,否則將不能達到臨界質量。重水反應堆不單可以使用普通鈾,而且會把
鈾238轉化成為可製作核彈的
鈽。印度、巴基斯坦、以色列、北韓都是以這樣方法製造核燃料。為了防止核子武器擴散,重水的生產和出售在很多國家都受到限制。
 用於核電站的重水
用於核電站的重水重水在尖端科技中有十分重要的用途。原子能發電站的心臟是原子反應堆,為了控制原子反應堆中核裂變反應的正常進行,需要用重水做
中子的減速劑.電解重水可以得到重氫,重氫是制氫彈的原料,中國已於1967年6月17日成功地爆炸了第一顆氫彈,增漲了中國人民的志氣.更重要的是重氫進行核聚變反應時,可放出巨大的能量,而且不會污染環境.有人計算推測,如果將海水中的重氫都用於熱核反應發電,其總能量相當於全部海洋都變成了石油。
生產方法
重水可以通過多種方法生產。最初的方法是用
電解法,因為重水無法電解,這樣可以從普通水中把它分離出來。還有一種簡單方法是利用重水沸點高於普通水通過反覆蒸餾得到。後來又發展了一些其他較佳的方法。
然而只有兩種方法已證明具有商業意義:水——
硫化氫交換法(GS法)和
氨——
氫交換法。
GS法是基於在一系列塔內(通過頂部冷和底部熱的方式操作)水和硫化氫之間氫與氘交換的一種方法。在此過程中,水向塔底流動,而硫化氫氣體從塔底向塔頂循環。使用一系列多孔塔板促進硫化氫氣體和水之間的混合。在低溫下氘向水中遷移,而在高溫下氘向硫化氫中遷移。氘被濃縮了的硫化氫氣體或水從第一級塔的熱段和冷段的接合處排出,並且在下一級塔中重複這一過程。最後一級的產品(氘濃縮至高達30%的水)送入一個蒸鎦單元以製備反應堆級的重水(即99.75%的
氧化氘)。
氨——氫交換法可以在催化劑存在下通過同
液態氨的接觸從合成氣中提取氘。合成氣被送進交換塔,而後送至氨轉換器。在交換塔內氣體從塔底向塔頂流動,而液氨從塔頂向塔底流動。氘從合成氣的氫中洗滌下來並在
液氨中濃集。液氨然後流入塔底部的氨裂化器,而氣體流入塔頂部的氨轉換器。在以後的各級中得到進一步濃縮,最後通過蒸餾生產出
反應堆級重水。合成氣進料可由氨廠提供,而這個氨廠也可以結合氨——氫交換法重水廠一起建造。氨—氫交換法也可以用普通水作為氘的供料源。利用GS法或氨—氫交換法生產重水的工廠所用的許多關鍵設備項目是與化學工業和石油工業的若干生產工序所用設備相同的。對於利用GS法的小廠來說尤其如此。然而,這種設備項目很少有“現貨”供應。GS法和氨—氫交換法要求在高壓下處理大量易燃、有腐蝕性和有毒的流體。因此,在制定使用這些方法的工廠和設備所用的設計和運行標準時,要求認真注意材料的選擇和材料的規格,以保證在長期服務中有高度的安全性和可靠性。規模的選擇主要取決於經濟性和需要。因而,大多數設備項目將按照用戶的要求製造。
 重水的生產
重水的生產最後,應該指出,對GS法和氨—氫交換法而言,那些單獨地看並非專門設計或製造用於重水生產的設備項目可以組裝成專門設計或製造用於生產重水的系統。氨—氫交換法所用的催化劑生產系統和在上述兩方法中將重水最終加濃至
反應堆級所用的水蒸餾系統就是此類系統的實例。
專門設計或製造用於利用GS法或氨—氫交換法生產重水的設備項目包括如下:
專門設計或製造用於利用GS法生產重水的、用優質碳鋼(例如ASTM A516)製造的交換塔。該塔直徑6米(20英尺)至9米(30英尺),能夠在大於或等於2兆帕(300磅/平方英寸)壓力下和6毫米或更大的腐蝕允量下運行。
2. 鼓風機和壓縮機
專門為利用GS法生產重水而設計或製造的用於循環硫化氫氣體(即含H2S 70%以上的氣體)的單級、低壓頭(即0.2兆帕或30磅/平方英寸)
離心式鼓風機或壓縮機。這些鼓風機或壓縮機的氣體通過能力大於或等於56立方米/秒(120000 標準立方英尺/分),能在大於或等於1.8兆帕(260磅/平方英寸)的吸入壓力下運行,並有對濕H2S介質的密封設計。
3.氨——氫交換塔
專門設計或製造用於利用氨——氫交換法生產重水的氨——氫交換塔。該塔高度大於或等於35米(114.3英尺),直徑1.5米(4.9英尺)至2.5米(8.2英尺),能夠在大於15兆帕(2225磅/平方英寸)壓力下運行。這些塔至少都有一個用法蘭聯結的軸向孔,其直徑與交換塔
筒體部分直徑相等,通過此孔可裝入或拆除塔內構件。
4. 塔內構件和多級泵
專門為利用氨——氫交換法生產重水而設計或製造的塔內構件和多級泵。塔內構件包括專門設計的促進氣/液充分接觸的多級接觸裝置。多級泵包括專門設計的用來將一個接觸級內的液氨向其他級塔循環的水下泵。
5. 氨裂化器
專門設計或製造的用於利用氨—氫交換法生產重水的氨裂化器。該裝置能在大於或等於3兆帕(450磅/平方英寸)的壓力下運行。
6. 紅外吸收分析器
能在氘濃度等於或高於90%的情況下“線上”分析氫/氘比的
紅外吸收分析器。
7. 催化燃燒器
專門設計或製造的用於利用氨—氫交換法生產重水時將濃縮氘氣轉化成重水的催化燃燒器。
提煉方法
地球上的水約有3,200分之一是
半重水(HDO)。半重水可以透過電解及蒸餾,或以化學方法從普通水中提煉出來。可以使用化學方法,是因為重氫及普通氫原子由於質量稍為不同,所以化學反應的速度有異。當水中的半重水到了相當的濃度,重水便會因為水分子之間交換氫原子而慢慢出現。要從半重水再提煉純正的重水亦可使用電解、蒸餾及化學方法。但是電解及
蒸餾所需要的能量會非常巨大,因此一般這一步只會使用化學方法。
 生產重水
生產重水健康問題
重水雖然在尖端技術上是寶貴的資源,但對人卻是有害的.人是不能飲用重水的,微生物、魚類在純重水或含重水較多(超過80%)的水中,只要數小時就會死亡.相反,含重水特別少的輕水,如
雪水,卻能刺激生物生長。
一般相信重水並不屬於有毒物質,但是人體內的某些代謝需要輕水,所以如果只喝重水會生病。因為重水中的D比H多一個中子,D重量是H的兩倍,導致其化學性質發生一定的改變以及物理性質的大幅改變。D的各種鍵比H強,而且更重的D的轉移速率會比H慢很多,導致關於D的化學反應會發生減速,干擾生物體正常代謝。
以老鼠做的實驗發現重水能抑制細胞的
有絲分裂,引起需要迅速代謝的身體組織變壞。實驗中的老鼠連續數天只喝重水後,體內約一半的體液變成重水;這時症狀開始出現,需要快速細胞分裂的組織,如髮根及胃膜最先出現毛病。本來快速增長的
癌細胞生長速度亦出現減慢,不過減慢的程度並不足以令重水作為可行的治療方法。
 用於核電站的重水
用於核電站的重水 重水的生產
重水的生產 生產重水
生產重水