基本介紹
- 中文名:標準摩爾反應焓變
- 外文名:Standard molar reaction enthalpy change
- 計算方法:方程式、生成焓、燃燒焓
理論基礎

相關定義
標準摩爾生成焓

標準摩爾燃燒焓

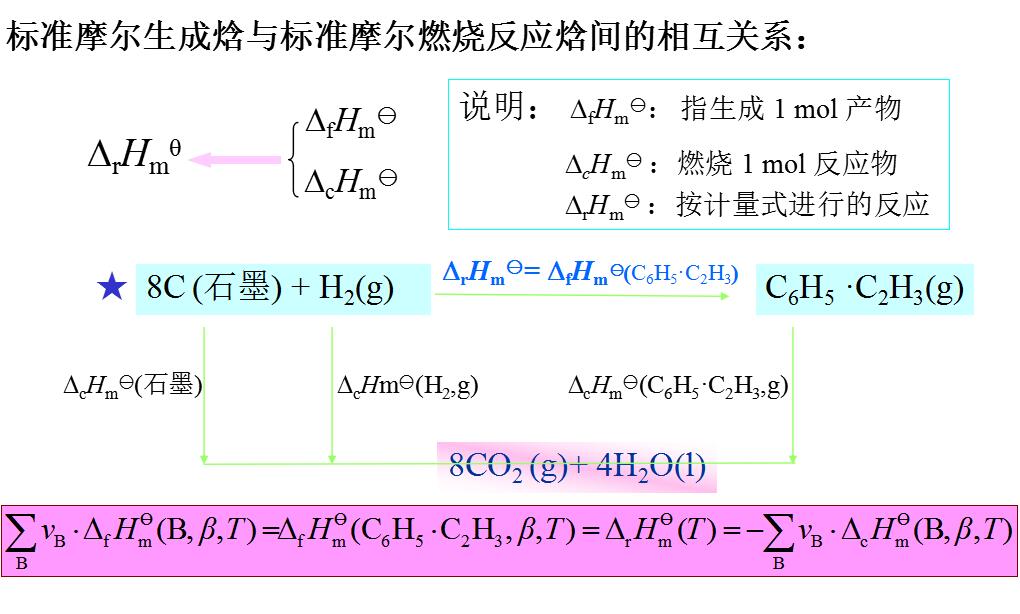
標準摩爾反應焓變的計算方法
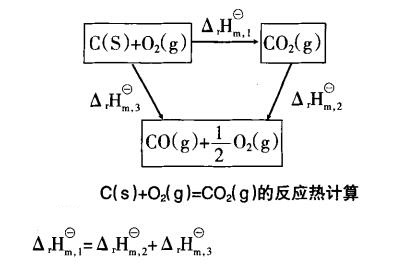
利用熱化學方程式的組合計算


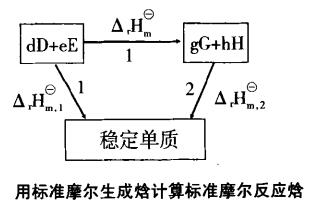
利用標準摩爾生成焓計算






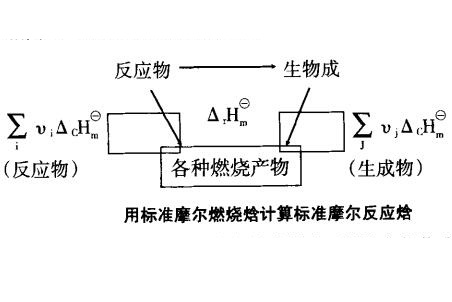
利用標準摩爾燃燒焓計算

利用水合離子的標準摩爾生成焓計算



利用鍵能估算























標準摩爾反應焓變是指參加反應的各物質都處於標準態時的反應焓變。熱力學是無機化學課程的重要組成部分,它是以熱力學第一定律、熱力學第二定律、熱力學第三定律為基礎,主要解決化學反應中能量轉化及化學反應進行的方向和程度問題,其中...
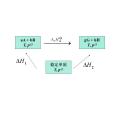
這個熱化學方程式表示:在標準狀態,298.15K時,發生了一個單位的反應,即1mol的Zn與1mol的CuSO₄發生置換反應生成1mol的ZnSO₄和1mol的Cu,此時的化學反應的焓變△Hₘ(298.15K)稱為298.15K時的標準摩爾焓變,其單位為kJ/mol...
在標準壓力(100kPa)下,在進行反應的溫度時,由最穩定的單質合成標準 壓力p下單位量物質B的反應焓變,叫做物質B的標準摩爾生成焓,用符號△Hₘ表示。定義 在標準壓力(100kPa)下,在進行反應的溫度時,由最穩定的單質合成標準 壓...
標準焓變是恆壓下,化學反應的焓變可由實驗測定Qp而得到,但一般也可利用熱力學數據計算得出,由於焓的絕對值和內能一樣,也是無法測定的。因而只能採取一些相對的標準,這樣可方便地計算反應的焓變,常把 △rHm一稱作標準摩爾焓變,△rHm...
標準摩爾燃燒焓是指一摩爾物質在標準狀況下完全燃燒時的反應焓變,用符號ΔHₘ表示,其中下標“c”表示燃燒(combustion),其單位為kJ/mol(又作kJ·mol)。如標準狀況下,甲烷完全燃燒時的反應式如下:CH₄(g) + 2 O₂(g) ...
計算標準反應焓 對任一化學反應,利用各種反應物和生成物的標準摩爾生成焓變的數據,就可以求得該反應的標準摩爾反應焓變 。物質的標準摩爾生成焓變的數值可從各種化學、化工手冊或熱力學數據手冊中查到。可以通過設定路徑來計算反應的...
標準燃燒焓 可燃物質B在標準的壓力下,反應溫度T時,單位量的物質B與氧進行完全氧化為同溫下指定產物時的標準摩爾焓變。用 (298.15K)表示。常見物質的標準摩爾生成焓 相關計算 標準摩爾生成焓計算標準摩爾反應焓 (產物生成焓)- (反應...
嚴格的標準熱化學方程式格式: H2(g)+1/2O2(g)==H2O(l) ΔrHθm=-286kJ·mol-1(θ表示標準態,r表示反應,m表示1mol反應.含義為標準態下進行一摩爾反應的焓變)我們構想在同一溫度下發生同上的1mol反應:2H2(g)+O2(g)=2H2O...
1.單質的標準摩爾生成焓為零。根據定義,由穩定單質生成穩定單質,也就是由自己生成自己,沒有發生變化,所以焓變為0,因此穩定單質的標準摩爾生成自由能為零。穩定單質大體包括(標態):全部金屬單質、惰性氣體單質、第二周期元素常見...
標準反應焓 標準反應焓(standard enthalpy of reaction)是2019年發布的物理學名詞。公布時間 2019年經全國科學技術名詞審定委員會審定發布。出處 《物理學名詞》第三版。
我們查閱了相關文獻,如北京師大五院校合編的《無機化學》(高等教育出版社1996版)第253頁上的解釋是:這裡的反應熱△H就是摩爾焓變(298K、101kPa時,下同),表示某反應按給定的反應方程式進行1mol反應,即ξ=1mol時的焓變。因...
(參考態元素的標準摩爾生成焓為0)定義為:在溫度T(若為298.15K時則可不標出)下,由標準狀態的單質生成物質B(νB=+1)反應的標準摩爾焓變。即在標準狀態下(反應物和產物都是處於100KPa,通常溫度選定298.15K),由指定單質生成...
當反應進度ξ=1mol,即反應按所給反應式的計量係數比例進行時,則ΔrH=ΔrUm,稱“摩爾反應熱力學能變”,而ΔrH=ΔrHm,稱“摩爾反應焓變”,其中下標符號γ意反應,m示摩爾,量綱單位為J·mol-1。現以A、D代表反應物而G、H...
2.4.2 規定熵和標準熵 2.4.3 由標準摩爾熵計算化學反應的標準摩爾反應熵變 2.5 亥姆霍茲函式和吉布斯函式 2.5.1 亥姆霍茲函式 2.5.2 吉布斯函式 2.6 化學反應中的熱力學函式變化 2.6.1 標準摩爾反應焓變ΔrH?m和標準摩爾...
其定義為:在標準狀況下,將1mol氣態分子AB(g)解離為氣態原子A(g),B(g)所需的能量,用符號E表示,單位為kJ.mol-1。鍵能的數值通常用該溫度下該反應的標準摩爾反應焓變表示,如不指明溫度,應為298.15K。生物分子中化學鍵能...
對於一個化學反應,可以像給出它的標準摩爾反應焓△Hₘ【Θ表示標準狀態(273K,101kPa)】一樣給出它的標準摩爾反應自由能變化△Gₘ。跟熱力學能變△U、焓變△H隨溫度與壓力的改變不會發生大的改變完全不同,反應自由能△Gₘ...
224標準摩爾反應焓變ΔrHm26 225熱化學反應方程式27 226蓋斯定律27 227標準摩爾反應焓變ΔrHm的計算29 23化學反應的自發方向31 231熵31 232化學反應方向的判據32 233標準摩爾生成吉布斯...
第九節摩爾溶解焓、摩爾稀釋焓及摩爾混合焓41 1摩爾溶解焓41 2摩爾稀釋焓41 3混合焓42 第十節由標準摩爾生成焓和標準摩爾燃燒反應焓計算標準摩爾反應焓42 1標準摩爾生成焓及由標準摩爾生成焓計算標準摩爾反應焓42 2標準...
本書主要介紹了物質與化學反應的計量、 物質的計量、化學反應的計量、化學熱力學的基本概念與術語、體系與環境、狀態與狀態函式、過程與途徑、熱、功、熱力學能、熱力學第一定律、熱化學、化學反應的熱效應、焓與焓變、標準摩爾反應焓,...
三、物質的標準態及標準摩爾反應焓111 四、定壓反應熱和定容反應熱112 五、蓋斯定律113 第八節熱化學基本數據與反應焓變的 計算114 一、標準摩爾生成焓ΔfHm115 二、由標準摩爾生成焓計算標準摩爾反 應焓115 三、標準摩爾燃燒焓Δ...
2.6.1反應的標準摩爾焓變/040 2.6.2等壓反應熱與等容反應熱的關係/041 2.6.3標準生成焓/043 2.6.4標準燃燒焓/044 2.6.5平均鍵焓/045 2.6.6反應焓變與溫度的關係/047 2.7熱力學第二定律/049 2.7.1熱力學第二定律...
3. 由原電池電動勢及電動勢的溫度係數計算電池反應的摩爾焓變 4. 計算原電池可逆放電時的反應熱 5. 能斯特方程 §7.7 電極電勢和液體接界電勢 1. 電極電勢 2. 原電池電動勢的計算 3. 液體接界電勢及其消除 §7.8 電極的種類...
