有機化學中的氧化還原反應,是指有機分子中碳原子或其他原子的氧化還原反應。在反應過程中通常涉及元素的電子得失或轉移。
(氧化)
氧化和還原總是同時發生的:有一方被氧化,必有另一方被還原。在有機化學中,反應屬性由有機物的變化來決定。
現在對氧化還原反應的判別,根據有機反應中有機化合物分子中鍵電子所發生的重新分布。如果某個元素在化學結合上分享的電荷有正、負的變化,包括正、零、負之間的變化,就認為是發生了氧化還原反應。如以下各反應中烴基碳原子的氧化數的變化:
(負→正,氧化反應)
(正→負,還原反應)
(零→正,氧化反應)
(正→零,還原反應)
(R:負→零,氧化反應)
(R′:正→零,還原反應)
式中R為烴基;X為鹵素。如果沒有這種變化或只有程度的差別,如正的更正,負的更負,就不是氧化還原反應。
氧化數的確定規則不很嚴格,例如同種元素之間的結合氧化數為零的規定。例如,乙酸中C─C的鍵電子並不是平均分布的,兩個碳原子的電荷是不相等的,但被人為地規定為平均分布,氧化數為零。在異種元素之間的結合中,一律規定電負性大的為負,小的為正。在重鍵結合中也不管其中是否有反向的鍵電子偏移,都按電負性和經典的化合價來確定氧化數。例如,一氧化碳C=O,儘管其中有鍵電子偏向於碳的,仍然規定碳的氧化數為+2,氧為-2。因此,用氧化數去考察一個反應,有時會出現問題。但在大多數場合,氧化數的概念能很好地套用,例如可用於反應類型的判別和通過反應方程式的配平進行定量計算等。
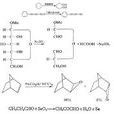
很多高效氧化劑能選擇性地氧化有機分子中各種不同的部位,如圖。
有機化學中的氧化還原反應氧化還原反應是重要的有機反應。在工業上,煤、石油的氧化燃燒能提供能源;火箭推進劑的燃燒能把宇宙飛船送上天空;對二甲苯可氧化成對苯二甲酸,是生產滌綸的原料:
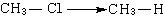 有機化學中的氧化還原反應
有機化學中的氧化還原反應 有機化學中的氧化還原反應
有機化學中的氧化還原反應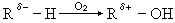 有機化學中的氧化還原反應
有機化學中的氧化還原反應 有機化學中的氧化還原反應
有機化學中的氧化還原反應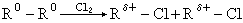 有機化學中的氧化還原反應
有機化學中的氧化還原反應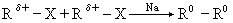 有機化學中的氧化還原反應
有機化學中的氧化還原反應 有機化學中的氧化還原反應
有機化學中的氧化還原反應 有機化學中的氧化還原反應
有機化學中的氧化還原反應 有機化學中的氧化還原反應
有機化學中的氧化還原反應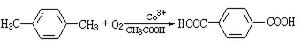 有機化學中的氧化還原反應
有機化學中的氧化還原反應