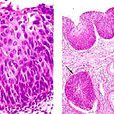
子 宮頸原位癌(cervical carcinoma in situ,CCIS)首先由Broder於1953年提出,1967年Richart[1]認為子宮頸上皮非典型增生和子宮頸原位癌同屬一種上皮變化譜, 有連續關係,是子宮頸浸潤癌的癌前病變,統稱為宮頸上皮內瘤變(cervical intraepithelial neoplasia,CIN)。
基本介紹
- 中文名:子宮頸原位癌
- 病變:是從宮頸上皮內瘤樣
- 常發生於:頸管下段移行帶附近
- 原因:HPV感染
病理現象,病理特點,原因,特點,檢查,注意事項,
病理現象
子宮頸原位癌是從宮頸上皮內瘤樣病變進展而來,包含在重度不典型增生即CINⅢ的分類中,它指的是當癌細胞占上皮內全層或接近全層,尚未穿破上皮基底膜侵入下方固有膜者。子宮頸原位癌的異型細胞比各級非典型增生者更具有顯著的多形性,上皮層完全為癌細胞所取代,細胞大小不一、形狀不一、排列紊亂、層次不清、極向消失。細胞核大而濃染、核漿比值增大,細胞膜、細胞間橋及細胞境界不清,核分裂像散見於全層,並且可見病理性核分裂像。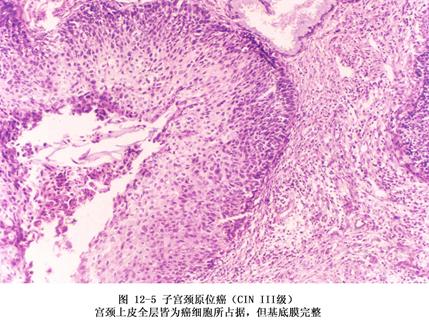 高倍鏡下的子宮頸原位癌
高倍鏡下的子宮頸原位癌
 高倍鏡下的子宮頸原位癌
高倍鏡下的子宮頸原位癌病理特點
當前關於子宮頸原位癌的病理特點有了進一步的認識。多數學者認為基底膜的完整與否並不是鑑別浸潤癌與原位癌的可靠指標,因為增值的基底膜細胞和炎細胞均可破壞基底膜,在良性的上皮腳周圍,基底膜可以消失,而在浸潤癌的邊緣可以見到完整的基底膜。
在浸潤病灶周圍的間質纖維組織顯得疏鬆,纖維收縮斷裂和間質的基質改變,由於基質的改變,在HE染色的切片上有一定程度的嗜鹼性,間質中有不等量的原形細胞浸潤;而在子宮頸原位癌中,病灶周圍雖然可可有明顯的炎細胞反應,但是無間質的改變。除了間質改變以外,腫瘤細胞的形態和排列亦有參考價值。
原因
人群、地域相關因素
患者的發病年齡和子宮頸浸潤癌有著不同的分布,子宮頸原位癌的發病年齡高峰為30~34歲,較宮頸浸潤癌的發病早20年或20多年,這種年齡分布特點反映了子宮頸原位癌患者接觸發病因素以後需要經過一段時間的進展才能夠發展成為宮頸浸潤癌。
HPV感染
HPV感染以後,經過感染潛伏期、亞臨床期才發展成為感染臨床期。HPV感染潛伏期是及其不穩定的時期,平均潛伏期為1-8個月。在最初感染的幾年內,多數婦女的症狀會轉歸、清除。當有嚴重的細胞調節免疫性損傷時,則會促使HPV大量複製,接著在表層和中層細胞核里逐漸出現大量的病毒DNA,因此會增加個體產生新的或者重複性損傷的可能性。
行為因素
(1) 性行為:大量的流行病學研究證實,性生活過早、多個性伴侶、性混亂等因素使子宮頸原位癌的危險性增高。
(4) 吸菸:吸菸作為HPV感染的協同因素可以增加子宮頸癌的患病風險,在吸菸者的宮頸黏液中可以檢測到尼古丁和菸草中的其他致癌成分,直接增加致癌的機會;另外部分學者認為吸菸者思想開放,持續感染HPV的機會較大。
特點
1.常發生於頸管下段移行帶附近;
2.也可局限於一個宮頸管黏膜息肉內;
3.可累及成組的腺體結構或單個腺體,呈芽狀生長入間質,使腺體呈篩狀改變,由上皮細胞構成的乳頭亦可穿入腺體內或突出於頸管表面,但非浸潤;
4.原位腺癌由假復層柱狀上皮構成。
檢查
1.細胞學檢查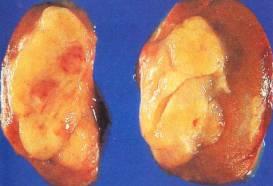 切除後的圖片
切除後的圖片
 切除後的圖片
切除後的圖片2.陰道鏡檢查
陰道鏡檢查是診斷CIN和早期宮頸癌的重要的輔助診斷方法。陰道鏡檢查可以發現較隱秘的病變部位,提高檢出率。在陰道鏡檢查的指導下活檢,能夠大大提高盲目活檢的準確性。如果細胞學診斷和陰道鏡檢查結果不一致,必要時還可以行頸管搔刮術,明確頸管有無病灶的可能。
3.宮頸錐切
宮頸錐切是非常傳統的診斷方法,此方法一度被忽視。由於陰道鏡的套用得到普遍開展,經過不斷的臨床實踐發現陰道鏡指導下的宮頸活檢仍然有其局限性,在陰道鏡指導下的宮頸活檢診斷的正確率為75%到90%,除了檢查者的經驗、素質以外,還與檢查技術本身的局限性有關。
注意事項
由於子宮頸病變的特點,大多數病例能夠得到及時準確的診斷。需要強調的是,子宮頸原位癌的診斷是建立在宮頸錐切病理診斷的基礎之上,因此,嚴格說來,陰道鏡指導下宮頸活檢得到宮頸原位癌的診斷結論並不太可靠,宮頸錐切後的診斷更加可信。
子宮頸原位癌治療以後隨訪十分重要。儘管治療後復發或者浸潤癌的風險降低,但是與普通人群相比,還是高很多。一般再術後3-6個月進行第一次複查,確定隨診計畫。當前較多採用是以細胞學為基礎的追蹤方法,有條件的考慮陰道鏡檢查。4-6個月1次,重複細胞學檢查滿2年,然後每年1次。
治療成功之後,宮頸HPV感染清除率很高,因此,HPV DNA檢測可以作為隨訪檢測的手段之一。為了給HPV感染的清除提供足夠時間,HPV DNA檢測應該在治療後6個月再開始檢測。