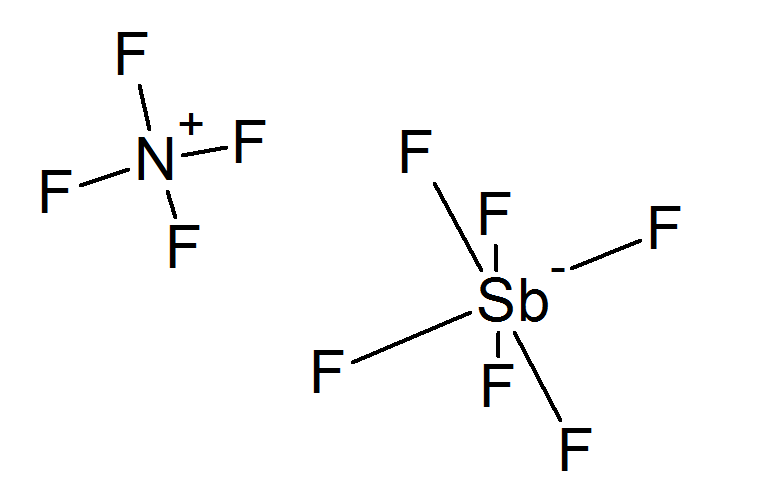
基本介紹
- 中文名:四氟銨
- 英文名:tetrafluoroammonium
- 化學式:NF4+
- 分子量:90.00
- CAS登錄號:暫無
- 熔點:無意義
- 沸點:無意義
- 水溶性:無意義
- 密度:無意義
- 外觀:無意義
- 閃點:無意義
- 套用:製取氟
- 安全性描述:無意義
- 危險性符號:第5.1類 氧化劑
- 危險性描述:氧化性,毒性
- 母體分子:五氟化氮
介紹,存在形式,結構,製備,反應,套用,其他,烯烴環氧化,羥基化,其他氧化反應,
介紹
存在形式
四氟銨的存在形式主要是一系列含氟陰離子的鹽。這些例子包括氟氫根離子(HF2−),四氟合溴酸根離子(BrF4−),金屬五氟化物陰離子(XF5−(X=Ge、Sn或Ti)),六氟化物陰離子(XF6−)(X=P、As、Sb、Bi或Pt),七氟化物陰離子(XF7−)(其中X是W、U或Xe),八氟化物陰離子(XeF82−), 許多種氟氧化物(XF5O-(X=W,U)、SO3F−(氟磺酸根)、BrF4O-)以及高氯酸根(ClO4−)。四氟銨的硝酸鹽NF4NO3,也已獲得。
結構
製備
- 四氟銨鹽的製備方法是在強路易斯酸(作為氟離子的受體)存在的條件下,用氟氧化三氟化氮製得。
Tolberg、Rewick、Stringham和Hill在1966年最早進行的製備實驗使用五氟化銻作為路易斯酸:
NF3+ F2+ SbF5→NF4SbF6 - NF4+鹽也可以通過二氟化氪(KrF2)氟化NF3來製備,作為路易斯酸的是氟化物MFn(其中M是Sb、Nb、Pt、Ti或B)。 比如,NF3與KrF2和TiF4的反應生成[NF4]+2TiF62−:
- 2NF3 + 2KrF2 + TiF4 → [NF4]+2TiF62−+ 2Kr
反應
套用
其他
有報告顯示,四氟銨離子中氟離子帶少量正電荷,水解時中間產物為次氟酸,因此四氟銨鹽具有類似於氟和次氟酸的性質,可視為固體氟,四氟銨鹽加熱時可釋放出氟。因此四氟銨鹽能參與很多次氟酸能參與的反應,並且反應條件更加溫和。
它參與的反應大致可分為幾類:
烯烴環氧化
羥基化
對α-羥基羰基化合物的研究一直吸引著有機化學家的興趣。用氟氧酸作氧化劑氧化烯醇醚(通常為三甲矽基)製得α-羥基羰基化合物的方法,避免了其他方法殘留的重金屬廢料,減少了對環境的污染。一般認為該反應中氟氧酸先對烯醇的雙鍵進行環氧化,然後氟離子和水分子對環碳原子的親核進攻,引入羥基,三元環打開。而後氟、羥基及矽基離去,恢復羰基,得到α-羥基羰基化合物。
下圖中的化合物與1,2-茚二酮都可用於檢驗指紋。在製備方面,氟氧酸作原料的路線產率最高,有很強的優越性。
其他氧化反應
①氧化硫醚為碸