前言,範圍,離子色譜法,原理,試劑和材料,儀器和設備,分析步驟,分析結果的表述,精密度,其他,分光光度法,原理,試劑和材料,儀器和設備,分析步驟,分析結果的表述,精密度,其他,蔬菜、水果中硝酸鹽的測定 紫外分光光度法,原理,試劑和材料,儀器和設備,分析步驟,結果計算,精密度,其他,附 錄 A,亞硝酸鹽和硝酸鹽標準溶液的色譜圖,
前言 本標準代替GB5009.33—2010《食品安全國家標準 食品中亞硝酸鹽與硝酸鹽的測定》、NY/T1375—2007《植物產品中亞硝酸鹽與硝酸鹽的測定 離子色譜法》、NY/T1279—2007《蔬菜、水果中硝酸鹽的測定 紫外分光光度法》、SN/T3151—2012《出口食品中亞硝酸鹽和硝酸鹽的測定 離子色譜法》。
本標準與GB5009.33—2010相比,主要變化如下:
———合併原第二法、第三法為第二法;
範圍 本標準規定了食品中亞硝酸鹽和硝酸鹽的測定方法。
本標準適用於食品中亞硝酸鹽和硝酸鹽的測定。
離子色譜法 原理 試樣經沉澱蛋白質、除去脂肪後,採用相應的方法提取和淨化,以氫氧化鉀溶液為淋洗液,陰離子交換柱分離,電導檢測器或紫外檢測器檢測。以保留時間定性,外標法定量。
試劑和材料 除非另有說明,本方法所用試劑均為分析純,水為GB/T6682規定的一級水。
試劑
乙酸(CH3COOH)。
氫氧化鉀(KOH)。
試劑配製
乙酸溶液(3%):量取乙酸3mL於100mL容量瓶中,以水稀釋至刻度,混勻。
氫氧化鉀溶液(1mol/L):稱取6g氫氧化鉀,加入新煮沸過的冷水溶解,並稀釋至100mL,混勻。
標準品
亞硝酸鈉(NaNO2,CAS號:7632-00-0):基準試劑,或採用具有標準物質證書的亞硝酸鹽標準溶液。
硝酸鈉(NaNO3,CAS號:7631-99-4):基準試劑,或採用具有標準物質證書的硝酸鹽標準溶液。
標準溶液的製備
亞硝酸鹽標準儲備液(100mg/L,以NO2- 計,下同):準確稱取0.1500g於110℃~120℃乾燥至恆重的亞硝酸鈉,用水溶解並轉移至1000mL容量瓶中,加水稀釋至刻度,混勻。
硝酸鹽標準儲備液(1000mg/L,以NO3- 計,下同):準確稱取1.3710g於110℃~120℃乾燥至恆重的硝酸鈉,用水溶解並轉移至1000mL容量瓶中,加水稀釋至刻度,混勻。
亞硝酸鹽和硝酸鹽混合標準中間液:準確移取亞硝酸根離子(NO2- )和硝酸根離子(NO3- )的標準儲備液各1.0mL於100mL容量瓶中,用水稀釋至刻度,此溶液每升含亞硝酸根離子1.0mg和硝酸根離子10.0mg。
亞硝酸鹽和硝酸鹽混合標準使用液:移取亞硝酸鹽和硝酸鹽混合標準中間液,加水逐級稀釋,製成系列混合標準使用液,亞硝酸根離子濃度分別為0.02mg/L、0.04mg/L、0.06mg/L、0.08mg/L、0.10mg/L、0.15mg/L、0.20mg/L;硝酸根離子濃度分別為0.2mg/L、0.4mg/L、0.6mg/L、0.8mg/L、1.0mg/L、1.5mg/L、2.0mg/L。
儀器和設備 離子色譜儀:配電導檢測器及抑制器或紫外檢測器,高容量陰離子交換柱,50μL定量環。
食物粉碎機。
超音波清洗器。
分析天平:感量為0.1mg和1mg。
離心機:轉速≥10000r/min,配50mL離心管。
0.22μm 水性濾膜針頭濾器。
淨化柱:包括C18柱、Ag柱和Na柱或等效柱。
注射器:1.0mL和2.5mL。
注:所有玻璃器皿使用前均需依次用2mol/L 氫氧化鉀和水分別浸泡4h,然後用水沖洗3次~5次,晾乾備用。
分析步驟 試樣預處理
蔬菜、水果:將新鮮蔬菜、水果試樣用自來水洗淨後,用水沖洗,晾乾後,取可食部切碎混勻。將切碎的樣品用四分法取適量,用食物粉碎機製成勻漿,備用。如需加水應記錄加水量。
糧食及其他植物樣品:除去可見雜質後,取有代表性試樣50g~100g,粉碎後,過0.30mm 孔篩,混勻,備用。
肉類、蛋、水產及其製品:用四分法取適量或取全部,用食物粉碎機製成勻漿,備用。
乳粉、豆奶粉、嬰兒配方粉等固態乳製品(不包括乾酪):將試樣裝入能夠容納2倍試樣體積的帶蓋容器中,通過反覆搖晃和顛倒容器使樣品充分混勻直到使試樣均一化。
發酵乳、乳、煉乳及其他液體乳製品:通過攪拌或反覆搖晃和顛倒容器使試樣充分混勻。
乾酪:取適量的樣品研磨成均勻的泥漿狀。為避免水分損失,研磨過程中應避免產生過多的熱量。
提取
蔬菜、水果等植物性試樣:稱取試樣5g(精確至0.001g,可適當調整試樣的取樣量,以下相同),置於150mL具塞錐形瓶中,加入80mL水,1mL1mol/L氫氧化鉀溶液,超聲提取30min,每隔5min振搖1次,保持固相完全分散。於75℃水浴中放置5min,取出放置至室溫,定量轉移至100mL容量瓶中,加水稀釋至刻度,混勻。溶液經濾紙過濾後,取部分溶液於10000r/min離心15min,上清液備用。
肉類、蛋類、魚類、及其製品等:稱取試樣勻漿5g(精確至0.001g),置於150mL具塞錐形瓶中,加入80mL水,超聲提取30 min,每隔5 min 振搖1次,保持固相完全分散。於75 ℃水浴中放置5min,取出放置至室溫,定量轉移至100mL容量瓶中,加水稀釋至刻度,混勻。溶液經濾紙過濾後,取部分溶液於10000r/min離心15min,上清液備用。
醃魚類、醃肉類及其他醃製品:稱取試樣勻漿2g(精確至0.001g),置於150mL具塞錐形瓶中,加入80mL水,超聲提取30 min,每隔5 min 振搖1次,保持固相完全分散。於75 ℃水浴中放置5min,取出放置至室溫,定量轉移至100mL容量瓶中,加水稀釋至刻度,混勻。溶液經濾紙過濾後,取部分溶液於10000r/min離心15min,上清液備用。
乳:稱取試樣10g(精確至0.01g),置於100mL具塞錐形瓶中,加水80mL,搖勻,超聲30min,加入3%乙酸溶液2mL,於4℃放置20min,取出放置至室溫,加水稀釋至刻度。溶液經濾紙過濾,濾液備用。
乳粉及乾酪:稱取試樣2.5g(精確至0.01g),置於100mL具塞錐形瓶中,加水80mL,搖勻,超聲30min,取出放置至室溫,定量轉移至100mL容量瓶中,加入3%乙酸溶液2mL,加水稀釋至刻度,混勻。於4℃放置20min,取出放置至室溫,溶液經濾紙過濾,濾液備用。
取上述備用溶液約15mL,通過0.22μm 水性濾膜針頭濾器、C18柱,棄去前面3mL(如果氯離子大於100mg/L,則需要依次通過針頭濾器、C18柱、Ag柱和Na柱,棄去前面7mL),收集後面洗脫液待測。
固相萃取柱使用前需進行活化,C18柱(1.0mL)、Ag柱(1.0mL)和Na柱(1.0mL),其活化過程為:C18柱(1.0mL)使用前依次用10mL甲醇、15mL水通過,靜置活化30min。Ag柱(1.0mL)和Na柱(1.0mL)用10mL水通過,靜置活化30min。
儀器參考條件
色譜柱:氫氧化物選擇性,可兼容梯度洗脫的二乙烯基苯-乙基苯乙烯共聚物基質,烷醇基季銨鹽功能團的高容量陰離子交換柱,4mm×250mm(帶保護柱4mm×50mm),或性能相當的離子色譜柱。
淋洗液
氫氧化鉀溶液,濃度為6mmol/L~70mmol/L;洗脫梯度為6mmol/L30min,70mmol/L5min,6mmol/L5min;流速1.0mL/min。
粉狀嬰幼兒配方食品:氫氧化鉀溶液,濃度為5mmol/L~50mmol/L;洗脫梯度為5mmol/L33min,50mmol/L5min,5mmol/L5min;流速1.3mL/min。
抑制器。
檢測器:電導檢測器,檢測池溫度為35℃;或紫外檢測器,檢測波長為226nm。
進樣體積:50μL(可根據試樣中被測離子含量進行調整)。
測定
標準曲線的製作
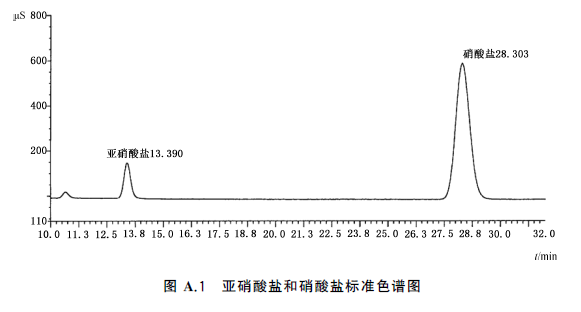
將標準系列工作液分別注入離子色譜儀中,得到各濃度標準工作液色譜圖,測定相應的峰高(μS)或峰面積,以標準工作液的濃度為橫坐標,以峰高(μS)或峰面積為縱坐標,繪製標準曲線(亞硝酸鹽和硝酸鹽標準色譜圖見圖A.1)。
試樣溶液的測定
將空白和試樣溶液注入離子色譜儀中,得到空白和試樣溶液的峰高(μS)或峰面積,根據標準曲線得到待測液中亞硝酸根離子或硝酸根離子的濃度。
分析結果的表述 試樣中亞硝酸離子或硝酸根離子的含量按式(1)計算:
式中:
X ———試樣中亞硝酸根離子或硝酸根離子的含量,單位為毫克每千克(mg/kg);
ρ ———測定用試樣溶液中的亞硝酸根離子或硝酸根離子濃度,單位為毫克每升(mg/L);
ρ0 ———試劑空白液中亞硝酸根離子或硝酸根離子的濃度,單位為毫克每升(mg/L);
V ———試樣溶液體積,單位為毫升(mL);
f ———試樣溶液稀釋倍數;
1000———換算係數;
m ———試樣取樣量,單位為克(g)。
試樣中測得的亞硝酸根離子含量乘以換算係數1.5,即得亞硝酸鹽(按亞硝酸鈉計)含量;試樣中測得的硝酸根離子含量乘以換算係數1.37,即得硝酸鹽(按硝酸鈉計)含量。
結果保留2位有效數字。
精密度 在重複性條件下獲得的兩次獨立測定結果的絕對差值不得超過算術平均值的10%。
其他 第一法中亞硝酸鹽和硝酸鹽檢出限分別為0.2mg/kg和0.4mg/kg。
分光光度法 原理 亞硝酸鹽採用鹽酸萘乙二胺法測定,硝酸鹽採用鎘柱還原法測定。
試樣經沉澱蛋白質、除去脂肪後,在弱酸條件下,亞硝酸鹽與對氨基苯磺酸重氮化後,再與鹽酸萘乙二胺偶合形成紫紅色染料,外標法測得亞硝酸鹽含量。採用鎘柱將硝酸鹽還原成亞硝酸鹽,測得亞硝酸鹽總量,由測得的亞硝酸鹽總量減去試樣中亞硝酸鹽含量,即得試樣中硝酸鹽含量。
試劑和材料 除非另有說明,本方法所用試劑均為分析純,水為GB/T6682規定的一級水。
試劑
亞鐵氰化鉀[K4Fe(CN)6·3H2O]。
乙酸鋅[Zn(CH3COO)2·2H2O]。
冰乙酸(CH3COOH)。
硼酸鈉(Na2B4O7·10H2O)。
鹽酸(HCl,ρ=1.19g/mL)。
氨水(NH3·H2O,25%)。
對氨基苯磺酸(C6H7NO3S)。
鹽酸萘乙二胺(C12H14N2·2HCl)。
鋅皮或鋅棒。
硫酸鎘(CdSO4·8H2O)。
硫酸銅(CuSO4·5H2O)。
試劑配製
亞鐵氰化鉀溶液(106g/L):稱取106.0g亞鐵氰化鉀,用水溶解,並稀釋至1000mL。
乙酸鋅溶液(220g/L):稱取220.0g乙酸鋅,先加30mL冰乙酸溶解,用水稀釋至1000mL。
飽和硼砂溶液(50g/L):稱取5.0g硼酸鈉,溶於100mL熱水中,冷卻後備用。
氨緩衝溶液(pH9.6~9.7):量取30mL鹽酸,加100mL水,混勻後加65mL氨水,再加水稀釋至1000mL,混勻。調節pH 至9.6~9.7。
氨緩衝液的稀釋液:量取50mLpH9.6~9.7氨緩衝溶液,加水稀釋至500mL,混勻。
鹽酸(0.1mol/L):量取8.3mL鹽酸,用水稀釋至1000mL。
鹽酸(2mol/L):量取167mL鹽酸,用水稀釋至1000mL。
鹽酸(20%):量取20mL鹽酸,用水稀釋至100mL。
對氨基苯磺酸溶液(4g/L):稱取0.4g對氨基苯磺酸,溶於100mL20%鹽酸中,混勻,置棕色瓶中,避光保存。
鹽酸萘乙二胺溶液(2g/L):稱取0.2g鹽酸萘乙二胺,溶於100mL水中,混勻,置棕色瓶中,避光保存。
硫酸銅溶液(20g/L):稱取20g硫酸銅,加水溶解,並稀釋至1000mL。
硫酸鎘溶液(40g/L):稱取40g硫酸鎘,加水溶解,並稀釋至1000mL。
乙酸溶液(3%):量取冰乙酸3mL於100mL容量瓶中,以水稀釋至刻度,混勻。
標準品
亞硝酸鈉(NaNO2,CAS號:7632-00-0):基準試劑,或採用具有標準物質證書的亞硝酸鹽標準溶液。
硝酸鈉(NaNO3,CAS號:7631-99-4):基準試劑,或採用具有標準物質證書的硝酸鹽標準溶液。
標準溶液配製
亞硝酸鈉標準溶液(200μg/mL,以亞硝酸鈉計):準確稱取0.1000g於110℃~120℃乾燥恆重的亞硝酸鈉,加水溶解,移入500mL容量瓶中,加水稀釋至刻度,混勻。
硝酸鈉標準溶液(200μg/mL,以亞硝酸鈉計):準確稱取0.1232g於110℃~120℃乾燥恆重的硝酸鈉,加水溶解,移入500mL容量瓶中,並稀釋至刻度。
亞硝酸鈉標準使用液(5.0μg/mL):臨用前,吸取2.50mL亞硝酸鈉標準溶液,置於100mL容量瓶中,加水稀釋至刻度。
硝酸鈉標準使用液(5.0μg/mL,以亞硝酸鈉計):臨用前,吸取2.50mL硝酸鈉標準溶液,置於100mL容量瓶中,加水稀釋至刻度。
儀器和設備 天平:感量為0.1mg和1mg。
組織搗碎機。
超音波清洗器。
恆溫乾燥箱。
分光光度計。
鎘柱或鍍銅鎘柱。
海綿狀鎘的製備:鎘粒直徑0.3mm~0.8mm。
將適量的鋅棒放入燒杯中,用40g/L硫酸鎘溶液浸沒鋅棒。在24h之內,不斷將鋅棒上的海綿狀鎘輕輕刮下。取出殘餘鋅棒,使鎘沉底,傾去上層溶液。用水沖洗海綿狀鎘2 次~3 次後,將鎘轉移至攪拌器中,加400mL鹽酸(0.1mol/L),攪拌數秒,以得到所需粒徑的鎘顆粒。將製得的海綿狀鎘倒回燒杯中,靜置3h~4h,期間攪拌數次,以除去氣泡。傾去海綿狀鎘中的溶液,並可按下述方法進行鎘粒鍍銅。
鎘粒鍍銅:
將製得的鎘粒置錐形瓶中(所用鎘粒的量以達到要求的鎘柱高度為準),加足量的鹽酸(2mol/L)浸沒鎘粒,振盪5min,靜置分層,傾去上層溶液,用水多次沖洗鎘粒。在鎘粒中加入20g/L硫酸銅溶液(每克鎘粒約需2.5mL),振盪1min,靜置分層,傾去上層溶液後,立即用水沖洗鍍銅鎘粒(注意鎘粒要始終用水浸沒),直至沖洗的水中不再有銅沉澱。
鎘柱的裝填:
如圖1所示,用水裝滿鎘柱玻璃柱,並裝入約2cm 高的玻璃棉做墊,將玻璃棉壓向柱底時,應將其中所包含的空氣全部排出,在輕輕敲擊下,加入海綿狀鎘至8cm~10cm[見圖1裝置a)]或15cm~20cm[見圖1裝置b)],上面用1cm 高的玻璃棉覆蓋。若使用裝置b),則上置一貯液漏斗,末端要穿過橡皮塞與鎘柱玻璃管緊密連線。
如無上述鎘柱玻璃管時,可以25mL酸式滴定管代用,但過柱時要注意始終保持液面在鎘層之上。
當鎘柱填裝好後,先用25mL鹽酸(0.1mol/L)洗滌,再以水洗2次,每次25mL,鎘柱不用時用水封蓋,隨時都要保持水平面在鎘層之上,不得使鎘層夾有氣泡。
圖1 鎘柱示意圖 說明:
1 ———貯液漏斗,內徑35mm,外徑37mm;
2 ———進液毛細管,內徑0.4mm,外徑6mm;
3 ———橡皮塞;
4 ———鎘柱玻璃管,內徑12mm,外徑16mm;
5、7———玻璃棉;
6 ———海面狀鎘;
8 ———出液毛細管,內徑2mm,外徑8mm。
鎘柱每次使用完畢後,應先以25mL鹽酸(0.1mol/L)洗滌,再以水洗2次,每次25mL,最後用水覆蓋鎘柱。
鎘柱還原效率的測定:吸取20mL硝酸鈉標準使用液,加入5mL氨緩衝液的稀釋液,混勻後注入貯液漏斗,使流經鎘柱還原,用一個100 mL 的容量瓶收集洗提液。洗提液的流量不應超過6mL/min,在貯液杯將要排空時,用約15mL水沖洗杯壁。沖洗水流盡後,再用15mL水重複沖洗,第2次沖洗水也流盡後,將貯液杯灌滿水,並使其以最大流量流過柱子。當容量瓶中的洗提液接近100mL時,從柱子下取出容量瓶,用水定容至刻度,混勻。取10.0mL還原後的溶液(相當10μg亞硝酸鈉)於50 mL 比色管中,以下按12.3 自“吸取0.00 mL、0.20 mL、0.40 mL、0.60 mL、0.80 mL、1.00mL……”起操作,根據標準曲線計算測得結果,與加入量一致,還原效率應大於95%為符合要求。
還原效率計算按式(2)計算:
式中:
X ———還原效率,%;
m1 ———測得亞硝酸鈉的含量,單位為微克(μg);
10 ———測定用溶液相當亞硝酸鈉的含量,單位為微克(μg)。
如果還原率小於95%時,將鎘柱中的鎘粒倒入錐形瓶中,加入足量的鹽酸(2moL/L)中,振盪數分鐘,再用水反覆沖洗。
分析步驟 試樣的預處理
同上一方法。
提取
乾酪:稱取試樣2.5g(精確至0.001g),置於150mL具塞錐形瓶中,加水80mL,搖勻,超聲30min,取出放置至室溫,定量轉移至100mL容量瓶中,加入3%乙酸溶液2mL,加水稀釋至刻度,混勻。於4℃放置20min,取出放置至室溫,溶液經濾紙過濾,濾液備用。
液體乳樣品:稱取試樣90g(精確至0.001g),置於250mL具塞錐形瓶中,加12.5mL飽和硼砂溶液,加入70℃左右的水約60mL,混勻,於沸水浴中加熱15min,取出置冷水浴中冷卻,並放置至室溫。定量轉移上述提取液至200mL容量瓶中,加入5mL106g/L亞鐵氰化鉀溶液,搖勻,再加入5mL220g/L乙酸鋅溶液,以沉澱蛋白質。加水至刻度,搖勻,放置30min,除去上層脂肪,上清液用濾紙過濾,濾液備用。
乳粉:稱取試樣10g(精確至0.001g),置於150mL具塞錐形瓶中,加12.5mL50g/L飽和硼砂溶液,加入70℃左右的水約150mL,混勻,於沸水浴中加熱15min,取出置冷水浴中冷卻,並放置至室溫。定量轉移上述提取液至200mL容量瓶中,加入5mL106g/L亞鐵氰化鉀溶液,搖勻,再加入5mL220g/L乙酸鋅溶液,以沉澱蛋白質。加水至刻度,搖勻,放置30min,除去上層脂肪,上清液用濾紙過濾,棄去初濾液30mL,濾液備用。
其他樣品:稱取5g(精確至0.001g)勻漿試樣(如製備過程中加水,應按加水量折算),置於250mL具塞錐形瓶中,加12.5mL50g/L飽和硼砂溶液,加入70℃左右的水約150mL,混勻,於沸水浴中加熱15min,取出置冷水浴中冷卻,並放置至室溫。定量轉移上述提取液至200mL容量瓶中,加入5mL106g/L亞鐵氰化鉀溶液,搖勻,再加入5mL220g/L乙酸鋅溶液,以沉澱蛋白質。加水至刻度,搖勻,放置30min,除去上層脂肪,上清液用濾紙過濾,棄去初濾液30mL,濾液備用。
亞硝酸鹽的測定
吸取40.0mL上述濾液於50mL帶塞比色管中,另吸取0.00mL、0.20mL、0.40mL、0.60mL、0.80mL、1.00mL、1.50mL、2.00mL、2.50mL亞硝酸鈉標準使用液(相當於0.0μg、1.0μg、2.0μg、3.0μg、4.0μg、5.0μg、7.5μg、10.0μg、12.5μg亞硝酸鈉),分別置於50mL帶塞比色管中。於標準管與試樣管中分別加入2mL4g/L對氨基苯磺酸溶液,混勻,靜置3min~5min後各加入1mL2g/L鹽酸萘乙二胺溶液,加水至刻度,混勻,靜置15min,用1cm 比色杯,以零管調節零點,于波長538nm 處測吸光度,繪製標準曲線比較。同時做試劑空白。
硝酸鹽的測定
鎘柱還原
先以25mL氨緩衝液的稀釋液沖洗鎘柱,流速控制在3mL/min~5mL/min(以滴定管代替的可控制在2mL/min~3mL/min)。
吸取20mL濾液於50mL燒杯中,加5mLpH9.6~9.7氨緩衝溶液,混合後注入貯液漏斗,使流經鎘柱還原,當貯液杯中的樣液流盡後,加15mL水沖洗燒杯,再倒入貯液杯中。沖洗水流完後,再用15mL水重複1次。當第2次沖洗水快流盡時,將貯液杯裝滿水,以最大流速過柱。當容量瓶中的洗提液接近100mL時,取出容量瓶,用水定容刻度,混勻。
亞硝酸鈉總量的測定
吸取10mL~20mL還原後的樣液於50mL比色管中。以下按12.3自“吸取0.00mL、0.20mL、0.40mL、0.60mL、0.80mL、1.00mL……”起操作。
分析結果的表述 亞硝酸鹽含量計算
亞硝酸鹽(以亞硝酸鈉計)的含量按式(3)計算:
式中:
X1 ———試樣中亞硝酸鈉的含量,單位為毫克每千克(mg/kg);
m2 ———測定用樣液中亞硝酸鈉的質量,單位為微克(μg);
1000———轉換係數;
m3 ———試樣質量,單位為克(g);
V1 ———測定用樣液體積,單位為毫升(mL);
V0 ———試樣處理液總體積,單位為毫升(mL)。
結果保留2位有效數字。
硝酸鹽含量的計算
硝酸鹽(以硝酸鈉計)的含量按式(4)計算:
式4 式中:
X2 ———試樣中硝酸鈉的含量,單位為毫克每千克(mg/kg);
m4 ———經鎘粉還原後測得總亞硝酸鈉的質量,單位為微克(μg);
1000———轉換係數;
m5 ———試樣的質量,單位為克(g);
V3 ———測總亞硝酸鈉的測定用樣液體積,單位為毫升(mL);
V2 ———試樣處理液總體積,單位為毫升(mL);
V5 ———經鎘柱還原後樣液的測定用體積,單位為毫升(mL);
V4 ———經鎘柱還原後樣液總體積,單位為毫升(mL);
X1 ———由式(3)計算出的試樣中亞硝酸鈉的含量,單位為毫克每千克(mg/kg);
1.232———亞硝酸鈉換算成硝酸鈉的係數。
結果保留2位有效數字。
精密度 在重複性條件下獲得的兩次獨立測定結果的絕對差值不得超過算術平均值的10%。
其他 第二法中亞硝酸鹽檢出限:液體乳0.06mg/kg,乳粉0.5mg/kg,乾酪及其他1mg/kg;硝酸鹽檢出限:液體乳0.6mg/kg,乳粉5mg/kg,乾酪及其他10mg/kg。
蔬菜、水果中硝酸鹽的測定 紫外分光光度法 原理 用pH9.6~9.7的氨緩衝液提取樣品中硝酸根離子,同時加活性炭去除色素類,加沉澱劑去除蛋白質及其他干擾物質,利用硝酸根離子和亞硝酸根離子在紫外區219nm 處具有等吸收波長的特性,測定提取液的吸光度,其測得結果為硝酸鹽和亞硝酸鹽吸光度的總和,鑒於新鮮蔬菜、水果中亞硝酸鹽含量甚微,可忽略不計。測定結果為硝酸鹽的吸光度,可從工作曲線上查得相應的質量濃度,計算樣品中硝酸鹽的含量。
試劑和材料 除非另有說明,本方法所用試劑均為分析純。水為GB/T6682規定的一級水。
試劑
鹽酸(HCl,ρ=1.19g/mL)。
氨水(NH3·H2O,25%)。
亞鐵氰化鉀[K4Fe(CN)6·3H2O]。
硫酸鋅(ZnSO4·7H2O)。
正辛醇(C8H18O)。
活性炭(粉狀)。
試劑配製
氨緩衝溶液(pH=9.6~9.7):量取20mL鹽酸,加入到500mL水中,混合後加入50mL氨水,用水定容至1000mL。調pH 至9.6~9.7。
亞鐵氰化鉀溶液(150g/L):稱取150g亞鐵氰化鉀溶於水,定容至1000mL。
硫酸鋅溶液(300g/L):稱取300g硫酸鋅溶於水,定容至1000mL。
標準品
硝酸鉀(KNO3,CAS號:7757-79-1):基準試劑,或採用具有標準物質證書的硝酸鹽標準溶液。
標準溶液配製
硝酸鹽標準儲備液(500mg/L,以硝酸根計):稱取0.2039g於110℃~120℃乾燥至恆重的硝酸鉀,用水溶解並轉移至250 mL 容量瓶中,加水稀釋至刻度,混勻。此溶液硝酸根質量濃度為500mg/L,於冰櫃內保存。
硝酸鹽標準曲線工作液:分別吸取0mL、0.2mL、0.4mL、0.6mL、0.8mL、1.0mL和1.2mL硝酸鹽標準儲備液於50mL容量瓶中,加水定容至刻度,混勻。此標準系列溶液硝酸根質量濃度分別為0mg/L、2.0mg/L、4.0mg/L、6.0mg/L、8.0mg/L、10.0mg/L和12.0mg/L。
儀器和設備 紫外分光光度計。
分析天平:感量0.01g和0.0001g。
組織搗碎機。
可調式往返振盪機。
pH 計:精度為0.01。
分析步驟 試樣製備
選取一定數量有代表性的樣品,先用自來水沖洗,再用水清洗乾淨,晾乾表面水分,用四分法取樣,切碎,充分混勻,於組織搗碎機中勻漿(部分少汁樣品可按一定質量比例加入等量水),在勻漿中加1滴正辛醇消除泡沫。
提取
稱取10g(精確至0.01g)勻漿試樣(如製備過程中加水,應按加水量折算)於250mL錐形瓶中,加水100mL,加入5mL氨緩衝溶液(pH=9.6~9.7),2g粉末狀活性炭。振盪(往復速度為200次/min)30min。定量轉移至250mL容量瓶中,加入2mL150g/L亞鐵氰化鉀溶液和2mL300g/L硫酸鋅溶液,充分混勻,加水定容至刻度,搖勻,放置5min,上清液用定量濾紙過濾,濾液備用。同時做空白實驗。
測定
根據試樣中硝酸鹽含量的高低,吸取上述濾液2mL~10mL於50mL容量瓶中,加水定容至刻度,混勻。用1cm 石英比色皿,於219nm 處測定吸光度。
標準曲線的製作
將標準曲線工作液用1cm 石英比色皿,於219nm 處測定吸光度。以標準溶液質量濃度為橫坐標,吸光度為縱坐標繪製工作曲線。
結果計算 硝酸鹽(以硝酸根計)的含量按式(5)計算:
式中:
X ———試樣中硝酸鹽的含量,單位為毫克每千克(mg/kg);
ρ ———由工作曲線獲得的試樣溶液中硝酸鹽的質量濃度,單位為毫克每升(mg/L);
V6———提取液定容體積,單位為毫升(mL);
V8———待測液定容體積,單位為毫升(mL);
m6———試樣的質量,單位為克(g);
V7———吸取的濾液體積,單位為毫升(mL)。
結果保留2位有效數字。
精密度 在重複性條件下獲得的兩次獨立測定結果的絕對差值不得超過算術平均值的10%。
其他 第三法中硝酸鹽檢出限為1.2mg/kg。
附 錄 A 亞硝酸鹽和硝酸鹽標準溶液的色譜圖 見圖A.1。
圖A.1 亞硝酸鹽和硝酸鹽標準色譜圖

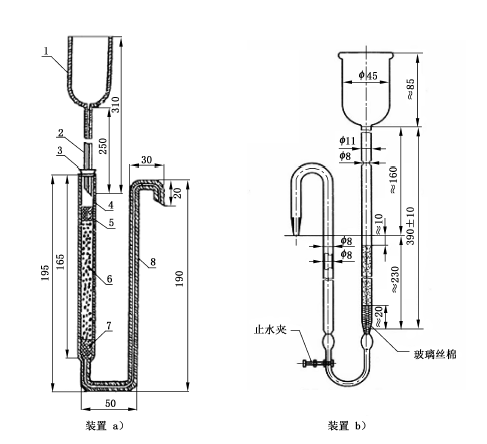 圖1 鎘柱示意圖
圖1 鎘柱示意圖
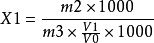
 式4
式4
 圖A.1 亞硝酸鹽和硝酸鹽標準色譜圖
圖A.1 亞硝酸鹽和硝酸鹽標準色譜圖
