專利背景
中藥
紅花為菊科植物CarthamustinctoriusL.的乾燥花,為一常用的活血化淤藥,可用於冠心病,心絞痛等諸多血液循環障礙疾病的治療。臨床上紅花以水煎液入藥,紅花黃色素為紅花的主要水溶性成分,為一混合查耳酮甙[參見.高其銘,中藥紅花的藥理研究概況,中西醫結合雜誌,1984,4(12):758-760.]紅花總黃色素粗品為一國家允許使用的食品色素(GB2760-86)[參見周立國,食用天然色素及其提取套用。158-160.濟南,山東科學技術出版社.],研究表明,它具多方面的心血管藥理作用,可抗凝,促進纖溶,抗血栓形成,改善微循環等[參見.高其銘,中藥紅花的藥理研究概況,中西醫結合雜誌,1984,4(12):758-760.]。此粗品紅花總黃色素的製備方法為水提醇沉法,因其未經層析等方法除雜質,其薄層圖譜為一從原點到前沿的拖尾色帶[參見天津醫藥工業研究所等,紅花的研究(二)紅花黃色素及其分離物的藥理研究。山西醫藥雜誌。1980:9(1)2-8],提示其純度較低。紅花總黃色素目前僅有水提醇沉法製得的粗品作為食品色素生產,尚無紅花總黃色素藥品或保健品製劑。
發明內容
專利目的
《紅花總黃色素及其製備方法和套用》提供了一種紅花總黃色素,該紅花總黃色素可用下述方法製得:以紅花為原料,加入適量的極性溶劑浸提,濾除藥渣合併浸提液,濃縮得到濃縮液;把經上述步驟得到的濃縮液進行柱層析,以極性洗脫液洗脫除去雜質後再以另一極性洗脫液洗脫紅花總黃色素;或以層析擔體對提取濃縮液進行吸附,以極性洗脫液直接洗下紅花總黃色素並使雜質吸附於層析擔體上,紅花總黃色素洗脫液回收溶劑,濃縮乾燥即得。
該發明還提供了一種紅花總黃色素的製備方法,該方法包括下述步驟:以紅花為原料,加入適量的極性溶劑浸提,濾除藥渣合併浸提液,濃縮得到提取濃縮液;把上述步驟得到的提取濃縮液進行柱層析,以極性洗脫液洗脫除去雜質後再以另一極性洗脫液洗脫紅花總黃色素;或以層析擔體對提取濃縮液進行吸附,以極性洗脫液直接洗下紅花總黃色素並使雜質吸附於層析擔體上,紅花總黃色素洗脫液回收溶劑,濃縮乾燥即得。
技術方案
在《紅花總黃色素及其製備方法和套用》的製備方法的一個優選實施方案中,所述的提取是以極性溶劑提取2-4次,每次1-3天,提取用極性溶劑用量為紅花生藥量的5-50倍。
在該發明的製備方法的另一優選實施方案中,所述的用於除雜質的紅花提取濃縮液濃度相當於0.5-10克生藥/毫升。
在該發明的製備方法的另一優選實施方案中,所述的柱層析除雜質方法為以聚醯胺柱層析法去除紅花提取濃縮液中的雜質,且其紅花提取濃縮液與所用聚醯胺粉之比按體積計為1:1-30。
在該發明的製備方法的另一優選實施方案中,所述的柱層析擔體除雜質方法是以矽膠吸附紅花提取濃縮液中的雜質,且其紅花提取濃縮液與所用矽膠粉之比按體積計為1:1-30。
在該發明的製備方法的另一優選實施方案中,所述的柱層析擔體除雜質方法是以大孔樹脂吸附紅花提取濃縮液中的紅花總黃色素,以洗脫液洗脫雜質,且其紅花提取濃縮液與所用大孔樹脂之比按體積計為1:1-30。
在該發明的製備方法的另一優選實施方案中,所述的極性洗脫液為水或者濃度為20-100重量百分比的乙醇,甲醇或丙醇水溶液。
在該發明的製備方法的另一優選實施方案中,所述的極性洗脫液為水或者濃度為40-95重量百分比的乙醇,甲醇或丙醇水溶液。
該發明提供了一種紅花總黃色素在製備預防及治療涉及組織缺血特別是心肌缺血及腦缺血,血栓形成及血小板激活因子與自由基所致損傷疾病的藥物中的套用。
該發明提供了一種紅花總黃色素在製備預防及治療涉及組織缺血特別是心肌缺血及腦缺血,血栓形成及血小板激活因子與自由基所致損傷疾病的保健品中的套用。
該發明提供了一種治療及預防心腦血管疾病等血液循環障礙性疾病的藥物,其中含有治療心腦血管等疾病有效量的紅花總黃色素和可藥用的載體。
該發明提供了一種治療及預防心腦血管疾病等血液循環障礙性疾病的保健品,其中含有治療心腦血管疾病有效量的紅花總黃色素和可藥用的載體。
該發明用於製備治療及預防涉及組織缺血特別是心肌缺血及腦缺血,血栓形成及具血小板激活因子及自由基損傷的血液循環障礙性疾病特別是血栓性疾病及心肌缺血性疾病的藥物及保健品組合物。此組合物含活性成分為紅花總黃色素及藥物可接受的賦形劑,載體或稀釋劑,以常規方法將其製成藥物或保健品製劑。
製備該組合物時,可將紅花總黃色素與載體混合或用載體包埋,此載體可以是膠囊或其他裝載形式。載體可為固體,半固體或液體物質,它作為紅花總黃色素的載體,賦形劑或介質。該組合物可以是片劑,丸劑,栓劑,粉末,醑劑,懸浮液,乳濁液,溶液,糖漿,注射劑等多種形式。
多種載體,賦形劑或稀釋劑可用於該組合物。如乳糖,
葡萄糖,蔗糖,山梨醇,甘露醇,澱粉,聚乙二醇,明膠等。該製劑中還可加入潤滑劑,濕潤劑,矯味劑,懸浮劑,防腐劑等。該發明的組合物可使用該領域通常採用的任何方法製備,以達到對患者使用後,活性成分發揮最大藥效的目的。
此藥物及保健品組合物可經口服,靜脈注射,肌肉注射,經皮或皮下注射給藥,經直腸等各種途徑給藥。可單次或多次連續使用,而藥物組合物使用劑量則應根據病人的具體情況決定,一般應控制在0.001-1.0克紅花總黃色素/千克體重·天。
該發明採取水提,聚醯胺柱層析洗脫法,矽膠吸附法或大孔樹脂吸附法除雜質後製得一純度較高的紅花總黃色素,這些方法在紅花成分提取製備的過程中的套用尚未見報導。它們可有效地除去多種雜質,明顯提高紅花總黃色素的純度,三種方法製備所得的紅花總黃色素的薄層圖譜均可見6-8個螢光斑點,而水提醇沉法所得的粗品在同樣條件下薄層螢光圖譜則為一拖尾嚴重的色帶,其上僅見2-3個輪廓模糊的斑點(見附圖),提示該發明的紅花總黃色素純度較粗品為高。且此法操作簡便,易於掌握,可作為紅花總黃色素製備及紅花水溶性成分檢測的初步淨化方法。據報導紅花黃色素具抗凝,促進纖溶,抗血栓形成,改善微循環等心血管藥理作用,實驗結果表明,該發明製得的紅花總黃色素具清除自由基,抗血小板激活因子,抑制血小板聚集,抗血栓形成,抗心肌缺血等作用,因此它可用於諸多血液循環障礙疾病的治療及預防,特別可用於腦血栓,腦缺血及心絞痛,心肌梗塞等具血栓形成及缺血性疾患的治療及預防。
該發明製得的紅花總黃色素(簡稱黃素)具下述藥效(下述實驗中所用黃素均為實施例4方法製備):
(1)黃素抑制血小板激活因子誘發的血小板聚集的作用
紐西蘭家兔,體重3-4千克,雌雄不限。Chronolog型血小板聚集儀,血小板激活因子(PAF)為Sigma公司產品,其他試劑均為國產分析純。取家兔耳正中動脈血10毫升(ACD:全血=1:6抗凝),500轉/分離心5分鐘,得富血小板血漿,2000轉/分離心5分鐘得血小板,以pH6.5的無鈣台氏液洗滌兩次,每次洗後2000轉/分離心5分鐘,棄上清,加pH7.4含0.25%牛血清白蛋白50毫摩爾/升Tris台氏液(TTBSA)調整血小板濃度至2×10/毫升,即為家兔洗滌血小板懸液(WRP)。取0.18毫升WRP,37度(該文所提及的溫標均為攝氏溫標)預熱後加入0.01毫升紅花總黃色素溶液,加0.01毫升血小板激活因子後以比濁法記錄血小板聚集曲線。空白對照管以蒸餾水代替黃素溶液。以黃素管血小板聚集率與空白管血小板聚集率比較,計算血小板聚集抑制率衡量其藥效。
結果表明,黃素抑制血小板激活因子誘發的家兔洗滌血小板聚集具明顯的量效關係。其它實施例方法製得的黃素依該法實驗所得數據與上述結果趨勢相同。
(2)黃素抑制血小板激活因子誘發的血小板釋放5-羥色胺(5-TH)的作用
以上法製得的WRP,取0.8毫升WRP,加入黃素溶液,37℃預熱2分鐘後加10微升血小板激活因子37℃反應4分鐘2000轉/分離心10分鐘,取上清液0.3毫升加TTBSA0.7毫升,再加0.3毫升100%三氯醋酸3500轉/分離心20分鐘,取0.5毫升上清液,加2毫升0.05%鄰苯二甲醛/HCl溶液,100℃水浴加熱10分鐘,水冷後加2毫升氯仿混勻後3500轉/分離心20分鐘,取上清1毫升測定5-TH螢光(Ex360納米,Em475納米)。陰性對照管以蒸餾水代替黃素溶液,以同濃度黃素TTBSA稀釋液代替WRP管為試劑空白。各反應管測定值均扣除試劑空白值測得5-TH螢光值F(Ex360納米,Em475納米)。
結果表明,黃素抑制血小板激活因子導致的5-TH釋放具明顯的量效關係。其它實施例方法製得的黃素依該法實驗所得數據與上述結果趨勢相同。
(3)黃素抑制血小板激活因子誘發的小鼠毛細血管通透性增加的作用
昆明種小鼠,雌雄不限,體重20-40克,隨機分組,小鼠腹腔注射黃素溶液後30分鐘,尾靜脈注射3%依文斯藍生理鹽水溶液2毫升/千克,尾靜脈注射後30分鐘於小鼠一側後腿股四頭肌注射PAF0.25%牛血清白蛋白生理鹽水溶液以造成局部炎症反應,於同一動物另一側後腿股四頭肌注射同體積生理鹽水,注射後30分鐘處死動物,分別取兩後腿肌肉剪碎,每隻後腿肌肉碎塊中加入2毫升甲醯胺,56℃提取24小時,3000轉/分離心20分鐘後取上清液,於620納米以每隻動物生理鹽水側後腿提取液為空白,測定對側後腿提取液吸光度,以此數據衡量小鼠毛細血管通透性的改變。無損傷空白對照組以生理鹽水代替PAF,生理鹽水代替黃素溶液為陰性空白。
| | | | | |
| | | | | |
| | | | | |
| | | | | |
| | | | | |
與空白組對照比較▲▲P<0.01;與PAF組對照比較*P<0.05 |
上述結果表明,黃素腹腔注射,可明顯抑制PAF致小鼠局部毛細血管通透性增加的作用具明顯的量效關係。其它實施例方法製得的黃素依該法實驗所得數據與上述結果趨勢相同。
(4)黃素清除自由基作用
以鄰二氮菲鐵氧化法檢測黃素清除羥自由基的作用,反應體系中含鄰二氮菲0.75毫摩爾/升,FeSO40.75摩爾/升,150毫摩爾/升pH7.4磷酸鹽緩衝液,H2O20.01%,加黃素後及其他試劑加H2O2,37℃保溫60分鐘後,測A536納米。以蒸餾水為陰性對照,未損傷管不加H2O2及抗氧化藥。以同濃度黃素稀釋液為比色空白,羥自由基清除率計d算法:d=[(A536加藥-A536損傷)/(A536未損傷-A536損傷)]×100%。
結果表明,黃素清除羥自由基的作用具明顯的量效關係。其它實施例方法製得的黃素依該法實驗所得數據與上述結果趨勢相同。
(5)黃素小鼠血栓形成的作用
雄性
昆明小鼠,體重18-22克,按體重均衡隨機分為五組,即正常對照組,阿司匹林組,黃素低,中,高劑量組。實驗前禁食12小時,灌胃給藥後30分鐘將小鼠依次放置於固定器中,使其尾部垂直,在距尾尖1.5毫米處剪斷後立即開始計時並迅速將其尾尖浸入37℃生理鹽水液面下1.5厘米處,記錄出血終止時間。
| | |
| | |
| | |
| | |
| | |
| | |
與生理鹽水組比較*P<0.05,**P<0.01,***P<0.001 |
結果表明該發明製得的黃素抑制小鼠血栓形成的作用具明顯的量效關係。其它實施例方法製得的黃素依該法實驗所得數據與上述結果趨勢相同。
(6)黃素抑制ADP誘發血小板聚集的作用
紐西蘭家兔,體重3-4千克,雌雄不限。儀器:Chronolog型血小板聚集儀,ADP為BM公司產品,其他試劑均為國產分析純。取家兔耳正中動脈血(3.8%枸櫞酸鈉:全血=1:9抗凝),500轉/分離心5分鐘,得富血小板血漿(PRP),下層液3000轉/分離心10分鐘得貧血小板血漿(PPP),以PPP調整PRP血小板濃度為2×10/毫升,取0.165毫升PRP,37度(該文所提及的溫標均為攝氏溫標)預熱後加入0.03毫升黃素溶液,加0.005毫升1克/升ADP後以比濁法記錄血小板聚集曲線。空白對照管以蒸餾水代替黃素溶液。以黃素管血小板聚集率與空白管血小板聚集率比較,計算血小板聚集抑制率。
結果表明該發明製得的黃素抑制ADP誘發的家兔血小板聚集具明顯的量效關係。其它實施例方法製得的黃素依該法實驗所得數據與上述結果趨勢相同。
(7)黃素抑制垂體後葉素誘發的大鼠心肌缺血的作用
雄性wistar大鼠,體重180-220克,實驗前依下法篩選動物:大鼠腹腔注射烏拉坦1-1.2克/千克麻醉,靜注垂體後葉素0.5或1.0u/千克,選擇T波上升0.1毫伏以上或下降超過50%的敏感動物隨機分為三組,即生理鹽水組,硝酸甘油組和紅花總黃色素組,4-6小時後進行藥效學實驗。抗心肌缺血藥物或生理鹽水腹腔注射後30分鐘靜脈注射垂體後葉素(各實驗組每組15隻大鼠中靜注0.75u/千克者均為7隻,靜注1.0u/千克者均為8隻),靜脈注射垂體後葉素前及靜注後5,10,15,20,30,45s,1,2,3,5,10,15,20分鐘記錄第II導聯心電圖,以靜注垂體後葉素後較注射前T波上升1毫伏以上或下降超過50%為藥物抗心肌缺血作用無效,T波上升不足1毫伏或下降不足50%為藥物作用有效。
結果表明該發明製得的黃素具抑制垂體後葉素誘發的大鼠心肌缺血的作用。其它實施例方法製得的黃素依該法實驗所得數據與上述結果趨勢相同。
(8)黃素抑制異丙腎上腺素誘發的大鼠心肌缺血的作用
雄性wistar大鼠,體重240-260克,隨機分為兩組即生理鹽水組和紅花總黃色素組,腹腔注射烏拉坦1克/千克麻醉,紅花總黃色素或生理鹽水腹腔注射30分鐘後腹腔注射異丙腎上腺素0.05毫克/千克,首次給紅花總黃色素或生理鹽水後12小時及24小時同樣方式各給紅花總黃色素或生理鹽水一次。首次腹注異丙腎24小時後再同法注射同劑量異丙腎上腺素,記錄初次注射異丙腎前與末次注射異丙腎後3分鐘第II導聯心電圖。選取心電圖中五個J點計算J/R值,取平均值作為該點數據,以每隻動物首次給異丙腎前及末次給異丙腎後J/R值進行自身對照,計算首次給異丙腎前及末次給異丙腎後J/R值之差的絕對值,以t檢驗法比較。給異丙腎前後J/R值的變化,以變化顯著者為心肌缺血明顯,變化不顯著者為缺血被抑制。
結果表明,紅花總黃色素腹腔注射可明顯抑制異丙腎誘發的大鼠心肌缺血。其它實施例方法製得的黃素依該法實驗所得數據與上述結果趨勢相同。
該發明製得的紅花總黃色素(簡稱該發明黃素)與市售水提醇沉法製得的紅花黃色素(簡稱市售黃素)的比較:
(1)該發明黃素與市售黃素抑制血小板激活因子誘發的
血小板聚集作用的比較
依該說明書前述“黃素抑制血小板激活因子誘發的血小板聚集的作用”方法,以同一動物血製備WRP於同一次試驗比較兩種黃素作用,結果如下:
上述結果表明,該發明製得的紅花總黃色素藥效明顯高於市售黃素。
(2)該發明黃素急性毒性實驗
1)灌胃給藥實驗
取昆明小鼠20隻,雌雄各半,小鼠體重18-22克,給藥後觀察動物情況,連續觀察七天,記錄死亡動物只數。灌胃給藥組結果:
結果表明,該發明黃素灌胃劑量達10克/千克時,小鼠無一死亡。
2)腹腔注射實驗:取昆明小鼠80隻,隨機分為四組,每組20隻,雌雄各半,小鼠體重18-22克,給藥後觀察動物情況,連續觀察七天,以各組死亡動物率計算半數致死量(LD50)。
計算得該發明黃素腹腔注射LD50=7.54±0.24克/千克。
據文獻報導,市售黃素腹腔注射LD50=5.49克/千克(95%可信限:5.11-5.59克/千克),灌胃給藥LD50=5.53克/千克(95%可信限:5.39-5.69克/千克),[參見黃正良等:紅花黃色素的毒理研究,甘肅醫藥,1983,(4):22-24]因此上述結果表明,該發明製得的紅花總黃色素毒性明顯低於市售黃素。
(3)該發明黃素與市售黃素薄層層析結果的比較
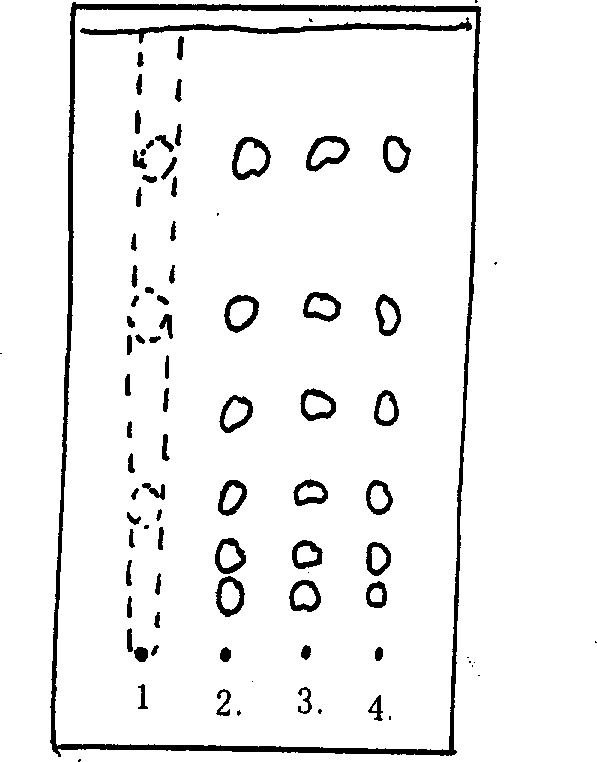
見附圖,層析結果表明,該發明製得的紅花總黃色素純度較市售黃素明顯提高。
附圖說明
圖中:1.市售紅花總黃色素;2.《紅花總黃色素及其製備方法和套用》聚醯胺層析法製備的紅花總黃色素;3.該發明矽膠吸附法製備的紅花總黃色;4.該發明大孔樹脂吸附法製備的紅花總黃色素。
權利要求
1.一種紅花總黃色素,該紅花總黃色素可用下述方法製備獲得(1)以紅花為原料,加入適量的極性溶劑浸提,濾除藥渣合併浸提液,濃縮得到提取濃縮液;(2)把上述步驟得到的提取濃縮液進行柱層析,以極性洗脫液洗脫除去雜質後再以另一極性洗脫液洗脫紅花總黃色素;或以層析擔體對提取濃縮液進行吸附,以極性洗脫液直接洗下紅花總黃色素並使雜質吸附於層析擔體上;(3)收集去除雜質的紅花總黃色素洗脫液,回收溶劑,濃縮乾燥即得。
2.一種紅花總黃色素的製備方法,該方法包括下述順序的步驟(1)以紅花為原料,加入適量的極性溶劑浸提,濾除藥渣合併浸提液,濃縮得到提取濃縮液;(2)把上述步驟得到的提取濃縮液進行柱層析,以極性洗脫液洗脫除去雜質後再以另一洗脫液洗脫紅花總黃色素;或以層析擔體對提取濃縮液進行吸附,以極性洗脫液直接洗下紅花總黃色素並使雜質吸附於層析擔體上;(3)收集去除雜質的紅花總黃色素洗脫液,回收溶劑,濃縮乾燥即得。
3.權利要求2的製備方法,其特徵在於所述的提取是以極性溶劑提取2-4次,每次1-3天,提取用適量極性溶劑用量為紅花生藥重量的5-50倍。
4.權利要求2的製備方法,其特徵在於提取所用的極性溶劑為水或乙醇,甲醇及丙醇水溶液。
5.權利要求2的製備方法,其特徵在於所述的用於除雜質的紅花提取濃縮液濃度相當於0.1-10克生藥/毫升。
6.權利要求2的製備方法,其特徵在於以聚醯胺柱層析法去除紅花提取濃縮液中的雜質,且其紅花提取濃縮液與所用聚醯胺粉之比按體積計為1:1-30。
7.權利要求2的製備方法,其特徵在於以矽膠吸附紅花提取濃縮液中的雜質,且其紅花提取濃縮液與所用矽膠粉之比按體積計為1:1-30。
8.權利要求2的製備方法,其特徵在於以大孔樹脂吸附紅花提取濃縮液中有效組分,去除雜質,且其紅花提取濃縮液與所用之大孔樹脂比按體積計為1:1-30。
9.權利要求2的製備方法,其特徵在於所述的極性洗脫液為水或者濃度為20-100重量百分比的乙醇,甲醇或丙醇水溶液。
10.權利要求2的製備方法,其特徵在於所述的極性洗脫液為水或者濃度為40-95重量百分比的乙醇,甲醇或丙醇水溶液。
11.一種治療心腦血管疾病的藥物及保健品,其特徵在於含有治療或預防心腦血管疾病等血液循環障礙性疾病有效量的權利要求1的紅花總黃色素和可藥用的載體。
12.權利要求11的藥物及保健品,其特徵在於可以製成膠囊,針劑,片劑,栓劑和口服液等可使用的製劑。
13.權利要求1的紅花總黃色素在製備預防及治療涉及組織缺血特別是心肌缺血及腦缺血,血栓形成及血小板激活因子與自由基所致損傷疾病的藥物及保健品中的套用。
實施方式
實施例1
聚醯胺層析法製備紅花總黃色素:取100克紅花生藥藥粉,每次加0.5千克水室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次水提液,過濾除去藥渣,50-90度減壓濃縮至200毫升即得紅花水提濃縮液,取上述紅花水提濃縮液,上柱床體積為3000毫升的聚醯胺柱,以蒸餾水洗脫至洗脫液Molish反應及茚三酮反應陰性,以40重量百分比乙醇洗脫聚醯胺柱上吸附的紅花黃色素至洗脫液無色即可。上述洗脫液回收乙醇,50-90度減壓濃縮,乾燥即得紅花總黃色素。
實施例2
聚醯胺層析法製備紅花總黃色素:取100克紅花生藥藥粉,每次加0.5千克20重量百分比甲醇室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次提取液,過濾除去藥渣,回收溶劑,50-90度減壓濃縮至200毫升即得紅花水提濃縮液。取上述紅花水提濃縮液,上柱床體積為3000毫升的聚醯胺柱,以蒸餾水洗脫至洗脫液Molish反應及茚三酮反應陰性,以95重量百分比乙醇洗脫聚醯胺柱上吸附的紅花黃色素至洗脫液無色即可。上述洗脫液回收乙醇,50-90度減壓濃縮,乾燥即得紅花總黃色素。
實施例3
聚醯胺層析法製備紅花總黃色素:取100克紅花生藥藥粉,每次加3000毫升20重量百分比乙醇室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次提取液,過濾除去藥渣,回收乙醇,50-90度減壓濃縮至40毫升即得紅花提取濃縮液。取上述紅花提取濃縮液,上柱床體積為1200毫升的
聚醯胺柱,以
蒸餾水洗脫至洗脫液Molish反應及茚三酮反應陰性,以75重量百分比乙醇洗脫聚醯胺柱上吸附的紅花黃色素至洗脫液無色即可。上述洗脫液回收乙醇,50-90度減壓濃縮,乾燥即得紅花總黃色素。
實施例4
矽膠吸附法製備紅花總黃色素:取100克紅花生藥藥粉,每次加0.5千克水室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次水提液,過濾除去藥渣,50-90度減壓濃縮至200毫升即得紅花水提濃縮液。取上述紅花提取濃縮液與1000克柱層析用矽膠粉拌勻,60度減壓烘乾後以2000毫升40重量百分比乙醇洗脫上述矽膠即得紅花總黃色素洗脫液。取紅花總黃色素洗脫液,回收乙醇,50-90度減壓濃縮蒸乾後即得紅花總黃色素。
實施例5
矽膠吸附法製備紅花總黃色素:取100克紅花生藥藥粉,每次加0.5千克20重量百分比甲醇室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次提取液,過濾除去藥渣,回收溶劑,50-90度減壓濃縮至200毫升即得紅花水提濃縮液,取上述紅花提取濃縮液與1000克柱層析用矽膠粉拌勻,60度減壓烘T後以2000毫升95重量百分比乙醇洗脫上述矽膠即得紅花總黃色素洗脫液。取紅花總黃色素洗脫液,回收乙醇,50-90度減壓濃縮蒸乾後即得紅花總黃色素。
實施例6
矽膠吸附法製備紅花總黃色素:取100克紅花生藥藥粉,每次加3000毫升20重量百分比乙醇室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次提取液,過濾除去藥渣,回收乙醇,50-90度減壓濃縮至40毫升即得紅花提取濃縮液。取上述紅花提取濃縮液與1200克柱層析用矽膠粉拌勻,60度減壓烘乾後以2000毫升75重量百分比乙醇洗脫上述矽膠即得紅花總黃色素洗脫液。取紅花總黃色素洗脫液,回收乙醇,50-90度減壓濃縮蒸乾後即得紅花總黃色素。
實施例7
大孔樹脂吸附法製備紅花總黃色素:取100克紅花生藥藥粉,每次加0.5千克水室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次水提液,過濾除去藥渣,50-90度減壓濃縮至200毫升即得紅花水提濃縮液。取上述紅花水提濃縮液,與體積為3000毫升的大孔樹脂拌勻,60度減壓烘乾後,以蒸餾水反覆洗脫至洗脫液Molish反應及茚三酮反應陰性,以40重量百分比乙醇洗脫大孔樹脂上吸附的紅花黃色素至洗脫液無色即可。上述洗脫液回收乙醇,50-90度減壓濃縮,乾燥即得紅花總黃色素。
實施例8
大孔樹脂吸附法製備紅花總黃色素:取100克紅花生藥藥粉,每次加0.5千克20重量百分比甲醇室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次提取液,過濾除去藥渣,回收溶劑,50-90度減壓濃縮至200毫升即得紅花水提濃縮液。取上述紅花水提濃縮液,與體積為3000毫升的大孔樹脂拌勻,60度減壓烘乾後,以蒸餾水反覆洗脫至洗脫液Molish反應及茚三酮反應陰性,以95重量百分比乙醇洗脫大孔樹脂上吸附的紅花黃色素至洗脫液無色即可。上述洗脫液回收乙醇,50-90度減壓濃縮,乾燥即得紅花總黃色素。
實施例9
大孔樹脂吸附法製備紅花總黃色素:取100克紅花生藥藥粉,每次加3000毫升20重量百分比乙醇室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次提取液,過濾除去藥渣,回收乙醇,50-90度減壓濃縮至40毫升即得紅花提取濃縮液。取上述紅花提取濃縮液,與體積為1200毫升的大孔樹脂拌勻,60度減壓烘乾後,以蒸餾水反覆洗脫至洗脫液Molish反應及茚三酮反應陰性,以75重量百分比乙醇洗脫大孔樹脂上吸附的紅花黃色素至洗脫液無色即可。上述洗脫液回收乙醇,50-90度減壓濃縮,乾燥即得紅花總黃色素。
實施例10
大孔樹脂吸附法製備紅花總黃色素:取100克紅花生藥藥粉,每次加0.5千克水室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次水提液,過濾除去藥渣,50-90度減壓濃縮至200毫升即得紅花水提濃縮液。取上述紅花水提濃縮液,上柱床體積為3000毫升的大孔樹脂柱,以蒸餾水洗脫至洗脫液Molish反應及茚三酮反應陰性,以40重量百分比乙醇洗脫大孔樹脂柱上吸附的紅花黃色素至洗脫液無色即可。上述洗脫液回收乙醇,50-90度減壓濃縮,乾燥即得紅花總黃色素。
實施例11
大孔樹脂吸附法製備紅花總黃色素:取100克紅花生藥藥粉,每次加0.5千克20重量百分比甲醇室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次提取液,過濾除去藥渣,回收溶劑,50-90度減壓濃縮至200毫升即得紅花水提濃縮液。取上述紅花水提濃縮液,上柱床體積為3000毫升的大孔樹脂柱,以蒸餾水洗脫至洗脫液Molish反應及茚三酮反應陰性,以95重量百分比乙醇洗脫大孔樹脂柱上吸附的紅花黃色素至洗脫液無色即可。上述洗脫液回收乙醇,50-90度減壓濃縮,乾燥即得紅花總黃色素。
實施例12
大孔樹脂吸附法製備紅花總黃色素:取100克紅花生藥藥粉,每次加3000毫升20重量百分比乙醇室溫浸48小時,其間不時攪拌,共提取兩次,合併兩次提取液,過濾除去藥渣,回收乙醇,50-90度減壓濃縮至40毫升即得紅花提取濃縮液。取上述紅花提取濃縮液,上柱床體積為1200毫升的大孔樹脂柱,以蒸餾水洗脫至洗脫液Molish反應及茚三酮反應陰性,以75重量百分比乙醇洗脫大孔樹脂柱上吸附的紅花黃色素至洗脫液無色即可。上述洗脫液回收乙醇,50-90度減壓濃縮,乾燥即得紅花總黃色素。
製劑實施例1
紅花總黃色素口服硬膠囊劑:紅花總黃色素100克、乾澱粉100克,上述組分混合後裝入1000個硬膠囊,即得紅花總黃色素口服硬膠囊劑
製劑實施例2
紅花總黃色素注射劑:紅花總黃色素50克、注射用水適量、全量1000毫升,取50克紅花總黃色素以適量注射用水溶解後加至1000毫升按常規方法經灌裝,封口等步驟製得紅花總黃色素注射劑。
製劑實施例3
紅花總黃色素栓劑:紅花總黃色素500克、半合成脂肪酸甘油脂適量、製成1000粒,取半合成脂肪酸甘油脂加熱使融,適當降溫後加入500克紅花黃色素混勻,制栓,冷卻即得紅花總黃色素栓劑。
製劑實施例4
紅花總黃色素口服液:紅花總黃色素0.5克、蒸餾水10毫升,紅花總黃色素溶解後按常規方法經灌裝,封口等步驟生產即得紅花總黃色素口服液。
製劑實施例5
紅花總黃色素片劑:紅花總黃色素500克、硬脂酸鎂5克、澱粉20克,製成1000片。紅花總黃色素,硬脂酸鎂與澱粉混勻後按常規方法經壓片,包衣,裝瓶等工藝即得紅花總黃色素片劑。
榮譽表彰
2014年11月6日,《紅花總黃色素及其製備方法和套用》獲得第十六屆中國專利優秀獎。