基本介紹
- 中文名:稀土氫氧化物
- 定義:把氨水或鹼加入稀鹽溶液,生成不穩定的膠狀沉澱
- 特性:膠狀沉澱、受熱不穩定
合成及物理性質
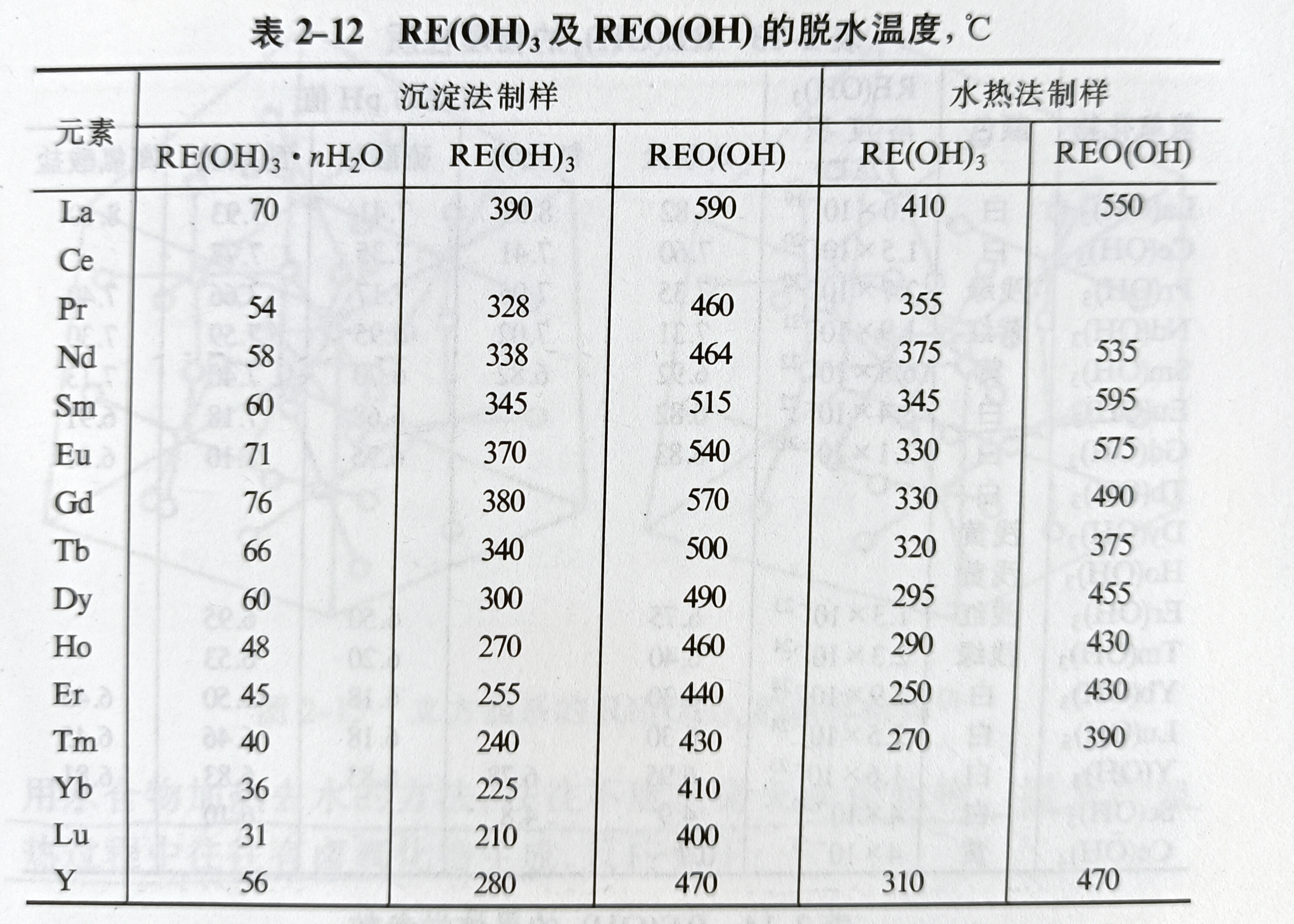
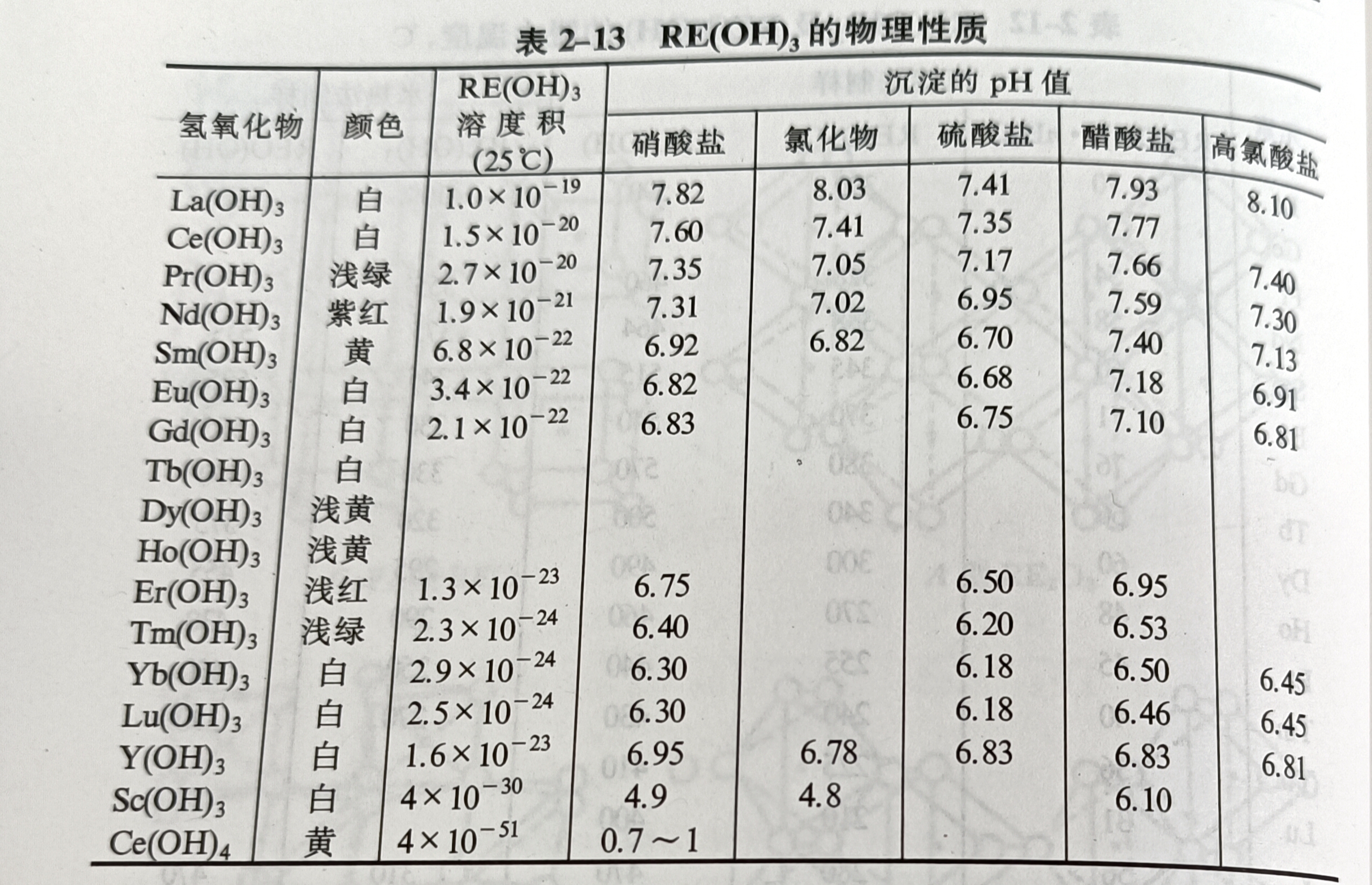
氫氧化物的結構
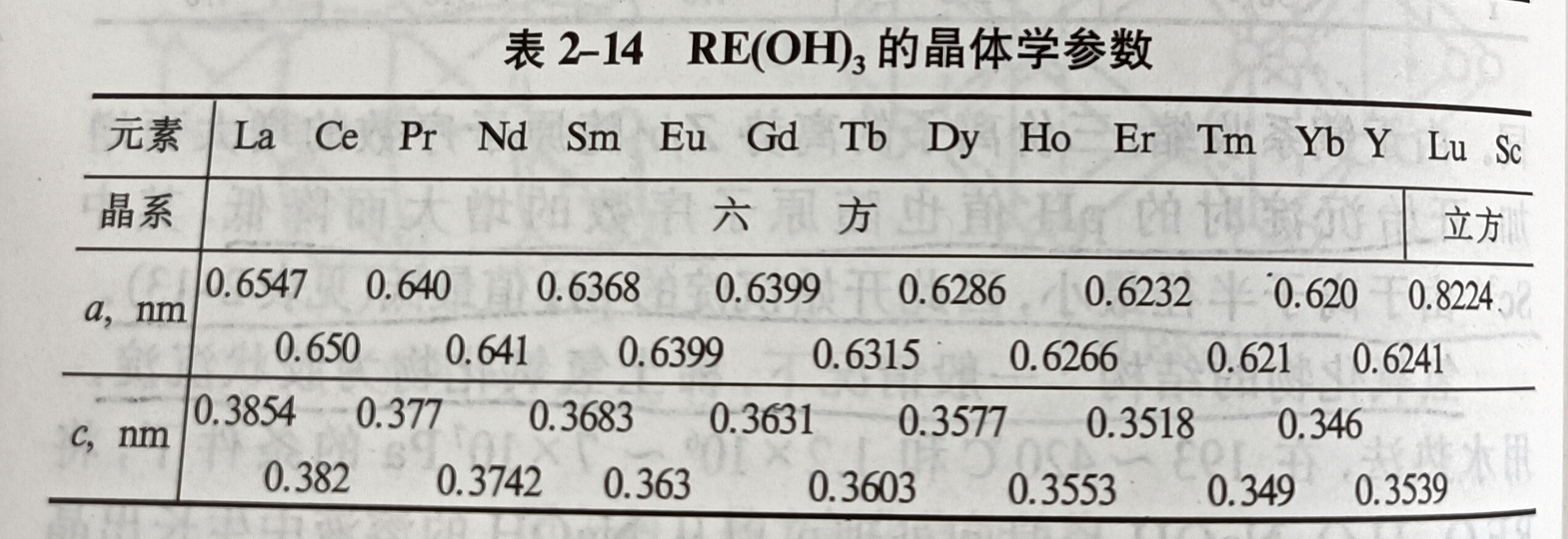
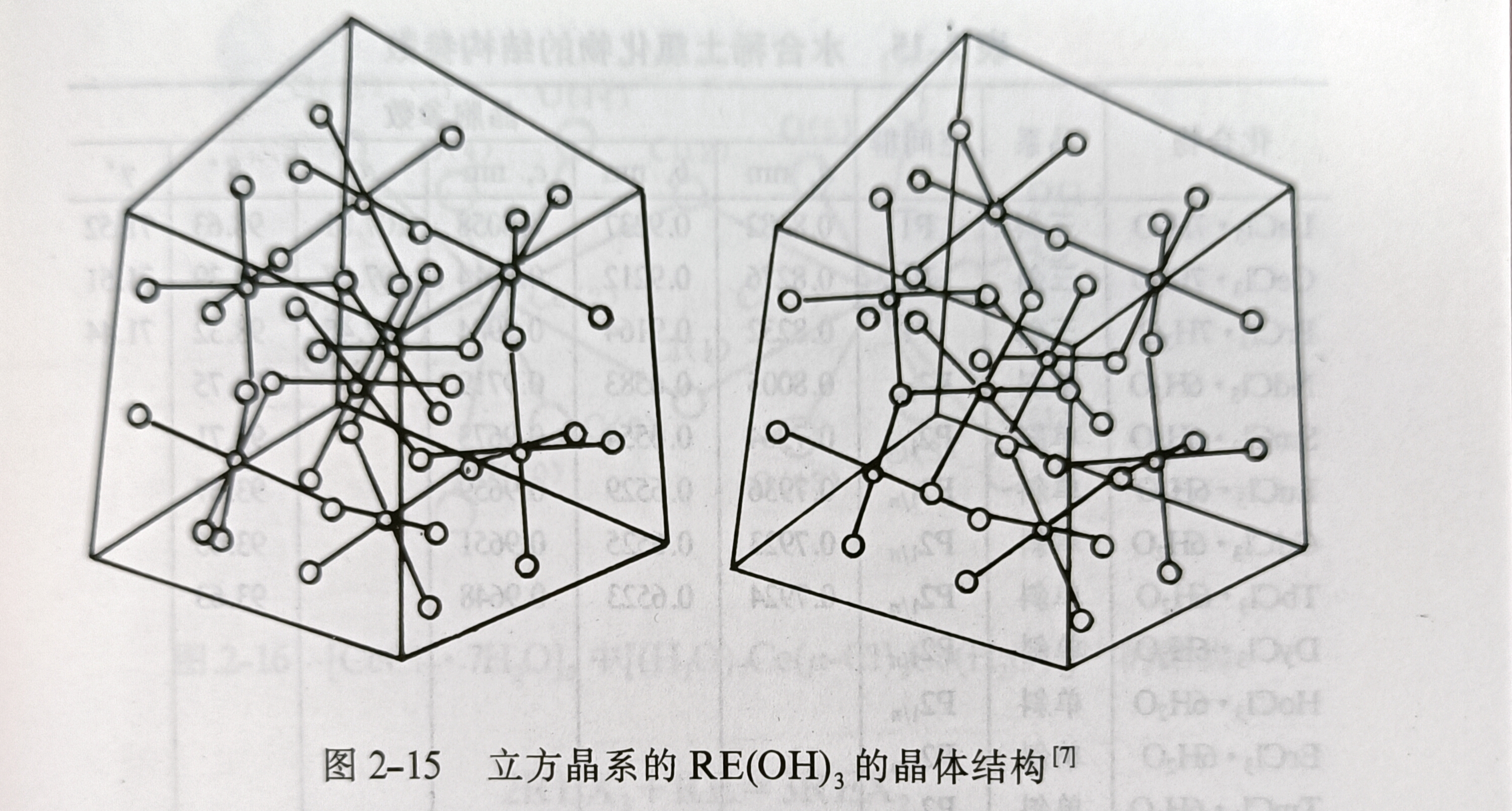




往稀土鹽溶液中加入氨水或其他鹼,可以產生稀土的氫氧化物。稀土氫氧化物具有熱不穩定性。受鑭系收縮的影響,不同稀土元素開始沉澱的最低pH值不同。1合成及物理性質往稀土鹽溶液中加入氨水或其他鹼,可以產生稀土的氫氧化物,它是一種...
《稀土氫氧化物二維及三維結構調控及其光致發光性能》是依託北京師範大學,由楊曉晶擔任項目負責人的面上項目。項目摘要 作為發光材料及其前驅體的稀土氫氧化物的合成、結構、發光性能的研究方興未艾。由於稀土金屬離子通常採取高配位數與羥基/H2O/氧離子結合,因此與其他金屬氫氧化物(如層狀雙金屬氫氧化物,LDHs)相比...
主要指標 : 產品中w(REO)=99% ,w(CeO2)=99%; 稀土回收率約95%。該產品適用於高速拋光。這種高鈰拋光粉最早代替了古典拋光的氧化鐵粉(紅粉)。(2)中鈰系稀土拋光粉的製備 用混合稀土氫氧化物(w(REO)=65% ,w(CeO2)≥48%) 為原料,以化學方法預處理得稀土鹽溶液,加入中間體( 沉澱劑) 使轉化成...
、氫氧化鈷 、氫氧化金 ,還有稀土金屬氫氧化物。兩性氫氧化物 也有一些金屬元素的氫氧化物呈兩性,它們既能與酸反應生成鹽和水,又能與鹼反應生成相應的鹽,這樣的氫氧化物稱兩性氫氧化物,如氫氧化鋁 ,氫氧化銅 、氫氧化鈹 等。化學性質 特性 氫氧化物具有鹼的特性。能與酸生成鹽和水。可溶性氫氧化物與可溶...
中強鹼 鹼性介於強鹼與弱鹼之間的鹼叫做中強鹼。所謂“中強”通常都是指電離平衡常數在0.001到0.01數量級的酸鹼。實際上,中強鹼屬於弱鹼 常見的中強鹼有:氫氧化銀,氫氧化鎂,氫氧化鈣,氫氧化鎳,氫氧化錳,稀土元素的氫氧化物
優溶液 優溶液(selective solution)是2019年公布的冶金學名詞,出自《冶金學名詞》第二版。定義 稀土氫氧化物沉澱經水洗過濾後的鹼餅,用鹽酸優先溶解稀土,過濾後獲得的含混合稀土氯化物的溶液。出處 《冶金學名詞》第二版。
優溶渣 優溶渣(selective solution slag)是2019年公布的冶金學名詞,出自《冶金學名詞》第二版。定義 稀土氫氧化物沉澱經水洗過濾後的鹼餅,用鹽酸優先溶解稀土,濾出優溶液後的濾渣。渣中尚含有未溶解的精礦和釷、鐵等雜質。出處 《冶金學名詞》第二版。
3、隨著電解的進行,陰極液酸度降低,可能出現稀土氫氧化物沉澱,必須控制好陰極液酸度。在使用體系2時:1、還原率及電效率遜於體系1;2、陽極放出氯氣;3、陰極液不出現稀土氫氧化物沉澱;4、陽離子膜強度好、壽命長。在電解還原製備二價銪的工藝中,陽極液的鹽酸濃度為0.01-1.5摩爾/升,若陽極液為鹽酸和...
然後向溶液中加入氨水,使三價稀土呈氫氧化物定量沉澱析出,而Eu仍留在溶液中。過濾所得的濾液用過氧化氫或空氣將Eu氧化為Eu,Eu與溶液中存在過量的OH⁻生成氫氧化銪沉澱。製得的氫氧化銪中Eu₂O₃/RE₂O₃ 99.99%。與其他兩種提純方法相比,此法具有工藝簡單,產品質量穩定的優點,是氧化銪提純的主要...
鋅粉還原-鹼度法 鋅粉還原-鹼度法(zinc powder deoxidization-alkalinity method)是2019年公布的冶金學名詞。定義 經鋅粉還原得到的二價銪的溶液中, 加入氨水調節成鹼性,使三價稀土生成難溶的氫氧化物沉澱, 而與銪分離的方法。出處 《冶金學名詞》第二版。
