生物物理基礎,電阻抗斷層成像基本原理,EIT檢測技術,1.電極模組,2.交流恆流驅動模組,3.信號檢測模組,4.數據採集模組,5.驅動、測量模式設定模組,EIT硬體系統結構,1. 硬體系統主要結構,2.硬體系統主要特點,擴展閱讀,
生物物理基礎 生物組織由細胞和細胞間質共同組成,其中細胞間質為具電解液特性的組織液及懸浮理學於其中的大分子化合物構成,可等效為一定阻值的電阻。細胞膜為具有低的漏電特性的絕緣膜,是組織阻抗容性成分的主要貢獻者。細胞質與細胞間質相類似,表現為阻性。
對生物體來說,一方面由於細胞種類、排列的疏密、細胞間質及細胞膜通透性的不同,不同組織、甚至於同種組織的不同方向及狀態所表現出的阻抗特性都有可能不同;另一方面由於組織的生理或病理改變必然會影響到細胞膜的通透性、細胞間質的電解質濃度等的變化,從而影響到其阻抗特性。
電阻抗斷層成像基本原理 生物電阻抗斷層成像(Electrical Impedance Tomography,簡稱EIT)是以生物體內電阻抗分布的絕對值(靜態EIT)或阻抗的變化量(動態EIT)為成像對象的一種新型成像技術。目前,EIT常採用體表激勵、體表測量技術對成像區域的阻抗分布信息進行測量,通過體表電極注入安全、微弱的交變電流(電壓),並同步測量邊界上的電壓(電流),電極數目一般為8、16、32等,均勻放置體表一周,採用輪轉驅動電極和測量電極的方式,實現等效四電極阻抗測量,並獲得體表不同部位的一幀阻抗數據,利用圖象重構算法對阻抗數據進行重構,得到反映體內阻抗分布或變化的斷層圖像。
靜態成像(Static imaging)。靜態EIT以測量對象內部電阻(導)率的絕對分布為成像目標,通過對測量目標外加驅動電壓或電流測量其邊界電壓或電流,以估計目標內部電阻(導)率分布的絕對值。
靜態EIT技術需要目標表面形狀、電極結構和位置的準確信息,微小的誤差可能會導致重構結果的發散。因此,靜態EIT技術需要很高的測量精度和電極的精確定位,增加了對儀器的許多限制和要求,同時生物結構的各向異性和實際場的三維分布給靜態重構算法的收斂帶來了困難。由於這些條件的限制,靜態EIT技術還處於仿真和物理模型研究階段。
動態成像(Dynamic imaging)。動態EIT技術以測量對象內部的電阻(導)率分布的變化為求解目標,利用兩組測量數據的差值進行成像,去除了測量系統誤差,反映了兩次測量中阻抗分布的變化情況,相對於靜態成像,提高了系統對被測目標形狀、電極位置的魯棒性。因而成為目前能在臨床進行套用研究的EIT新技術,取得了初步的臨床效果。
總體上,EIT技術具有操作簡便、成像速度快、體表無創測量、儀器價格較低、檢查費用較低,對人體生理和病理改變引起的阻抗變化敏感的特點和優勢。
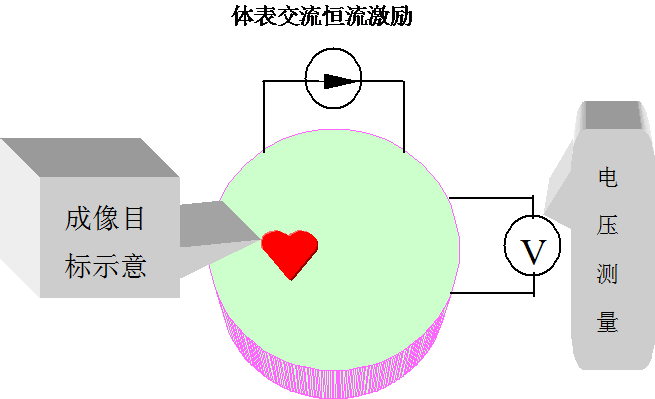
EIT檢測技術 EIT檢測技術的基本要求是按照套用需求,採用現代電子技術和計算機技術以一定的速度和精度,對成像部位的阻抗信息進行安全和有效檢測。目前,常用的是體表交流恆流激勵、體表電壓測量,通過解調技術獲取阻抗信息。圖1-1為EIT體表激勵和測量基本示意圖。
圖1-1 EIT體表激勵、測量示意圖
一個基本的EIT檢測系統包括電極模組、交流恆流驅動模組、信號放大和檢測模組、數據採集模組、驅動及測量模式設定模組、電源模組及計算機等,完成阻抗數據的採集、傳輸、存儲等功能,供阻抗成像算法調用。
1.電極模組 為了使用方便並較好的從體表獲取阻抗信息,目前EIT中常用8、16、32個體表電極,儘量均勻的配置在成像部位的一周;在用於三維成像中,電極數最多達到了960個。電極結構為單個電極或複合電極,均採用一對電極激勵、另外的一對電極測量的4電極法阻抗測量模式。電極材料一般為醫用電極材料,如用於頭部的鍍金、鍍銀杯狀電極,用於胸腹部的一次性自貼上心電電極、導電橡膠電極等。對電極的基本要求是能與皮膚穩定、良好接觸,對皮膚沒有腐蝕或損害,皮膚與電極接觸阻抗儘量小。
2.交流恆流驅動模組 為了安全,並部分消除電極皮膚接觸阻抗的影響,生物阻抗測量大部分採用基於歐姆定律的交流恆流激勵(I恆定)、測量體表電位差(V)的方法,通過解調間接獲得一對驅動電極與一對測量電極間的等效阻抗。產生一定頻率的交流信號,可以採用模擬正弦發生器或直接數字合成技術(DDS),恆流激勵輸出一般採用壓控電流源電路(VCCS),輸出電流小於5mA的恆流激勵信號,施加到一對驅動電極上。對恆流激勵模組的要求是輸出阻抗高、噪聲小、穩定性好、頻率回響好。
3.信號檢測模組 針對一對測量電極上的體表信號,完成高精度放大、動態範圍調整及阻抗信號解調等功能。信號放大通常採用高性能儀表放大器(IA),並滿足高輸入阻抗、高共模抑制比、低噪聲和寬頻的需求。
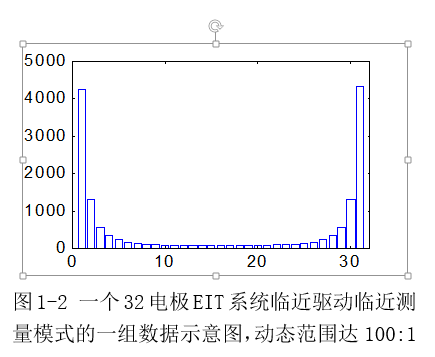
針對EIT中不同測量電極對之間的信號幅值變化較大的實際,在前置放大器之後一般設定程控增益放大器(PGA),調整信號的動態範圍,圖1所示為一個32電極EIT系統臨近驅動臨近測量模式的一組數據,最大值與最小值之比達100:1,因此要採用PGA對小信號提供更高的放大倍數,以降低小信號在A/D轉換時的量化誤差。
放大後的信號,可以採用模擬或數字解調技術,對被測信號中的阻抗實部、虛部信息(模值或相位)進行解調。常用的模擬解調技術或器件主要有均方值法(RMS)、整流濾波法、開關解調法、模擬乘法器和高速采保解調器等,數字解調就是對被測信號和參考信號進行高速、高精度多點同步採樣後,採用數值解調方法對被測信號序列和參考信號序列進行運算,求得被測信號的幅值和相對於參考信號的相位信息。
4.數據採集模組 主要完成模擬信號到數位訊號的轉換功能(A/D)。根據精度和速度的要求,A/D一般要有12位以上的解析度;若採用模擬解調技術,則A/D的採集速度較低,若採用數字解調技術,則為了提高解調精度,解調數據序列要足夠長,在單位周期時間內要求A/D能採集到足夠多的數據,採集速度較快才能滿足要求。
5.驅動、測量模式設定模組 選擇多電極中的一對作為恆流激勵電極、並選擇另外一對電極作為體表回響電壓的測量電極。一般選用電子開關,可程控選擇任意2個用於激勵、任意2個用於信號檢測,最常用的激勵方式是臨近(一對相鄰電極)激勵和對向(一對徑向的相對電極)激勵,最常用的測量方式是臨近(一對相鄰電極)測量。
無論採用何種激勵和測量模式,都必須按一定的組合方式和時序將激勵信號載入到一對驅動電極上,將一對測量電極上的信號或校準信號(定標信號)載入到信號檢測模組的輸入端,實現這一功能目前主要採用高速模擬開關(Analog Multiplexer)。要求模擬開關的導通電阻儘量小且一致,通道串擾小、頻率回響好、溫度特性好、切換速度快。
EIT硬體系統結構 1. 硬體系統主要結構 從整體結構上,EIT硬體系統分為串列激勵、串列測量的串列結構,串列激勵、並行測量或並行激勵、串列測量的半並行結構,以及並行激勵、並行測量的全並行結構。
串列結構的系統,只有單通道激勵源和單通道測量模組,在選擇不同電極對進行驅動和測量時,要用多路開關進行切換,因此影響了系統的總體測量速度,在成像速度較慢的系統中,可以採用串列結構的系統。其優點是結構簡單、費用低、維護方便。
並行結構的系統,有多通道的激勵源和測量模組。可以在同一時間向多對電極施加激勵,已獲得較優激勵模式;可以同時測量多對電極上的信號,大大提高測量速度。其不足是結構較複雜、費用高,需要綜合考慮通道一致性和穩定性,系統需要定期校準和定標。
半並行結構兼具串列和並行的優勢,可以獲得較高的速度和較好的性能。
2.硬體系統主要特點 儘管EIT硬體系統結構有串列、並行和串並混合型,採用的技術、選用的功能電路和器件各不相同,但高精度和/或高速度是其共同特點。
高精度。 在電EIT中要求高精度的原因,主要來自臨床需要。文獻報導,在一個心動周期中,肺部組織因血流改變導致的阻抗變化約為肺組織自身阻抗的3%,在體表電壓測量中,僅能測量到這種阻抗變化的5%,即肺部血流灌注引起的阻抗變化在體表能觀測到約0.15%的改變,因此胸部EIT中的測量系統要求能至少測量0.1%的變化。在腦部,因為顱骨高電阻率的存在,激勵電流中僅有少部分進入顱內,顱內阻抗變化信號經進一步衰減後才能從頭皮測到,因此腦EIT的硬體系統,要求其精度更高。仿真研究表明,在腦部EIT中,要能夠檢測到有臨床意義的顱內出血或缺血引起的阻抗變化,腦EIT的阻抗解析度要至少達到0.01%。由於電路自身噪聲、器件的非線性、系統內部串擾、來自外界的干擾及測量誤差在實際測量系統中都不同程度的、不可避免的存在,高精度EIT系統是阻抗成像的基礎和硬體支撐。
高速度。 心臟的收縮是體內器官最快的活動之一,在胸部EIT中要動態顯示一個完整的心動周期中血流灌注引起的阻抗變化,則成像速度不得低於20幀/秒,考慮到人眼視覺上對動態圖像無閃爍感的最低要求,胸部EIT圖像動態顯示速度理論上應不低於25幀/秒,即硬體系統採集一組數據的時間加上算法使用這組數據重構一幅圖像並動態顯示的時間應小於40ms。因此,胸部EIT硬體系統應當具有高速度的特性,這是高速成像的前提,在此前提下,還應當有高精度的特性,才能從胸部體表有效檢測到血流灌注引起的阻抗變化。
一個典型的阻抗成像檢測系統的指標主要有:電極數目16個,激勵頻率50KHz,激勵電流從0.1mA~2.5mA可程控設定,恆流源輸出阻抗大於500 KΩ;信號檢測模組輸入阻抗大於2MΩ,50KHz CMRR大於70dB,R.T.I.小於100μV,測量精度(Sd/Mean)優於0.1%,測量速度每秒15幀數據。
EIT技術因其無創、快速、費用低、操作簡便的優勢,在腦部、胸部和腹部重要臟器的生理、病理功能變化的快速、動態監測方面,展示了很好的套用前景。
擴展閱讀 (1) 董秀珍。生物電阻抗成像研究的現狀與挑戰[J]. 中國生物醫學工程學報,2008,05:641-643+649
(2) 徐桂芝,楊碩,李穎,顏威利。電阻抗斷層成像技術綜述[J]. 河北工業大學學 報,2004,02:35-40.
(3) Brown BH. Cardiac and respiratory related electrical impedance changes in the human thorax. IEEE Trans Biomed Eng.,1994; 41(8):729-733
(4) Robert WM, Smith HJ. A real-time electrical impedance tomography system for clinical use-design and preliminary results. IEEE Trans Biomed Eng., 1995;42(2) 133-140
(5) 史學濤,董秀珍, 帥萬鈞,尤富生,付峰,劉銳崗。適用於腦部電阻抗斷層成像的單源驅動電流模式, 第四軍醫大學學報, 2006, 27(3): 279-282.
(6) 尤富生,董秀珍,史學濤,付峰,劉銳崗,李江。電阻抗斷層成像中臨近和對向驅動模式的研究[J].第四軍醫大學學報,2004,01:88-91.
(7) 尤富生,董秀珍,史學濤,付峰,劉銳崗,秦明新,湯孟興,李江。生物電阻抗模擬解調技術的研究[J].北京生物醫學工程,2004,01:21-23+16。
(8) 尤富生,董秀珍,史學濤,付峰,劉銳崗。多頻生物電阻抗高精度模擬解調技術的研究[J].醫療衛生裝備,2004,07:10-11.
(9) 尤富生,董秀珍,秦明新,史學濤,付峰,劉銳崗,湯孟興,李江,吳曉明。電阻抗斷層成像中驅動和測量模式程控系統的設計[J].第四軍醫大學學報,2001,03:273-275.
(10)尤富生,董秀珍,秦明新,史學濤,湯孟興,劉銳崗。一個32電極電阻抗斷層成像硬體系統[J].第四軍醫大學學報,1998,S1:7-9.
(11)尤富生.電阻抗斷層成像硬體系統[J]。國外醫學-生物醫學工程分冊,1998,03:6-11.
(12)顏威利,徐桂芝,等著。生物醫學電磁場數值分析[B]。第八章.電阻抗成像裝置與系統測試。2006.3,機械工業出版社。