基本介紹
- 中文名:環合
- 外文名:cyclization
- 別稱:閉環;成環縮合
- 特點:脫掉小分子,易成五元或六元環等
- 分類:分子間環合和分子內環合
- 套用:有機合成
簡介
環合類型
 分子內環合
分子內環合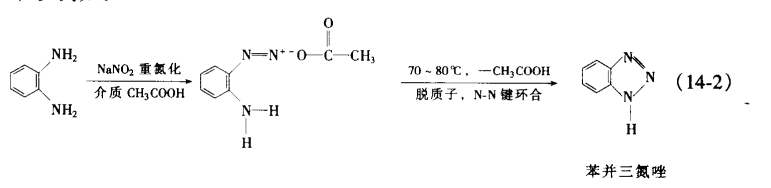 分子間環合
分子間環合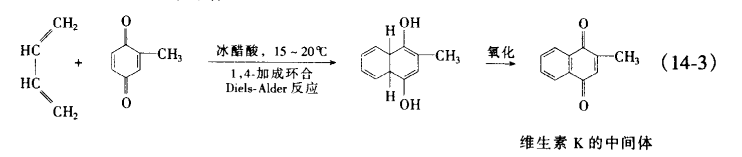 協同環合
協同環合環合特點
環合反應
形成六元碳環的環合反應
形成含一個氧原子的雜環的環合反應
形成含一個氮原子的雜環的環合反應
具體套用
 環合反應歷程
環合反應歷程 分子內環合
分子內環合 分子間環合
分子間環合 協同環合
協同環合 環合反應歷程
環合反應歷程形成新的碳環或雜環的反應過程,也稱閉環縮合或成環縮合。環合一般形成芳香族的六元碳環以及五元和六元雜環,因為這些環比較穩定,而且容易生成。大多數環合過程是...
簡介左氧氟環合酯是合成左氧氟沙星藥物的一個主要原料 中文名稱 :左氧氟環合酯 化學名為:(S)-(-)-9-氟-2,3-二氫-3-甲基-10-(4-甲基-1-哌嗪基)-...
基本信息 有機環合反應原理與套用 作者:孫昌俊、劉少傑、李文保 主編 出版日期:2016年1月 書號:978-7-122-24880-0 開本:16K 787×1092 1/16 裝幀:精 ...
環合·府前一號由寫字樓、精品酒店以及高端商業廣場共同組成,三大產品業態融合互動,提升共榮,於繁華中央再造繁華! 中心首發商務勢力——寫字樓 當之無愧的新市政府...
寧波環合地產有限公司於2009年09月28日在寧波市工商行政管理局鄞州分局登記成立。法定代表人周小華,公司經營範圍包括房地產開發、經營,酒店管理,物業管理,自有房屋...
羅賓遜環合反應(Robinson annulation),是Michael 加成反應後的某些產物,還可以進行分子內的羥醛縮合,這種通過分子內的羥醛縮合生成環己酮衍生物的合成稱作羅賓遜環合...
仙峰·環合中心是一個地產項目,位於寧波江東區。...... 仙峰·環合中心吸收國際前沿的設計理念,以現代簡約主義為建築外立面風格,使建築擁有簡潔、流暢的線條美感,...
自由基環合反應的理論研究,作者石景,劉滿倉指導...... 自由基環合反應的理論研究,作者石景,劉滿倉指導 副題名外文題名Theoretical studies on radical cyclization ...
左氧氟環合酯是合成左養氟沙星藥物的一個主要原料。...... 左氧氟環合酯是合成左養氟沙星藥物的一個主要原料。中文名 左氧氟環合酯 英文名 LEVOFLOXACIN ACI...
藥物合成反應指的是藥物合成中常用的有機合成反應。如:鹵化、硝化、磺化、重氮化、氧化、還原、消除、烴化、醯化、縮合、環合和重排反應等[1] 。...
環化反應(Cyclization reaction)是指在有機化合物分子中形成新的碳環或雜環的反應,也稱閉環或成環縮合。在形成碳環時,是以形成碳—碳鍵來完成環合反應的;在形成...
環化是指開鏈有機物轉化為閉環結構有機物的過程。含三個或以上雙鍵的多不飽和脂肪酸在加熱、鹼異構化與催化氫化等反應中會發生自環化,生成環化脂肪酸。如亞麻...
邃,深遠也。——《說文》 邃,深也。——《小爾雅》 閨中既邃遠兮。——《離騷》 高堂邃宇。——《楚辭·招魂》 坐潭上,四面竹樹環合,寂寥無人,淒神寒...
閉環反應,意思是有機化學中,結構上形成環,生成環合物的反應。...... 即有機化學中,結構上形成環,生成環合物的反應。包括分子內的成環和分子間的成環。開鏈化...
有些環合過程並不脫落任何小分子,這時反應物分子中要有雙鍵或三鍵。 “硫化”一詞有其歷史性,因最初的天然橡膠製品用硫磺作交聯劑進行交聯而得名,隨著橡膠工業...
近年來,在多元化發展方針的指引下,旗下擁有了寧波仙峰控股有限公司、寧波環福貿易有限公司、寧波環合地產有限公司、寧波金沃房地產開有限公司、江蘇金沃地產有限公司、...
