環加成反應,cycloaddition reaction
兩個共軛體系結合成環狀分子的一種雙分子反應。通過環加成反應,兩個共軛體系分子的端基碳原子彼此頭尾相接,形成兩個σ鍵,使這兩個分子結合成一個較大的環狀分子,例如丁二烯與乙烯(或它們的衍生物)的加成反應。
基本介紹
- 中文名:環加成反應
- 外文名:cycloaddition reaction
- 例如:丁二烯與乙烯加成反應
- 套用:分子軌道對稱守恆原理
- 屬性:反應
- 學科:化學
反應過程
反應實例


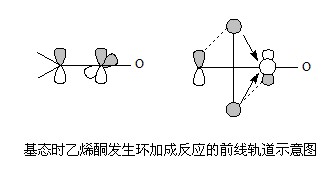

環加成反應,cycloaddition reaction
兩個共軛體系結合成環狀分子的一種雙分子反應。通過環加成反應,兩個共軛體系分子的端基碳原子彼此頭尾相接,形成兩個σ鍵,使這兩個分子結合成一個較大的環狀分子,例如丁二烯與乙烯(或它們的衍生物)的加成反應。



環加成反應,cycloaddition reaction兩個共軛體系結合成環狀分子的一種雙分子反應。通過環加成反應,兩個共軛體系分子的端基碳原子彼此頭尾相接,形成兩個σ鍵,使這兩...
加成反應是不飽和化合物類的一種特徵反應。加成反應是反應物分子中以重鍵結合的或共軛不飽和體系末端的兩個原子,在反應中分別與由試劑提供的基團或原子以σ鍵相...
(1,3-dipolar cycloaddition)是發生在1,3-偶極體和烯烴、炔烴或相應衍生物之間的環加成反應,產物是一個五元雜環化合物。烯烴類化合物在反應中稱親偶極體。德國...
周環反應是不同於離子型反應.,自由基反應的另一種叫協同反應.反應過程中,舊鍵斷裂與新鍵生成是同步的,周環反應分為:電環化反應,環加成反應,sigma遷移反應...
1,3-偶極加成:(1,3-dipolar cycloaddition)是發生在1,3-偶極體和烯烴、炔烴或相應衍生物之間的環加成反應,產物是一個五元雜環化合物。烯烴類化合物在反應中稱...
狄爾斯-阿爾德反應(Diels-Alder reaction)是一種有機反應(具體而言是一種環加成反應)。共軛雙烯與取代烯烴(一般稱為親雙烯體)反應生成取代環己烯。即使新形成的...
Bingel反應(Bingel reaction)是 C60 與溴代丙二酸酯在鹼(如氫化鈉、DBU)存在下加成為單一的 6-6 閉環產物的反應。產率較高。...
消除加成反應是一個化學反應的兩個相反過程,一般情況,它們遵循同一歷程,但起點不同、條件不同其結果也不同。...
不對稱環化反應(Asymmetric cyclization reaction),也可以稱作不對稱成環反應、手性環化反應,是一類利用分子空間結構或者手性催化劑,使原本還有對稱結構的底物形成新的...
狄爾斯-阿爾德反應(Diels-Alder reaction)是一種有機反應(具體而言是一種環加成反應)。共軛雙烯與取代烯烴(一般稱為親雙烯體)反應生成取代環己烯。即使新形成的...
普拉托反應(英語:Prato reaction)是發生在富勒烯或碳納米管與亞甲胺쭩內鹽之間的1,3-偶極環加成反應。...
在環狀有機化合物頂端一個成環碳原子再經環化,生成螺環化合物的反應。螺環化合物為抗菌劑的發展開闢了新的領域,螺環化合物的兩環平面相互垂直,對於雜環螺環...
環丙酮。是環丙烷的氧代衍生物。其熔點為-90°C,很不穩定, 可由乙烯酮與重氮甲烷在二氯甲烷中於-78℃反應製得,在-78℃以下可存在於乙醇、二氯甲烷等有機溶劑...
