多數化學反應時在常溫、定壓條件下發生的,因此用吉布斯自由能的變化來判斷反應的自發性是很方便的。有了吉布斯一亥姆霍茲方程△G=△H-T△S,並可以用△G值的正、負來判斷過程的自發性。
那么與標準摩爾生成焓一樣,可規定一套相對數值以計算體系的自由能改變數。標準摩爾生成自由能,一般是指標準摩爾生成吉布斯自由能,意為在規定溫度(T)和標準壓力p下,由穩定態單質生成1mol化合物或不穩定單質和其他形式的物質的自由能。
基本介紹
- 中文名:標準摩爾生成自由能
- 外文名:standard molar free energy of formation
- 套用學科:化學
定義

性質

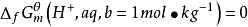
套用
查表
物質 | ΔfGΘm | 物質 | ΔfGΘm | 物質 | ΔfGΘm | 物質 | ΔfGΘm |
AgCl(s) | -109.80 | AgBr(s) | -96.9 | AgI(s) | -66.19 | Ag2O(s) | -11.2 |
Ag2CrO4(s) | -641.83 | AgNO3(s) | -33.47 | AlCl3(s) | -628.9 | Al2O3(s) | -124.4 |
BaSO4(s) | -1138 | BaCl2(s) | -810.4 | BaO(s) | -520.41 | BaCO3(s) | -1138 |
CaF2(s) | -1167 | CaCl2(s) | -748.1 | CaO | -604.04 | Ca(OH)2 | -898.56 |
CaCO3(s) | -1128.8 | CaSO4(s) | -1321.9 | CO(g) | -137.5 | CO2(g) | -386.0 |
Co(OH)2 | -454.4 | Cr2O3(s) | -1058 | CuS(s) | -53.6 | Cu2S(s) | -86.2 |
CuSO4(s) | -661.9 | CuSO4·5H2O(s) | -1880.06 | Fe2O3(s) | -742.2 | Fe3O4(s) | -1015.46 |
HCl(g) | -95.30 | HBr(g) | -53.43 | HI(g) | 1.30 | HgO(s) | -58.56 |
HgCl2(s) | -179 | Hg2Cl2(s) | -210.78 | KCl(s) | -409.2 | KI(s) | -324.89 |
判斷反應進行


